
【题目】(1)根据结构对有机物进行分类,有助于对其性质的掌握。
①下列有机物中属于芳香烃的是________(填字母),它与苯的关系是________,写出苯与溴发生反应的化学方程式:__________________________。
预测该芳香烃________(填“能”或“不能”)发生该类反应。
![]()
②下列有机物中属于羧酸类的是________(填字母)。
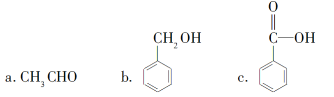
③下列有机物中属于糖类的是________(填字母)。
a.油脂 b.纤维素 c.蛋白质
(2)化合物X的结构简式为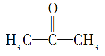 。
。
①一个X分子中有________种等效氢原子。
②X的一种同分异构体Z的结构简式为H2C===CH—CH2OH,请写出Z与Br2发生加成反应的化学方程式: ______。
【答案】c互为同系物![]() 能cb1H2C===CH—CH2OH+Br2―→BrH2C—CHBr—CH2OH
能cb1H2C===CH—CH2OH+Br2―→BrH2C—CHBr—CH2OH
【解析】
(1)①芳香烃中含苯环,只有C、H元素,苯与溴发生取代反应生成溴苯;②羧酸类物质含-COOH;
(1)①芳香烃中含苯环,只有C、H元素,a、b中不含苯环,则只有c符合,答案选c;与苯结构相似,相互1个CH2,互为同系物,苯与溴发生取代反应生成溴苯,反应的化学方程式为![]() ;预测该芳香烃能发生该类反应;②a中含-CHO,b中含-OH,c中含-COOH,则c属于羧酸类,故答案为:c;③纤维素是多糖,属于糖类,答案选b;(2)①该分子结构对称,分子中只有1种氢原子;②Z与Br2发生加成反应的化学方程式为H2C=CH—CH2OH+Br2―→BrH2C—CHBr—CH2OH。
;预测该芳香烃能发生该类反应;②a中含-CHO,b中含-OH,c中含-COOH,则c属于羧酸类,故答案为:c;③纤维素是多糖,属于糖类,答案选b;(2)①该分子结构对称,分子中只有1种氢原子;②Z与Br2发生加成反应的化学方程式为H2C=CH—CH2OH+Br2―→BrH2C—CHBr—CH2OH。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体d呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
a(干燥气体) | b(液体) |
| |
A | NO | 水 | |
B | CO2 | 饱和NaHCO3溶液 | |
C | Cl2 | 饱和NaCl溶液 | |
D | NH3 | 1 mol·L-1盐酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
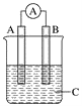
A.A是Cu,B是Zn,C为硫酸铜
B.A是Cu,B是Zn,C为稀硫酸
C.A是Fe,B是Ag,C为稀AgNO3溶液
D.A是Ag,B是Fe,C为稀AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年10月15日,中国用“长征三号乙”运载火箭成功以“一箭双星”方式发射北斗三号全球组网卫星系统第15、16号卫星,其火箭推进剂为高氯酸铵(NH4ClO4)等。制备NH4ClO4的工艺流程如下:
饱和食盐水![]() NaClO3
NaClO3![]() NaClO4
NaClO4![]() NaClO4
NaClO4![]() NH4ClO4
NH4ClO4
下列说法错误的是( )
A. NH4ClO4属于离子化合物
B. 溶解度:NaClO4>NH4ClO4
C. 该流程中可循环利用的物质是NH4Cl
D. 高氯酸铵中氯元素的化合价为+7价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg):
M2+(g)+CO32-(g) ![]() M2+(g)+O2(g)+CO2(g)
M2+(g)+O2(g)+CO2(g)
![]()
![]()
![]()
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
A. ΔH1(MgCO3)>ΔH1(CaCO3)>0
B. ΔH2(MgCO3)=ΔH2(CaCO3)>0
C. ΔH1(CaCO3)-ΔH1(MgCO3)=ΔH3(CaO)-ΔH3(MgO)
D. 对于MgCO3和CaCO3,ΔH1+ΔH2>ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知:CH4(g)+2H2S(g)![]() CS2(g)+4H2(g)。向恒容密闭容器中充入0.lmolCH4和0.2molH2S,如图所示:
CS2(g)+4H2(g)。向恒容密闭容器中充入0.lmolCH4和0.2molH2S,如图所示:
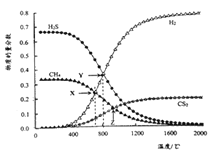
下列说法不正确的是
A.该反应的△H>0
B.X点CH4的转化率为20%
C.X点与Y点容器内压强比为55:51
D.维持Z点温度,向容器中再充入CH4、H2S、CS2、H2各0.1mol时v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1mol CO2和2.7g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
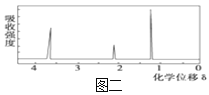
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1∶2∶3;
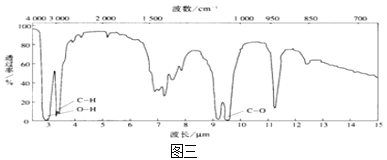
④用红外光谱仪处理该化合物,得到如图三所示图谱。
试回答下列问题:

(1)有机物A的相对分子质量是___________;
(2)有机物A的实验式是___________;
(3)推测有机物A的结构简式为___________,A中含官能团的名称是_________;
(4)质量分数为11.6%的某饱和一元醛水溶液5 g,跟足量新制的Cu(OH)2悬浊液反应,生成Cu2O1.44 g。通过计算推导出该有机物的分子式并写出其结构简式_______、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室为测定一新配的稀盐酸的准确浓度。通常用纯净的Na2CO3(无水)配成标准溶液进行滴定。具体操作是:称取W克纯净无水Na2CO3装入锥形瓶中,加适量的蒸馏水溶解。在酸式滴定管中加入待测盐酸滴定。
(1)由于CO2溶在溶液中会影响pH值,为准确滴定,终点宜选在pH值4—5之间,那么在石蕊、甲基橙、酚酞三种指示剂中应选用___。当滴定至溶液由___时,即表示到达终点。
(2)若达到滴定终点时,中和W克Na2CO3消耗盐酸V毫升,则盐酸的物质的量的浓度为___mol/L。
(3)若所称取的Na2CO3不纯,则测得盐酸的浓度就不准确。现设盐酸的准确浓度为c1mol/L,用不纯的Na2CO3标定而测得盐酸浓度为c2mol/L。在下述情况下,c1与c2的关系是(填“>”或“<”或“=”):
①当Na2CO3中含有NaHCO3时,则c1___c2。
②当Na2CO3中含有NaOH时,则c1___c2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的强氧化剂,工业上常用铬铁矿(主要成分是亚铬酸亚铁Fe(CrO2)2,还有硅、铝等杂质)为主要原料生产重铬酸钾(K2Cr2O7),主要工艺流程如图:

(1)步骤①中主要反应的化学方程式___。
(2)步骤③中沉淀是___(填化学式)
(3)步骤④中反应的离子方程式为___。
(4)有关物质的溶解度如图所示。
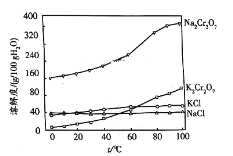
步骤⑤加氯化钾固体后的具体实验操作为___。经洗涤、干燥得到K2Cr2O7晶体样品,得到的样品中含有少量的NaCl等杂质,洗涤晶体适宜选用的试剂为___。
a.冷水 b.75%乙醇 c.四氯化碳
(5)向一支试管中加入H2O2溶液、乙醚、稀硫酸溶液和几滴K2Cr2O7溶液,经反应后发现上层为蓝色的CrO5乙醚溶液。CrO5中铬的化合价为+6价,求-2价和-1价氧的个数比为___,一段时间后,蓝色逐渐消失,其反应的离子方程式为4CrO5+12H+=4Cr3++7O2↑+6H2O,消耗1mol的CrO5转移电子的物质的量为___mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com