
【题目】为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1mol CO2和2.7g水;
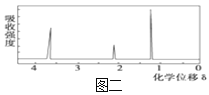
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1∶2∶3;
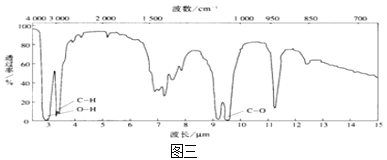
④用红外光谱仪处理该化合物,得到如图三所示图谱。
试回答下列问题:

(1)有机物A的相对分子质量是___________;
(2)有机物A的实验式是___________;
(3)推测有机物A的结构简式为___________,A中含官能团的名称是_________;
(4)质量分数为11.6%的某饱和一元醛水溶液5 g,跟足量新制的Cu(OH)2悬浊液反应,生成Cu2O1.44 g。通过计算推导出该有机物的分子式并写出其结构简式_______、________。
【答案】46 C2H6O CH3CH2OH 羟基 C3H6O CH3CH2CHO
【解析】
(1)根据质谱图(图一)分析判断;
(2)根据n=![]() 计算生成的水的物质的量,再计算碳元素、氢元素的质量,根据质量守恒判断有机物A是否含有氧元素,若含有氧元素,计算氧元素质量、氧原子物质的量,根据原子守恒确定有机物A中C、H、O原子个数比值确定最简式;
计算生成的水的物质的量,再计算碳元素、氢元素的质量,根据质量守恒判断有机物A是否含有氧元素,若含有氧元素,计算氧元素质量、氧原子物质的量,根据原子守恒确定有机物A中C、H、O原子个数比值确定最简式;
(3)根据图二、三可知,结合化学式分析写出结构简式;
(4)饱和一元醛与新制的Cu(OH)2悬浊液反应关系为R-CHO~Cu2O,根据Cu2O的质量结合反应关系分析计算。
(1)根据质谱图(图一)的质荷比可知,有机物A的相对分子质量为46,故答案为:46;
(2)2.3g有机物燃烧生成0.1molCO2,2.7g水,则n(C)=n(CO2)=0.1mol,m(C)=0.1mol×12g/mol=1.2g,n(H2O)=![]() =0.15mol,n(H)=0.3mol,m(H)=0.3mol×1g/mol=0.3g,则m(C)+m(H)=1.2g+0.3g=1.5g<2.3g,故有机物含有O元素,且m(O)=2.3g-1.5g=0.8g,故n(O)=
=0.15mol,n(H)=0.3mol,m(H)=0.3mol×1g/mol=0.3g,则m(C)+m(H)=1.2g+0.3g=1.5g<2.3g,故有机物含有O元素,且m(O)=2.3g-1.5g=0.8g,故n(O)=![]() =0.05mol,n(C)∶n(H)∶n(O)=0.1mol∶0.3mol∶0.05mol=2∶6∶1,即该有机物最简式为:C2H6O,故答案为:C2H6O;
=0.05mol,n(C)∶n(H)∶n(O)=0.1mol∶0.3mol∶0.05mol=2∶6∶1,即该有机物最简式为:C2H6O,故答案为:C2H6O;
(3)由图三可知,该有机物分子中含有O-H键、C-O键和C-H键,其分子式为C2H6O,故该有机物结构式为:CH3CH2OH,满足核磁共振氢谱三个峰的面积之比是1∶2∶3,含有的官能团为羟基,故答案为:CH3CH2OH;羟基;
(4)设该饱和一元醛的结构简式为R-CHO,质量分数为11.6%的某饱和一元醛水溶液5g,醛的质量为11.6%×5g=0.58g,n(Cu2O)=![]() =0.01mol,根据R-CHO~Cu2O可知n(R-CHO)=0.01mol,所以醛的相对分子质量为
=0.01mol,根据R-CHO~Cu2O可知n(R-CHO)=0.01mol,所以醛的相对分子质量为![]() =58,则R的式量为58-29=29,R为-CH2CH3,则该有机物的分子式为C3H6O,结构简式为CH3CH2CHO,故答案为:C3H6O;CH3CH2CHO。
=58,则R的式量为58-29=29,R为-CH2CH3,则该有机物的分子式为C3H6O,结构简式为CH3CH2CHO,故答案为:C3H6O;CH3CH2CHO。


科目:高中化学 来源: 题型:
【题目】锌电池是一种极具前景的电化学储能装置。![]() 扣式可充电电池组成示意图如下。
扣式可充电电池组成示意图如下。![]() 可以在
可以在![]() 晶体中可逆地嵌入和脱除,总反应为
晶体中可逆地嵌入和脱除,总反应为![]() 。下列说法错误的是( )
。下列说法错误的是( )
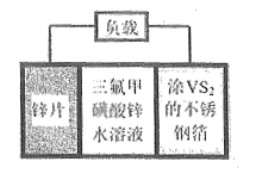
A. 放电时不锈钢箔为正极,发生还原反应
B. 放电时负极的反应为![]()
C. 充电时电池正极上的反应为:![]()
D. 充电时锌片与电源的负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关如图所示的说法正确的是

A. 图甲中开关置于N处时铜锌合金腐蚀的速率增大
B. 图乙中接通开关时,锌腐蚀的速率增大,锌上放出气体的速率增大
C. 图丙中接通K2时铁棒不被腐蚀,属于牺牲阳极保护法
D. 图丙中接通K1时,石墨棒周围溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据结构对有机物进行分类,有助于对其性质的掌握。
①下列有机物中属于芳香烃的是________(填字母),它与苯的关系是________,写出苯与溴发生反应的化学方程式:__________________________。
预测该芳香烃________(填“能”或“不能”)发生该类反应。
![]()
②下列有机物中属于羧酸类的是________(填字母)。
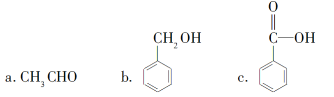
③下列有机物中属于糖类的是________(填字母)。
a.油脂 b.纤维素 c.蛋白质
(2)化合物X的结构简式为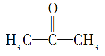 。
。
①一个X分子中有________种等效氢原子。
②X的一种同分异构体Z的结构简式为H2C===CH—CH2OH,请写出Z与Br2发生加成反应的化学方程式: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
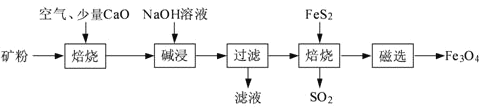
(1)粉碎高硫铝土矿石的目的是___。
(2)第一次焙烧时发生氧化还原反应:___。
(3)碱浸时发生反应的化学方程式为___。
(4)过滤后向滤液中通入过量的CO2气体,反应的离子方程式为___;___。
(5)“过滤”得到的滤渣中含有大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应2A(g)![]() B(g) ΔH>0,在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够长时间后反应再次达到平衡状态,此时c(A)/c(B=b,下列叙述正确的是( )
B(g) ΔH>0,在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够长时间后反应再次达到平衡状态,此时c(A)/c(B=b,下列叙述正确的是( )
A. 在该温度下,保持容积固定不变,向容器内补充了B气体,则a<b
B. 若a=b,则容器中可能使用了催化剂
C. 若其他条件不变,升高温度,则a<b
D. 若保持温度、压强不变,充入惰性气体,则a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硫及其化合物的说法正确的是( )
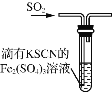
A.浓硫酸具有脱水性,可用于干燥氨气
B.加氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有![]()
C.二氧化硫能使溴水、酸性高锰酸钾溶液褪色,因其有漂白性
D.如图装置中血红色褪去,可以验证 SO2 的还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易水解,其中:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑,下列推测正确的是( )
A. XeF2分子中各原子均达到8电子稳定结构
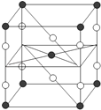
B. 某种氟化氙的晶体结构单元如右图,可推知其化学式为XeF2
C. XeF4按已知方式水解,每生成3molO2,共转移12mol电子
D. XeF2加入水中,在水分子作用下将重新生成Xe和F2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取乙酸乙酯的装置。请回答:
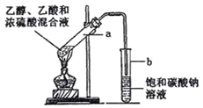
(1)检验该装置气密性的方法是___________________。
(2)浓硫酸的作用是__________。
(3)下列有关该实验的说法中,正确的是___________。
A.向a试管中加入沸石,作用是防止加热时液体暴沸
B.饱和碳酸钠溶液可以除去产物中混有的乙酸
C.乙酸乙酯是一种无色透明、密度比水大的油状液体
D.若原料为CH3COOH 和 CH3CH218OH,则乙酸乙酯中含有18O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com