
【题目】工业废电路板的铜常用FeCl3溶液来溶解处理回收。现将一块电路板浸泡在100 mLFeCl3溶液中使铜全部溶解(电路板上其他物质均不发生反应),测得电路板质量减少了3.2 g,在浸泡液中加足量的Fe粉并使之充分反应,过滤干燥固体,固体质量比加入的Fe粉质量减少了2.4g。
请计算:
(1)浸泡液中的溶质是__________(写化学式) 。
(2)参与反应的铁的质量是__________g。
(3)假设溶液的体积不变,最后所得溶液中c(Fe2+)=__________mol·L-1。
【答案】FeCl3、FeCl2、CuCl2 5.6 3
【解析】
铜与FeCl3溶液反应会生成FeCl2与CuCl2,发生的化学反应为:①Cu+2Fe3+=2Fe2++Cu2+;加入铁粉后发生的反应有:②Fe+2Fe3+=3Fe2+;③Fe+Cu2+=Cu+Fe2+;根据元素守恒法及物质之间的转化关系分析作答。
(1)铜与FeCl3溶液反应会生成FeCl2与CuCl2,发生的化学反应为:①Cu+2Fe3+=2Fe2++Cu2+,电路板质量减少了3.2 g,则参与反应的铜的质量为3.2g,铜的物质的量n(Cu)=![]() =0.05mol,生成的Fe2+的物质的量n1(Fe)= 2n(Cu)=0.1mol;在浸泡液中加足量的Fe粉并使之充分反应,过滤干燥固体,固体质量比加入的Fe粉质量减少了2.4g。若铁粉只与生成的氯化铜反应会生成铜单质与氯化亚铁,则固体质量会增加,可见浸泡液中还有反应剩余的氯化铁,因此浸泡液的溶质有FeCl3、FeCl2、CuCl2,故答案为:FeCl3、FeCl2、CuCl2;
=0.05mol,生成的Fe2+的物质的量n1(Fe)= 2n(Cu)=0.1mol;在浸泡液中加足量的Fe粉并使之充分反应,过滤干燥固体,固体质量比加入的Fe粉质量减少了2.4g。若铁粉只与生成的氯化铜反应会生成铜单质与氯化亚铁,则固体质量会增加,可见浸泡液中还有反应剩余的氯化铁,因此浸泡液的溶质有FeCl3、FeCl2、CuCl2,故答案为:FeCl3、FeCl2、CuCl2;
(2)加入铁粉后发生的反应有:②Fe+2Fe3+=3Fe2+,③Fe+Cu2+=Cu+Fe2+,根据铜元素守恒可知,参加反应的铜的物质的量为0.05mol,与铜反应时固体质量增加为x g,则
Fe+Cu2+=Cu+Fe2+ △m
56 64 8
3.2 x
解得x=0.4
该反应生成的Fe2+的物质的量为n3(Fe2+)= n(Cu2+)= n(Cu)=0.05mol
反应的Fe的质量m3(Fe)=0.05mol![]() 56g/mol=2.8g
56g/mol=2.8g
则反应②中固体质量减少应为2.4g+0.4g=2.8g,即消耗的Fe粉的质量m2(Fe)=2.8g,总的消耗的铁粉的质量m(Fe)= m3(Fe)+ m3(Fe)=2.8g+2.8g=5.6g,故答案为:5.6;
(3)上述反应②Fe+2Fe3+=3Fe2+中n2(Fe)=![]() =0.05mol,根据关系式Fe
=0.05mol,根据关系式Fe![]() 3Fe2+可得生成的Fe2+的物质的量为n2(Fe2+)=3n2(Fe)=0.15mol,那么总的Fe2+的物质的量= n1(Fe2+)+ n2(Fe2+)+ n3(Fe2+)=0.1mol+0.15mol+0.05mol=0.3mol,则c(Fe2+)=
3Fe2+可得生成的Fe2+的物质的量为n2(Fe2+)=3n2(Fe)=0.15mol,那么总的Fe2+的物质的量= n1(Fe2+)+ n2(Fe2+)+ n3(Fe2+)=0.1mol+0.15mol+0.05mol=0.3mol,则c(Fe2+)=![]() =3mol/L,故答案为:3。
=3mol/L,故答案为:3。


科目:高中化学 来源: 题型:
【题目】已知Cu、Ag都能溶解在硝酸中,某同学设计如下实验测量m g铜银合金样品中铜的质量分数,下列说法中正确的是( )
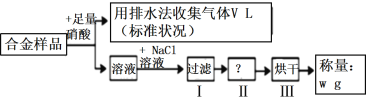
A. 被Cu还原的硝酸为![]() molB. 操作I所用到的玻璃仪器是烧杯、蒸发皿、玻璃棒
molB. 操作I所用到的玻璃仪器是烧杯、蒸发皿、玻璃棒
C. 操作Ⅱ为蒸发D. 铜的质量分数为![]() ×100%
×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中不能使酸性KMnO4溶液褪色的是( )
①乙烯 ②苯 ③乙醇 ④甲烷 ⑤乙酸 ⑥二氧化硫
A.①②③④⑤B.②④⑤C.②④⑤⑥D.①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1996年诺贝尔化学奖授于斯莫利等三位化学家,以表彰他们发现富勒烯(C60)开辟了化学研究的新领域。后来,人们又发现了一种含碳量极高的链式炔烃──棒碳,它是分子中含300~500个碳原子的新物质,其分子中只含有交替连接的单键和叁键。对于C60与棒碳,下列说法正确的是
A.C60与棒碳中所有的化学键都是非极性共价键
B.棒碳不能使溴水褪色
C.C60在一定条件下可能与CuO发生置换反应
D.棒碳与乙炔互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液加入铝可以产生H2,则在该溶液中可能大量存在的离子组是
A. Na+、Fe3+、SO42-、SCN- B. K+ 、Na+、AlO2-、Cl-
C. K+ 、Na+、I-、MnO4- D. Na+、K+、HCO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况.试判断,违反了泡利原理的是_____,违反了洪特规则的是______。
![]()
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为________;其最高价氧化物对应水化物的化学式是________。
(3)用符号“>”“<”或“=”表示下列各项关系。
①第一电离能:Na________Mg,Mg________Ca。
②电负性:O________F,F________Cl。
③能量高低:ns________(n+1)s,ns________np。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物虽然种类繁多,但其命名是有规则的。下列有机物的命名正确的是( )
A. ![]() 1,4一二甲基丁烷 B.
1,4一二甲基丁烷 B. ![]() 3-甲基丁烯
3-甲基丁烯
C. HOOC-CH2-COOH丙二酸 D. CH2Cl-CH2Cl二氯乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化钛是生产金属钛及其化合物的重要中间体。某校化学课外活动小组准备利用下图装置制备四氯化钛(部分夹持仪器已略去)。

资料表明:室温下,四氯化钛为无色液体,熔点:-25 ℃,沸点:136.4 ℃。在空气中发烟生成二氧化钛固体。在650~850 ℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。回答下列问题:
(1)检查该装置气密性的方法是_______________________________________________。
(2)实验中B装置的作用是____________________。
(3)写出D装置中物质制备的化学方程式________________________________;写出四氯化钛在空气中发烟的化学方程式______________________________。
(4)E处球形冷凝管的冷却水应从________(填“c”或“d”)口通入。
(5)F装置中盛装的物质是________。
(6)该实验设计略有缺陷,请指出其不足之处:______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com