
【题目】某溶液中含有较大量的Cl-、CO![]() 、OH-三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序中,正确的是( )
、OH-三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序中,正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③B.④②③②①
C.①②③②④D.④②①②③
【答案】D
【解析】
检验氯离子用AgNO3溶液;检验氢氧根离子可用Mg(NO3)2溶液;检验碳酸根离子可用Ba(NO3)2溶液;
由于碳酸根离子能与AgNO3溶液、Mg(NO3)2溶液反应,分别生成Ag2CO3沉淀、MgCO3沉淀,故要先检验碳酸根离子,再检验氢氧根离子、氯离子,由于氢氧根离子与银离子结合成的AgOH极不稳定,故要先检验氢氧根离子。仅用一份样品溶液,可先滴加Ba(NO3)2溶液产生白色沉淀,说明含有碳酸根离子;过滤,向滤液中再滴加Mg(NO3)2溶液产生白色沉淀,说明含有氢氧根离子;过滤,再向滤液中再滴加AgNO3溶液,产生白色沉淀,说明含有氯离子;综上所述,正确的实验操作顺序是④②①②③。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】已知H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的物质的量分数(分布系数)δ随溶液pH变化的关系如图所示,下列说法正确的是
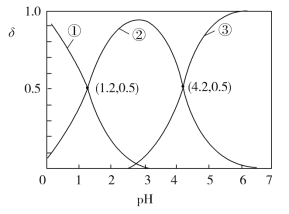
A.曲线①代表的粒子是HC2O4-
B.H2C2O4的Ka1=-1.2
C.向草酸溶液中滴加KOH溶液至pH=4.2:c(K+)<3c(C2O42-)
D.浓度均为0.01 mol·L1的草酸与KOH溶液等体积混合并充分反应得到的溶液:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯与HCl加成可能发生反应①和②,其能量与反应进程如图所示:下列说法正确的是
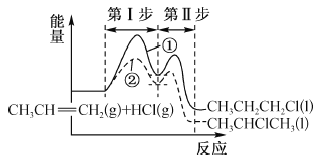
A. CH3CHClCH3 比 CH3CH2CH2Cl 稳定
B. 反应①的第I步与第Ⅱ步均放出能量
C. 反应②的第I步比第Ⅱ步反应速率快
D. 活化能反应①比②的大,反应①更易进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)广泛用于电镀、鞣制皮革、棉织品漂白后的脱氯剂等。某实验小组的同学以Na2S和SO2为原料制备Na2S2O3。回答下列问题:
(1)制备Na2S溶液
①Na2S溶液呈碱性,原因是____________________________(用离子方程式表示)。
②工业品硫化钠中常含有少量Na2SO4和Na2CO3,需进行纯化,他们将硫化钠溶于水,然后加入适量的_____________(填化学式)溶液充分搅拌并过滤,再精制得Na2S溶液。
(2)利用下图装置制备Na2S2O3
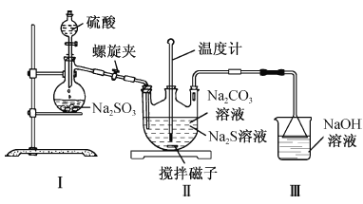
①装置Ⅰ中反应的化学方程式为___________________________________。
②实验过程中打开螺旋夹并调节螺旋夹至适当的位置,一方面使反应产生的SO2气体较均匀地通入Na2S—Na2CO3溶液中,另一方面的作用是______________________________。
③三口烧瓶内生成Na2S2O3的化学方程式为;____________________________________;装置Ⅲ的作用是_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定容积的密闭容器中通入amolN2与bmolH2的混合气体,保持温度不变,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
(1)若反应到某时刻t时,n(N2)=9mol,n(NH3)=2mol,则a=____mol;
(2)反应达平衡时,混合气体的体积为448L(标况下),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量____;
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比、下同),n(始)∶n(平)=____;
(4)原混合气体中,a∶b=_____;
(5)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列物质的结构简式:
(1)2,4,6-三甲基-5-乙基辛烷:________________________________;
(2)3-甲基-1-戊炔:______________________________;
(3)1,4-戊二烯:______________________________;
(4)苯乙烯:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对一种未知有机物的结构测定,往往需要多种复杂方法相结合,一般来说,主要包括以下几个方面:①相对分子质量;②元素组成(种类和比例);③该有机物的各种性质的研究;④结构的确定。
(1)相对分子质量的确定一般有质谱法,蒸气密度法等。蒸气密度法是指一定条件下将有机物气化,测定该条件下的密度,利用气态方程式计算相对分子质量。蒸气密度法的要求是该有机物在______。如果沸点过高,可以采用________方法。质谱法是在一定条件下让有机物失去电子变成阳离子,测其相对分子质量。该过程中,复杂的有机物分子往往变成小的片断,如C4H10断裂成CH3CH2CH2+、CH3CH2+、CH3+、CH3CH2CH2CH2+等,其式量最大的就是其相对分子质量。该法测定某有机物A质谱中显示相对分子质量最大是72。
(2)组成元素的测定往往采用元素分析仪,以前也常用燃烧法。称取3.6 gA,跟足量氧气充分燃烧后通过浓硫酸,浓硫酸增重5.4 g,剩余气体通过碱石灰,碱石灰增重11 g,则该有机物的分子式为________。
(3)核磁共振谱常用氢谱和碳谱,它主要测定分子中具有不同特点的C或H的种类与比例。如对于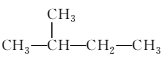 ,经测定,C谱有四个峰,其数值高低比例为2∶1∶1∶1;H谱有四个峰,其数值高低比例为1∶2∶3∶6。有机物A碳谱有两个峰,峰高比为4∶1。氢谱有一个峰。试写出有机物A的结构简式________。
,经测定,C谱有四个峰,其数值高低比例为2∶1∶1∶1;H谱有四个峰,其数值高低比例为1∶2∶3∶6。有机物A碳谱有两个峰,峰高比为4∶1。氢谱有一个峰。试写出有机物A的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同条件下进行化学反应2A(g)=B(g)+D(g),B、D起始浓度均为0,反应物A的浓度(mol/L)随反应时间的变化情况如下表:
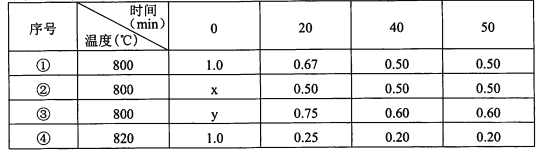
下列说法不正确的是
A.①中B在0~20 min平均反应速率为8.25xl0-3moI.L-l.min-l
B.②中K=0.25,可能使用了催化剂
C.③中y= 1.4 moI.L-l
D.比较①、④可知,该反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“NaH2PO2还原法”制备高纯度氢碘酸和亚磷酸钠(Na2HPO3)的工业流程如图。
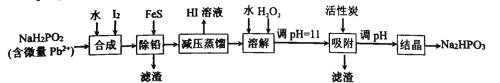
已知:25℃时,H3PO3的pKa1=1.3,pKa2=6.6。
(1)“合成”过程,主要氧化产物为H3PO3,相应的化学方程式为______________
(2)“除铅”过程,FeS除去微量Pb2+的离子方程式为______________。
(3)“减压蒸馏”过程,I-回收率为95%,则剩余固体的主要成分为____(填化学式)。
(4)“调pH=11”的作用是______________。
(5)若“结晶”前溶液中Na2HPO3的浓度为0.1mol.L-1,则“吸附”处理后,应调节溶液pH至______________(填数值)。
(6)氢碘酸也可以用“电解法”制备,装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-;A、B为离子交换膜。
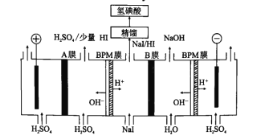
①B膜最佳应选择______________
②阳极的电极反应式是____。
③少量的I一因浓度差通过BPM膜,若撤去A膜,其缺点是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com