
����Ŀ����~��Ϊ������Ԫ�أ��䳣�����ϼ���ԭ�������Ĺ�ϵ����ͼ��ʾ����ش��������⡣
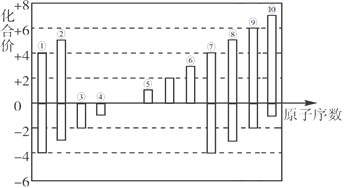
��1��������ļ����Ӱ뾶�ɴ�С��˳��Ϊ_______�������ӷ��ţ���
��2��������Ԫ���γɵ����ȶ�����õ���̬�⻯��ĵ���ʽΪ_______��
��3���ڵļ��⻯����������������ˮ������Է������Ϸ�Ӧ�����ò����а����Ļ�ѧ������Ϊ_________________��
��4��������������������ˮ���������________��________���ѧʽ����
��5��д���ĵ��ʺ͢ݵ�����������Ӧˮ�����ˮ��Һ֮�䷴Ӧ�����ӷ���ʽ��_______________________________________________��
���𰸡� Cl-��F- ![]() ���Ӽ� ���Լ� HClO4��H3PO4 2Al+2OH-+2H2O=2AlO2-+3H2��
���Ӽ� ���Լ� HClO4��H3PO4 2Al+2OH-+2H2O=2AlO2-+3H2��
����������ͼ�л��ϼۿ�֪���۵Ļ��ϼ�ֻ��-2�ۣ�û�������ϼۣ��ʢ�ΪOԪ�أ��ٵĻ��ϼ�Ϊ+4��-4�ۣ���ΪCԪ�أ����ΪN����ΪF����ֻ��+1�ۣ�ΪNa���١��ߵĻ��ϼ���ͬ���١���λ��ͬ���壬���ΪSi������Al������P����ΪSԪ�أ�����������Ϊ+7��ԭ������������ΪCl����1��ͬ������ϵ������Ӱ뾶�����ܡ���ļ����Ӱ뾶�ɴ�С��˳��ΪCl-��F-����2��������Ԫ���γɵġ��ȶ�����õ���̬�⻯����HF������ʽΪ![]() ����3���ڵļ��⻯�ﰱ����������������ˮ����������Է������Ϸ�Ӧ��������泥����ò����а����Ļ�ѧ������Ϊ���Ӽ������Լ�����4���ǽ�����Խǿ����ۺ����������Խǿ����Ԫ�طǽ�����ǿ����Ԫ�أ��ࡢ�������������ˮ���������ǿ��˳����HClO4��H3PO4����5�������ʺ͢ݵ�����������Ӧˮ�����ˮ��Һ��������֮�䷴Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O��2AlO2-+3H2����
����3���ڵļ��⻯�ﰱ����������������ˮ����������Է������Ϸ�Ӧ��������泥����ò����а����Ļ�ѧ������Ϊ���Ӽ������Լ�����4���ǽ�����Խǿ����ۺ����������Խǿ����Ԫ�طǽ�����ǿ����Ԫ�أ��ࡢ�������������ˮ���������ǿ��˳����HClO4��H3PO4����5�������ʺ͢ݵ�����������Ӧˮ�����ˮ��Һ��������֮�䷴Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O��2AlO2-+3H2����


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ʵı��治��ȷ����
A. AgNO3��ҺӦ��������ɫƿ�� B. Ũ����Ҫ�ܷⱣ��
C. Һ�ȿ��Ա����ڸ���ĸ�ƿ�� D. Ư��¶���ڿ����б���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӱ��ӵ��Ҵ���Һ�л��ձ���������8�ֿɹ�ѡ��IJ��������к����IJ����ǣ� ��
������ �ڹ��� �۾��÷�Һ �ܼ������������� ��ͨ������CO2 ��������NaOH��Һ ����������Ũ������Һ���� ��������������Ȼ�����Һ��
A.�ܢݢ�
B.�ߢ�
C.��
D.�ޢ٢ݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��������ͼ��ʾ��װ�ý����Ҵ��Ĵ�����ʵ�鲢��ȡ��ȩ���Թܱ�����ˮ���ղ����ͼ������̨�ȹ̶�װ������ȥ��ʵ��ʱ���ȼ��Ȳ������е�ͭ˿��Լ1min��������������д���пհף�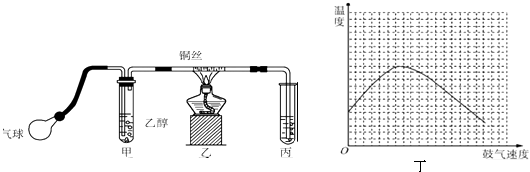
��1��������ȩ���Լ���������ĸ����
A.������Һ
B.̼��������Һ
C.����Cu��OH��2
D.����ͭ
��2���Ҵ�������������Ӧ�Ļ�ѧ����ʽΪ�� ��
��3��ʵ��ʱ����������װ�ý���70��80���ˮԡ�У�Ŀ���� �� ����װ������ϵ�ȱ�ݣ�ʵ�����ʱ���ܻ� ��
��4����Ӧ��������ȥ�ƾ��ƣ����÷�Ӧ�����ų���������ά�ַ� Ӧ�������У���һ���о������������ٶ��뷴Ӧ��ϵ���¶ȹ�ϵ������ͼ����ʾ���Խ������ٶȹ��죬��Ӧ��ϵ�¶ȷ����½���ԭ�� �� ��ʵ���С������ٶȡ���һ��������Ϊ������������
��5���ÿ���С��żȻ��������ˮ�м�����ȩ��Һ����ˮ��ɫ����ͬѧΪ������������������ֲ��룺����ˮ����ȩ����Ϊ�������ˮ����ȩ�����ӳɷ�Ӧ���������һ����ʵ�飬̽����һ�ֲ�����ȷ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ�����ӻ�����KW���¶�t���棩�Ĺ�ϵ��ͼ��ʾ��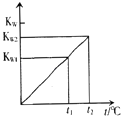
��1����t1=25�棬��KW1=����t2=100��ʱ��KW2=10��12 �� ��0.05molL��1��Ba��OH��2��Һ��pH= ��
��2����֪25��ʱ��0.1L0.1molL��1��NaA��Һ��pH=10����NaA��Һ�������ڵĻ�ѧƽ���У������ӷ���ʽ��ʾ���� �� ��Һ�и����ӵ����ʵ���Ũ���ɴ�С��˳��Ϊ ��
��3��25��ʱ����pH=11��NaOH��Һ��pH=4��������Һ��ϣ������û����ҺpH=9����NaOH��Һ��������Һ�������Ϊ ��
��4��100��ʱ����10�����ijǿ����Һ��1�����ijǿ����Һ��Ϻ���Һ�����ԣ�����֮ǰ����ǿ���pH��pH������ǿ���pH��pH����֮��Ӧ����Ĺ�ϵΪ��pH���ᣩ+pH���= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У������ʷ����ǰ�ߴ����ں��ߵ�һ���ǣ� ��
A. ������������B. ���������������
C. �ᡢ�����D. �������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼ����ɽ������ᷴӦ��ã�Ҳ��ͨ��������������Ӧ��õ���
A. CuCl2 B. FeCl2 C. FeCl3 D. AlCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������ǿ���������� ��
A. Ag��B. Mg2��C. H��D. Cu2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20mL0.2molL��1H2C2O4��Һ�еμ�0.2molL��1NaOH��Һ���й������ʵ����ı仯��ͼ������I����H2C2O4 �� �����HC2O ![]() �������C2O
�������C2O ![]() ��������ͼʾ�жϣ�����˵����ȷ���ǣ� ��
��������ͼʾ�жϣ�����˵����ȷ���ǣ� �� 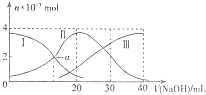
A.H2C2O4��ˮ�еĵ��뷽��ʽ�ǣ�H2C2O4?2H++C2O ![]()
B.��V��NaOH��=20mLʱ����Һ��ˮ�ĵ���̶ȱȴ�ˮС
C.��V��NaOH��=30mLʱ����Һ�д������¹�ϵ��2c��H+��+2c��HC2O ![]() ��+3c��H2C2O4���Tc��C2O
��+3c��H2C2O4���Tc��C2O ![]() ��+2c��OH����
��+2c��OH����
D.��֪H2C2O4�ĵ��볣���ֱ�ΪK1��K2 �� ��a���c��H+��=K2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com