
【题目】下列离子哪种是最强的氧化剂( )
A. Ag+B. Mg2+C. H+D. Cu2+
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的叙述正确的是( )
A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序:c(Cl﹣)>c(NH ![]() )>c(H+)=c(OH﹣)
)>c(H+)=c(OH﹣)
B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①~⑩为短周期元素,其常见化合价与原子序数的关系如下图所示。请回答下列问题。
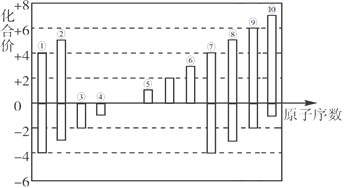
(1)④、⑩的简单离子半径由大到小的顺序为_______(填离子符号)。
(2)由上述元素形成的、稳定性最好的气态氢化物的电子式为_______。
(3)②的简单氢化物与其最高价氧化物的水化物可以发生化合反应,所得产物中包含的化学键类型为_________________。
(4)⑧、⑩的最高价氧化物的水化物的酸性________>________(填化学式)。
(5)写出⑥的单质和⑤的最高价氧化物对应水化物的水溶液之间反应的离子方程式:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NH3和HCl都是能用来做喷泉实验的气体.若在同温同压下用等体积烧瓶一个收集满NH3 , 另一个收集HCl和N2的混合气体,如图所示.喷泉实验停止后,两个烧瓶内溶液的关系是(不考虑烧瓶内溶质的扩散,氨水的溶质按NH3计算)( ) 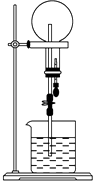
A.溶质的物质的量浓度相同、溶质的质量分数不同
B.溶质的质量分数相同、溶质的物质的量浓度不同
C.溶质的物质的量浓度和溶质的质量分数都不同
D.溶质的物质的量浓度和溶质的质量分数都相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的说法正确的是( )
A.在正极上发生氧化反应
B.化学性质较活泼的金属为负极
C.在外电路,电子流出正极
D.是由电能转化为化学能的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,科学家研制了一种间距为50 nm的“镊子”,利用它可以操控活细胞中的DNA分子等。下列分散系中分散质的粒子直径与该“镊子”间距相近的是( )。
A.溶液B.胶体C.悬浊液D.乳浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列盐类水解的离子方程式,并指出其溶液的酸碱性.
(1)硫酸铝溶液:(显性).
(2)硝酸铵溶液:(显_性).
(3)次氯酸钠溶液:(显性).
(4)碳酸氢钠溶液:(显性).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5 , 依次发生的分解反应为①N2O5(g)N2O3(g)+O2(g),②N2O3(g)N2O(g)+O2(g);在2L密闭容器中充入6mol N2O5 , 加热到t℃,达到平衡状态后O2为8mol,N2O3为3.2mol.则t℃时反应①的平衡常数为( )
A.10.7
B.8.5
C.32
D.64
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外活动小组为了验证元素非金属性递变规律,设计了如图所示的两套实验方案(图1和图2)进行实验探究:
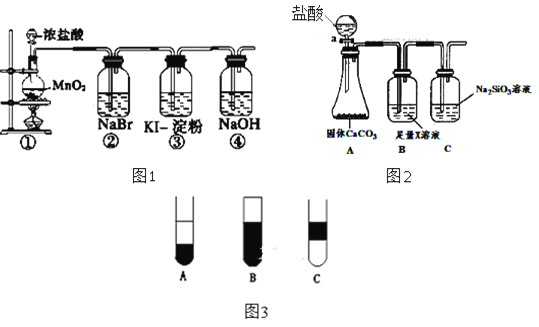
(1)根据方案一装置(图1)回答以下问题:
Ⅰ.写出装置①发生的化学反应方程式:______。
Ⅱ.若将反应后②中的溶液倒入CCl4中,出现的现象与图3吻合的是______。(填字母代号)
Ⅲ.装置③中的现象是______。
(2)根据方案二装置(图2)回答以下问题:
Ⅰ.B装置的作用是______,X是______。
Ⅱ.能说明碳元素和硅元素非金属性强弱的实验现象是______。
(3)实验结论:__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com