
【题目】下列关于原电池的说法正确的是( )
A.在正极上发生氧化反应
B.化学性质较活泼的金属为负极
C.在外电路,电子流出正极
D.是由电能转化为化学能的装置
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】常见物质A~K之间存在如下图所示的转化关系,其中D、E为单质,请回答下列问题(图中有些反应的产物和反应的条件没有全部标出)。
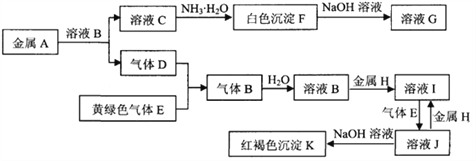
(1)写出下列物质中溶质的名称:B是 __________,G是____________
(2)反应“F→G”的化学方程式是_____________________________________________
(3)反应“J→I”的离子方程式是_____________________________________________
(4)溶液I中混有溶液J,除去J的方法是:________________________________________________________________
(5)检验溶液I中阳离子的方法是:__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的离子积常数KW与温度t(℃)的关系如图所示: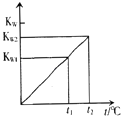
(1)若t1=25℃,则KW1=;若t2=100℃时,KW2=10﹣12 , 则0.05molL﹣1的Ba(OH)2溶液的pH= .
(2)已知25℃时,0.1L0.1molL﹣1的NaA溶液的pH=10,则NaA溶液中所存在的化学平衡有(用离子方程式表示): . 溶液中各离子的物质的量浓度由大到小的顺序为 .
(3)25℃时,将pH=11的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=9,则NaOH溶液与硫酸溶液的体积比为 .
(4)100℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH(pH酸)与强碱的pH(pH碱)之间应满足的关系为:pH(酸)+pH(碱)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分离或提纯,可选用蒸馏法的是
A. 除去石灰水中悬浮的碳酸钙颗粒
B. 除去氯化钠晶体中混有的碘单质
C. 分离汽油和煤油的混合物
D. 分离水和苯的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验,验证元素周期律.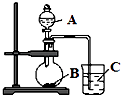
(1)甲同学在a、b、c、d四只烧杯里分别加入50mL冷水,再分别滴加几滴酚酞溶液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象.①甲同学设计实验的目的是验证:同一主族,从上到下元素的元素金属性逐渐增强;同一周期,从左到右,元素金属性;
②反应最剧烈的烧杯里金属是(填字母)
A、钠 B、镁 C、铝 D、钾;
③写出a烧杯里发生反应的离子方程式 .
④实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验的目的,请你帮助选择下列合适的方法 .
A.把镁、铝的金属块换成金属粉末
B.把烧杯中的冷水换成热水
C.把烧杯中的冷水换成盐酸
D.把烧杯中的冷水换成氢氧化钠溶液
(2)乙同学设计实验验证:非金属元素的非金属性越强,其最高价含氧酸的酸性就越强.他设计了如图装置以验证碳、氮、硅元素的非金属性强弱.乙同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,其浓溶液在常温下可与铜反应;B是块状固体;烧杯中盛放C的水溶液,打开分液漏斗的活塞后,C中可观察到白色胶状沉淀生成.①写出所选用物质的化学式:A、; C、 .
②写出烧瓶中发生反应的化学方程式: .
③碳、氮、硅三种元素的非金属性由强到弱顺序为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据相应的图象(图象编号与答案一一对应),判断下列相关说法正确的是( ) 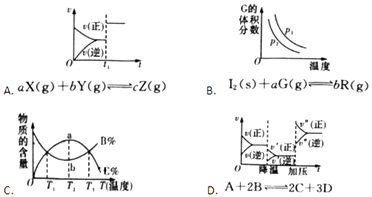
A.t1时改变某一条件有如图所示变化,则改变的条件一定是加入催化剂
B.反应达到平衡时,外界条件对平衡影响关系如图所示,若b=1,a为正整数,则P1<P2
C.从加入反应物开始,物质的百分含量与温度关系如图所示,则该反应的正反应为吸热反应
D.反应速率和反应条件变化如图所示,则该反应正反应为放热反应,A,B一定是气体,D一定不是气体,C可能不是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一水合硫酸四氨合铜(Ⅱ)[Cu(NH3)4]SO4)H2O为深蓝色晶体,在工业上用途广泛,常用作杀虫剂、媒染剂.某学习小组探究制备该晶体并测定其组成的实验过程如下:(Ⅰ)晶体的制备原理及流程:
CuSO4+4NH3+H2O═[Cu(NH3)4]SO4)H2O
回答下列问题:
(1)无水乙醇的作用;烘干晶体的温度性质60℃的原因是;
(2)实验制得产物晶体中往往有Cu2(OH)2SO4杂质,分析产生该杂质的原因可能是;
(3)(Ⅱ)晶体中溶解于酸性溶液中,加入NaI溶液,Cu2+可与I作用产生I2和白色沉淀,该反应的离子方程式为 , 再用Na2S2O3溶液滴定I2 , 即可得Cu2+含量;
(4)(Ⅲ)晶体中氮含量的测定实验装置如图所示,称取0.9380g[Cu(NH3)x]SO4H2O晶体[M=(178+17x)g/mol]于锥形瓶a中,通过分液漏斗向锥形瓶a中滴加10%NaOH溶液,用1.000mol/L的NaOH标准滴定b中剩余的HCl.
滴定管读数如图所示,消耗标准液mL;[Cu(NH3)x]SO4H2O中x= , 推测测量值(x)比理论值偏小的原因是;
(5)(Ⅳ)SO42﹣含量的测定﹣﹣沉淀法称取一定质量的试样,加稀盐酸溶解,将BaCl2加入溶液中,静置得到BaSO4沉淀,检验沉淀已完全的操作为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com