
【题目】下列物质属于共价化合物的是
A. CaOB. NaOHC. K2OD. CO2
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】雾霾已经成为部分城市发展的障碍。雾霾形成的最主要原因是人为排放,其中汽车尾气污染对雾霾的“贡献”逐年增加。回答下列问题:
(1)汽车尾气中含有NO,N2与O2生成NO的过程如下:

①1 mol O2与1 mol N2的总能量比2 mol NO的总能量________(填“高”或“低”)。
②![]() N2(g)+
N2(g)+![]() O2(g)===NO(g)的ΔH=________。
O2(g)===NO(g)的ΔH=________。
③NO与CO反应的热化学方程式可以表示为2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH=a kJ·mol-1,但该反应速率很慢,若使用机动车尾气催化转化器,可以使尾气中的NO与CO转化成无害物质排出。上述反应在使用“催化转化器”后,a值________(选填“增大”“减小”或“不变”)。
2CO2(g)+N2(g) ΔH=a kJ·mol-1,但该反应速率很慢,若使用机动车尾气催化转化器,可以使尾气中的NO与CO转化成无害物质排出。上述反应在使用“催化转化器”后,a值________(选填“增大”“减小”或“不变”)。
(2)氢能源是绿色燃料,可以减少汽车尾气的排放,利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH1。下图是该反应的能量变化图:

①通过图中信息可判断反应CH3OH(g)+H2O(g)===CO2(g)+3H2(g)的ΔH1________(选填“>”“=”或“<”)0。
②图中途径(Ⅱ)的条件是_______________,途径(Ⅰ)的反应热________(选填“>”“=”或“<”)途径(Ⅱ)的反应热。
③已知下列两个热化学方程式:
H2(g)+![]() O2(g)===H2O(g) ΔH2
O2(g)===H2O(g) ΔH2
2CH3OH(g)+3O2(g)===2CO2(g)+4H2O(g) ΔH3
ΔH1、ΔH2、ΔH3三者的关系式为:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应4CO+2NO2![]() N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A. υ(CO)=1.5 mol·L-1·min-1 B. υ(NO2)=0.7 mol·L-1·min-1
C. υ(N2)=0.4 mol·L-1·min-1 D. υ(CO2)=1.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验及现象能推出相应结论的是
选项 | 实验操作 | 现象 | 结论 |
A | 向苯酚钠溶液中加入NaHSO3溶液 | 溶液变浑浊 | 酸性:H2SO3>苯酚 |
B | 向KI淀粉溶液中滴入无色溶液X | 溶液变蓝色 | X一定为H2O2溶液 |
C | 将3体积SO2与1体积O2混合并通过灼热的催化剂充分反应,产物依次通过BaCl2溶液和品红溶液 | 前者产生白色沉淀,后者溶液褪色 | SO2与O2的反应为可逆反应 |
D | 向2支均盛有2mL1.0mol·L-1的KOH溶液的试管中,分别加入2滴浓度均为0.1mol·L-1的AlCl3和FeCl3溶液 | 一支试管出现红褐色沉淀,另一支无明显现象 | Ksp[Al(OH)3]> Ksp[Fe(OH)3] |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个容积相同的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下发生反应CH4(g)+ H2O(g) ![]() CO(g) + 3H2(g)(不发生其他反应),CH4的平衡转化率与温度、压强的关系如图所示。
CO(g) + 3H2(g)(不发生其他反应),CH4的平衡转化率与温度、压强的关系如图所示。
容器 | 起始物质的量/mol | CH4的平衡 转化率 | |||
CH4 | H2O | CO | H2 | ||
Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
Ⅱ | 0.1 | 0.1 | 0.1 | 0.3 | / |
Ⅲ | 0 | 0.1 | 0.2 | 0.6 | / |
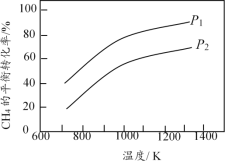
下列说法错误的是
A. 该反应的![]() H>0,图中压强P1>P2
H>0,图中压强P1>P2
B. 起始时,容器Ⅱ中v(CH4)正<v(CH4)逆
C. 达到平衡时,容器Ⅰ、Ⅱ中CO的物质的量满足:n(CO)Ⅱ< 2n(CO)Ⅰ
D. 达到平衡时,容器Ⅱ、Ⅲ中气体的总压强之比PⅡ∶PⅢ = 4∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气压强对许多物理实验和化学实验有着重要影响,制取氨气并完成喷泉实验。
图1 图2
图2
(1)检验圆底烧瓶中氨气收集满的方法是_________________________________。
(2)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是________,该实验的原理是________________________________________。
(3)如果只提供如图2的装置,请说明引发喷泉的方法:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 因为晶体硅有熔点高硬度大的性质,所以被用来做芯片
B. 工业上用焦炭在电炉中还原二氧化硅得到含有少量杂质的硅
C. 合金熔点、硬度都低于成分金属,钢是用量最大用途最广的合金
D. 工业生产玻璃、水泥都需要用到的原材料是石英砂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Cl2O常温下为气态,溶于水可得只含单一溶质A的弱酸性溶液,且有漂白性,A溶液在放置过程中其酸性会增强。常温下,Cl2O与NH3反应生成离子化合物B、气体单质C和常见液体D,C为空气中含量最多的物质。请回答下列问题:
(1)B的化学式为_______,气体单质C的结构式为_________。
(2)用化学方程式表示A溶液酸性增强的原因______。
(3)A溶液能使紫色石蕊溶液褪色,体现了A具有____性。
(4)固体B与碱共热能生成一种刺激性气味的气体,该气体是_____(填“离子” 或“共价”)化合物。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com