
����Ŀ���������ݻ���ͬ�ĺ����ܱ������У���ʼʱ��������Ӧ�����������ʣ�����ͬ�¶��·�����ӦCH4(g)+ H2O(g) ![]() CO(g) + 3H2(g)(������������Ӧ)��CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
CO(g) + 3H2(g)(������������Ӧ)��CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
���� | ��ʼ���ʵ���/mol | CH4��ƽ�� ת���� | |||
CH4 | H2O | CO | H2 | ||
�� | 0.1 | 0.1 | 0 | 0 | 50% |
�� | 0.1 | 0.1 | 0.1 | 0.3 | / |
�� | 0 | 0.1 | 0.2 | 0.6 | / |
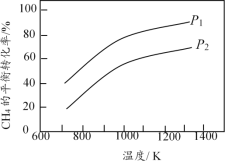
����˵����������
A. �÷�Ӧ��![]() H��0��ͼ��ѹǿP1>P2
H��0��ͼ��ѹǿP1>P2
B. ��ʼʱ����������v(CH4)����v(CH4)��
C. �ﵽƽ��ʱ����������CO�����ʵ������㣺n(CO)��< 2n(CO)��
D. �ﵽƽ��ʱ���������������������ѹǿ֮��P����P�� = 4��5
���𰸡�AD
��������
A������ͼ�������¶ȵ����ߣ�CH4��ת������������������ԭ��������Ӧ����Ϊ���ȷ�Ӧ������H>0������ͬ�¶��£�����ѹǿ���÷�Ӧƽ�����淴Ӧ������У�CH4��ת���ʽ��ͣ����P1<P2����A����
B�� CH4(g)+ H2O(g) ![]() CO(g) + 3H2(g)
CO(g) + 3H2(g)
��ʼ�� 0.1 0.1 0 0
�仯�� 0.05 0.05 0.05 0.15
ƽ�⣺ 0.05 0.05 0.05 0.15 �������������Ϊ1L�����ݻ�ѧƽ�ⳣ���Ķ��壬�÷�Ӧ�Ļ�ѧƽ�ⳣ��K=0.0675������II�е�Ũ����Ϊ0.33��0.1/(0.1��0.1)=0.27>0.0675��˵����Ӧ���淴Ӧ������У���v(CH4)����v(CH4)������B��ȷ��
C����II������ȫ��ת���ɷ�Ӧ�CH4��H2O�����ʵ�������0.2mol��II���Կ�����I�����ϣ���ͨ��0.1molCH4��0.1molH2O����ͨ��0.1molCH4��0.1molH2O���൱������ѹǿ������ƽ�ⲻ�ƶ�����ʱn��(CO)=2n(CO)I��������ѹǿ��ƽ�����淴Ӧ�����ƶ������n(CO)>n��(CO)����n(CO)��< 2n(CO)������C��ȷ��
D����II����ֵ��ȫ��ת����CO��H2O����III����ֵ��Ƚϣ�III��II��0.1molH2O������ѡ��B������II��III��Ӧ�����淴Ӧ������У���II������CO�����ʵ���Ϊxmol��III������CO�����ʵ���Ϊymol���ﵽƽ�����(0.6��2x)/(0.7��2y)=4/5��10x��8y=0.2����x=y=0.1ʱ��II���������������ʵ���Ϊ0.4mol��III���������������ʵ���Ϊ0.5mol��Ҳ����CO��H2Oȫ��ת����CH4��H2Oʱ���Ż����ѹǿ֮�ȵ���4��5�����÷�ӦΪ���淴Ӧ��������ȫ��ת������D����


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ�����͵Ĺ⻯ѧ��Դ�����������缫ʱ��ͨ��O2��H2S�������ȶ��ĵ�����H2AQ��AQ�������л��������˵������ȷ����
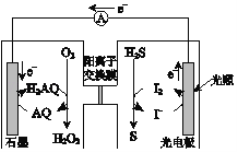
A. �����ĵ缫��ӦΪ2I����2e���TI2
B. �ܷ�ӦΪ H2S+O2 ![]() H2O2+S
H2O2+S
C. H+ͨ�������ӽ���Ĥ�����������븺����
D. ��Դ����ʱ�����˹��ܡ���ѧ�ܡ����ܼ��ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶ȵĶ����ܱ������У���ӦA2��g��+B2��g��![]() 2AB��g���ﵽƽ��״̬���ǣ�
2AB��g���ﵽƽ��״̬���ǣ�
A. ���������ܶȲ��ٸı�
B. �����ڵ���ѹǿ����ʱ����仯
C. ��λʱ��������2n mol AB��ͬʱ������n mol��B2
D. A2��B2��AB�ķ�����֮��Ϊ1:1:2ʱ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����������
A. ��ӦCaC2(s) + N2(g) = CaCN2(s) + C(s) ��![]() H��0
H��0
B. ����ʯ�����꾮ƽ̨������ӵ����������������Է���
C. H2O2���ֽ�ÿ����1molO2��ת�Ƶ��ӵ���ĿΪ2��6.02��1023
D. 25��ʱ����ˮϡ��0.1mol��L��1NH4Cl����Һ��![]() ��������
��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Mg / LiFePO4��صĵ�ط�ӦΪxMg2++2LiFePO4![]() xMg+2Li1��xFePO4+2xLi+����װ��ʾ��ͼ���£�
xMg+2Li1��xFePO4+2xLi+����װ��ʾ��ͼ���£�

����˵����ȷ����
A. �ŵ�ʱ��Li+����ԭ
B. ���ʱ������ת��Ϊ��ѧ��
C. �ŵ�ʱ����·��ÿ����2mol���ӣ���1molMg2+Ǩ����������
D. ���ʱ�������Ϸ����ĵ缫��ӦΪLiFePO4��xe��= Li1��xFePO4 + xLi+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������H(��������)������CT��顢��������Ӱ�ȣ���һ�ֺϳ�·�����£�

(1)H�еĺ�������������Ϊ_____��
(2)F��G�ķ�Ӧ����Ϊ_____��
(3)E�ķ���ʽΪC9H8N2O5��E��F������ԭ��Ӧ��д��E�Ľṹ��ʽ��_____��
(4)C��һ��ͬ���칹��ͬʱ��������������д����ͬ���칹��Ľṹ��ʽ��_____��
����������������ˮ������X��Y��Z�����л��
��X��һ�ְ����ᣬY�ܷ���������Ӧ��Z����FeCl3��Һ������ɫ��Ӧ�ҷ�����ֻ��2�ֲ�ͬ��ѧ�������⡣
(5)��Ӱ�����( )��һ��ҽѧ��ϼ���д����
)��һ��ҽѧ��ϼ���д����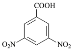 ��CH3CH2CH2Cl��(CH3CO)2OΪԭ���Ʊ���Ӱ������ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������) _________________��
��CH3CH2CH2Cl��(CH3CO)2OΪԭ���Ʊ���Ӱ������ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������) _________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ��10 L�ܱ�������ֻͶ��Ӧ���ij���淴Ӧ����ƽ�ⳣ������ʽΪK=c(CO)c(H2)/c(H2O)����ش��������⣺
(1)�÷�Ӧ�Ļ�ѧ����ʽΪ______________________________�����¶����ߣ� K������÷�Ӧ��___________ (��������������������)��Ӧ��
(2)���жϸ÷�Ӧһ���ﵽƽ��״̬����___________(����ĸ���)��
A.v��(H2O)=v��(H2)
B.�����������ƽ����Է�����������ʱ��ı�
C.����nmol H2��ͬʱ����nmol CO
D.���������ʵ������ʵ�������ʱ��ı�
(3)�÷�Ӧ��v(��)��ʱ��仯�Ĺ�ϵ��ͼ����t2minʱ�ı���ij���������ı������������______��________����д2����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�����̼����MCO3(M��Mg2����Ca2����Mn2��)�ij����ܽ�ƽ��������ͼ��ʾ������˵���������
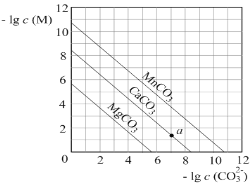
A. Ksp(MnCO3)��������Ϊ10��11
B. MgCO3������Һ�м�������ˮ�����c(Mg2��)����
C. a���ʾ����Һ�У�c(Ca2��)��c(CO32��)
D. ��Ũ�Ⱦ�Ϊ0.01mol��L��1��Mg2����Ca2����Mn2�������Һ����μ���Na2CO3��Һ�������γ�MgCO3����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com