
【题目】一定温度下,在一个10 L密闭容器中只投反应物发生某可逆反应,其平衡常数表达式为K=c(CO)c(H2)/c(H2O),请回答下列问题:
(1)该反应的化学方程式为______________________________;若温度升高, K增大,则该反应是___________ (填“吸热”或“放热”)反应。
(2)能判断该反应一定达到平衡状态的是___________(填字母序号)。
A.v正(H2O)=v逆(H2)
B.容器中气体的平均相对分子质量不随时间改变
C.消耗nmol H2的同时消耗nmol CO
D.容器中物质的总物质的量不随时间改变
(3)该反应的v(正)随时间变化的关系如图,在t2min时改变了某种条件,改变的条件可能是______、________。(写2条)

【答案】C+H2O![]() CO+H2 吸热 A B 增大反应物浓度 升高温度
CO+H2 吸热 A B 增大反应物浓度 升高温度
【解析】
(1)依据平衡常数表达式书写方法和元素守恒写出化学方程式,用生成物平衡浓度的幂次方乘积除以反应物平衡浓度幂次方乘积,平衡移动原理分析可知,温度升高,平衡常数中等,说明平衡正向进行为吸热反应;
(2)化学平衡的根本原因是正、逆反应速率相等,反应混合物中各组分的百分含量保持不变,然后根据具体的化学方程式,逐一判断;
(3)根据图象可知,t2时正反应速率立即增大,达到平衡时正反应速率大于原平衡状态时的反应速率
(1)①根据平衡常数的定义,生成物浓度的幂之积与反应物浓度的幂之积之比为平衡常数,反应的方程式为C(s)+H2O(g)CO(g)+H2(g),故答案为:C(s)+H2O(g)CO(g)+H2(g);
(2)A、v正(H2O)=v逆(H2)时,氢气正逆反应速率相同,反应达到平衡,故A正确;
B、反应前后气体的物质的量不相同,气体质量变化,容器中气体的平均相对分子质量不随时间变化即达到平衡,故B正确;
C、消耗nmolH2的同时消耗nmolCO,反应都代表逆反应,不能说明反应达到平衡状态,故C错误;
D、碳为固体,反应前后气体体积发生变化,容器中气体总物质的量不随时间变化,说明反应达到平衡状态,故D正确;故答案为:ABD;
(3)由图象可以知道,在t2时正反应速率立即增大,且达到平衡时正反应速率大于原平衡状态时的反应速率,说明达到平衡时反应物的浓度大于原平衡的浓度,根据影响反应速率的因素分析,可以加入生成物H2O(g),正反应速率会立刻增大,达到新的平衡时H2O(g)的浓度比原平衡的浓度大,反应速率增大;反应是吸热反应,也可以升高温度,正逆反应速率都增大,且达到平衡时正逆反应速率都大于原平衡的速率,故答案为:增大反应物浓度;升高温度.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
【题目】实验小组研究酸性条件下K2Cr2O7溶液和H2O2溶液的反应。
(实验Ⅰ)向盛有H2O2溶液的试管中,加入过量的K2Cr2O7溶液和硫酸,振荡,溶液立即变为紫红色,此时pH=1.溶液中持续产生气泡,最终溶液变为绿色。
资料:
ⅰ.Cr2(SO4)3溶液呈绿色。
ⅱ.酸性条件下,K2Cr2O7溶液和H2O2溶液反应生成CrO5,CrO5进一步反应生成Cr3+和O2。
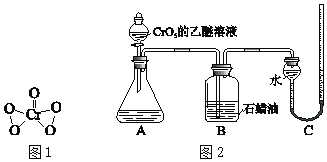
ⅲ.CrO5是一种+6价Cr的过氧化物,其结构如图1,CrO5可溶于水,易溶于乙醚得到蓝色溶液。
ⅳ.乙醚是一种无色、不溶于水、密度比水小的有机溶剂,化学性质稳定。
(1)实验Ⅰ中产生的气体是O2,检验的方法是___________。
(2)实验Ⅰ的紫红色溶液中含有CrO5。
①验证紫红色溶液中含有CrO5的操作及现象是_________________。
②生成CrO5的反应不是氧化还原反应,反应的离子方程式是_______________。
(3)对实验Ⅰ中溶液变为绿色和产生O2的原因,作出如下假设:
a.CrO5在酸性溶液中不稳定,自身氧化还原生成Cr3+和O2。
b.CrO5在酸性条件下氧化了溶液中的H2O2,生成Cr3+和O2。
为验证上述假设,用图2装置进行实验Ⅱ和实验Ⅲ(夹持装置已略,B中石蜡油用于吸收挥发出的乙醚)。实验操作及现象如下:
(实验Ⅱ)
ⅰ.将20mL CrO5的乙醚溶液加入A中的20mLpH=1的稀硫酸中,不断搅拌,乙醚层由蓝色变为无色,水层变为绿色,O2体积为V mL。
ⅱ.步骤ⅰ结束后向A中加入少量K2Cr2O7溶液,轻轻搅拌,静置,乙醚层又显出蓝色。
(实验Ⅲ)
仅将实验Ⅱ中的pH=1的稀硫酸替换为等量的含H2O2的pH=1的稀硫酸,重复实验。现象与实验Ⅱ相同,且O2体积仍为V mL。
①实验Ⅱ步骤ⅰ中消耗的CrO5与生成的O2的物质的量之比为2:3,补全离子方程式:2CrO5+____=2Cr3++3O2↑+_____+_____。
②甲同学认为依据实验Ⅱ和Ⅲ中生成O2的体积相同,无法说明假设b是否成立,其理由是_________。
(4)实验Ⅰ中总反应的离子方程式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
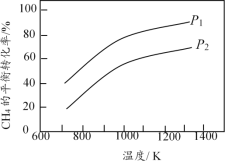
【题目】在三个容积相同的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下发生反应CH4(g)+ H2O(g) ![]() CO(g) + 3H2(g)(不发生其他反应),CH4的平衡转化率与温度、压强的关系如图所示。
CO(g) + 3H2(g)(不发生其他反应),CH4的平衡转化率与温度、压强的关系如图所示。
容器 | 起始物质的量/mol | CH4的平衡 转化率 | |||
CH4 | H2O | CO | H2 | ||
Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
Ⅱ | 0.1 | 0.1 | 0.1 | 0.3 | / |
Ⅲ | 0 | 0.1 | 0.2 | 0.6 | / |
下列说法错误的是
A. 该反应的![]() H>0,图中压强P1>P2
H>0,图中压强P1>P2
B. 起始时,容器Ⅱ中v(CH4)正<v(CH4)逆
C. 达到平衡时,容器Ⅰ、Ⅱ中CO的物质的量满足:n(CO)Ⅱ< 2n(CO)Ⅰ
D. 达到平衡时,容器Ⅱ、Ⅲ中气体的总压强之比PⅡ∶PⅢ = 4∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 因为晶体硅有熔点高硬度大的性质,所以被用来做芯片
B. 工业上用焦炭在电炉中还原二氧化硅得到含有少量杂质的硅
C. 合金熔点、硬度都低于成分金属,钢是用量最大用途最广的合金
D. 工业生产玻璃、水泥都需要用到的原材料是石英砂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:

(1)从反应开始到10 s,用Z表示的反应速率为____________Y的转化率为_____________。
(2)该反应的化学方程式为____________________________。
(3)10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示:则下列说法符合该图像的是___________。

A.t1时刻,增大了X的浓度
B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积
D.t1时刻,使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 合成氨工业上增大压强以提高反应物的转化率
B. 黄绿色的氯水光照后颜色变浅
C. 由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
D. 在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于浓度均为0.1mol·L-1的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
A. c(NH![]() ):③>①;水电离出的c(H+):①>②
):③>①;水电离出的c(H+):①>②
B. 将pH值相同②和③溶液加水稀释相同的倍数PH变化大的是③
C. ①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O)
D. ①和③等体积混合后的溶液:c(NH![]() )>c(Cl-)> c(NH3·H2O) >c(OH-)>c(H+)
)>c(Cl-)> c(NH3·H2O) >c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com