
【题目】在密闭容器中,一定条件下进行如下反应:NO (g) +CO(g)![]()
![]() N2(g) +CO2 (g) △H=-373.2 kJ/mol达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g) +CO2 (g) △H=-373.2 kJ/mol达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
科目:高中化学 来源: 题型:
【题目】在标准状况下充满HCl的烧瓶做完喷泉实验后得到稀盐酸,用标准碳酸钠溶液滴定这种盐酸测定它的准确浓度,请你回答下列问题:
(1)用标准Na2CO3溶液滴定这种盐酸时,Na2CO3溶液应装在_______式滴定管内,原因是(文字叙述并用有关离子方程式表示): ;若用甲基橙作指示剂,达到滴定终点时,溶液从_______色变为_______色。
(2)现配制三种浓度的标准Na2CO3溶液,你认为最合适的是下列第______种(填序号)。
①2.500 mol/L ②0.25 mol/L ③0.025mol/L
(3)若采用上述合适浓度的标准Na2CO3溶液滴定,用C(Na2CO3)表示,滴定时实验数据列表如下:
实验编号 | 待测盐酸体积(mL) | 滴入Na2CO3溶液体积(mL) |
1 | 20.00 | 18.80 |
2 | 20.00 | 16.95 |
3 | 20.00 | 17.05 |
根据以上数据计算时应带入的Na2CO3溶液体积为_________,求这种待测盐酸的物质的量浓度(用数据和符号列式即可):C(HCl)=_________ 。
(4)若盛装Na2CO3溶液的滴定管在滴定前未用标准液润洗,则最后所测盐酸浓度______(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 酯类物质是形成水果香味的主要成分
B. 可用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
C. 乙酸乙酯、油脂与烧碱溶液反应均有醇生成
D. 可向蔗糖的水解液中直接加入银氨溶液检验蔗糖是否发生水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.01molNH4Cl和0.005molNaOH溶于水配成1L溶液(pH>7).
(1)该溶液中存在的三个平衡体系是 、 、 。
(2)溶液中存在的离子物质的量浓度由大到小顺序为 。
(3)这些粒子中浓度为0.01mol/L的是 ,浓度为0.005mol/L的是 。
(4)物质的量之和为0.0lmol的二种粒子是 。
(5)NH4+和H+两种粒子物质的量之和比OH-多 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与氯气反应 :2NaClO2 + Cl2 ===2ClO2 + 2NaCl。
下图是实验室用于制备和收集一定量较纯净的ClO2的装置(某些夹持装置和垫持用品省略)。其中E中盛有CCl4液体(用于除去ClO2中的未反应的Cl2)。
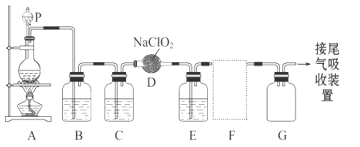
(1)仪器P的名称是______________________。
(2)写出装置A中烧瓶内发生反应的离子方程式:_____________________。
(3)B装置中所盛试剂是____________________。
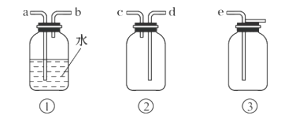
(4)F为ClO2收集装置,应选用的装置是______________(填序号),其中与E装置导管相连的导管口是__________(填接口字母)。
(5)若用100 mL 2 mol·L-1的浓盐酸与足量的MnO2制备Cl2,则被氧化的HCl的物质的量是________(填序号)。
A.>0.1 mol B.0.1 mol C.<0.1 mol D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关问题,与盐的水解无关的是( )
A.NH4Cl 与 ZnCl2 溶液可作焊接金属中的除锈剂
B.用 NaHSO4 去除暖手瓶中的水垢
C.实验室盛放 Na2CO3 溶液的试剂瓶不能用磨口玻璃塞
D.加热蒸干 AlCl3 溶液得到 Al(OH)3 固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如下图所示。

(1)由图中所给数据进行分析,该反应的化学方程式为_______________。
(2)反应从开始至2min末,用Z(为气态)的浓度变化表示的平均反应速率为_______ mol/(L·min)。
(3)当反应进行到第_____min时,该反应达到平衡。反应达到平衡后,下列措施一定能加快化学反应速率的有____
A.增大Z的量 B.升高温度
C.使用正催化剂 D.增大X或Y的量
(4)分别用X和Y的反应速率来表示已达到化学平衡状态的表达式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质按酸、碱、混合物、电解质的顺序组合的一组是
A. 氢氟酸、纯碱、空气、液氨
B. 硝酸、烧碱、水玻璃、硫酸钡
C. 醋酸、熟石灰,胆矾、小苏打
D. 硫酸、碱式碳酸铜、汽油、草木灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在溶液中可以大量共存的是
A. H+、AlO2-、Cl-、S2- B. Na+、K+、NH4+、CO32-
C. Br-、Al3+、Cl-、HCO3- D. Ba2+、OH-、SO42-、HCO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com