
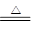 3Cu+N2+3H2O(2分)(4)氧化(1分) +4(2分)
3Cu+N2+3H2O(2分)(4)氧化(1分) +4(2分)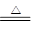 3Cu+N2+3H2O。
3Cu+N2+3H2O。

科目:高中化学 来源:不详 题型:单选题
| A.胶体:组成物质的直径是否在1nm~100nm之间 |
| B.氧化还原反应:反应前后元素的化合价是否发生了变化 |
| C.共价化合物:组成化合物的元素是否全部都是非金属元素 |
| D.化学变化:是否有热效应、颜色变化、气体或沉淀生成等四种实验现象 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只表现氧化性 | B.只表现还原性 |
| C.既表现氧化性又表现酸性的是 | D.既表现氧化性又表现还原性的是 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe3+、NO3–、I–、K+ | B.H+、NO3–、Fe2+、Na+ |
| C.K+、Al3+、H+、MnO4– | D.Cu2+、NH4+、Br–、OH– |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质 |
| B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质 |
| C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌 |
| D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com