
【题目】现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C 的最外层电子数相等,A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子。请回答下列问题.(题中的字母只代表元素代号,与实际元素符号无关):
(1)B的元素符号为_________,E在元素周期表中的位置为__________;
(2)A、C、D三种元素组成的一种常见化合物,是氯碱工业的重要的产品,请写出该反应的化学方程式___________。
(3)A2C和A2E两种物质沸点较高的是_______(填写化学式)。
(4)B与F两种元素形成的一种化合物分子,各原子均达8 电子结构,则该化合物化学式为____。B和F两种元素还能形成另一种化合物,其中B显最高正价,该化合物能与水反应生成两种酸,请写出该化合物与水反应的化学方程式:____________。
【答案】 N 3,VIA 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ H2O NCl3 NCl5+3H2O=HNO3+5HCl
2NaOH+H2↑+Cl2↑ H2O NCl3 NCl5+3H2O=HNO3+5HCl
【解析】A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与C形成的化合物常温下为液态,化合物为水,则A为H元素,C为O元素;A、B的最外层电子数之和与C的最外层电子数相等,B的最外层电子数为5,则B为N元素;A、D同主族,则D为Na元素;C与E同主族,则E为S元素;D、E、F同周期,A能分别与E、F形成电子总数相等的气体分子,则F为Cl元素,所以A、B、C、D、E、F分别是:H、N、O、Na、S、Cl,根据元素化合物的性质解决题干中的问题。
(1)根据分析,B元素是氮元素,其元素符号是N,E元素是硫元素,在周期表中位于第三周期,ⅥA族;正确答案:N;第三周期,ⅥA族;
(2)A、C、D三种元素组成的一种常见化合物是NaOH,氯碱工业是电解饱和食盐水,其反应的化学方程式:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,正确答案:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,正确答案:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
(3)A2C是H2O,A2E是H2S,它们都是分子晶体,但H2O间能够形成氢键,其沸点高于H2S,所以H2O的沸点较高,正确答案:H2O;
(4)对照氮和氯形成的化合物可以推出氮、氯形成的各原子均达八电子结构的化合物是NCl3,若氮呈最高正价,即为+5价,氯呈-1价,形成的化合物为NCl5,所以NCl5水解的产物为HCl和HNO3,反应的化学方程式是:NCl5+3H2O=HNO3+5HCl,正确答案:NCl3;NCl5+3H2O=HNO3+5HCl。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将1.60gCuSO4固体置于下图所示的装置(固定及夹持类仪器未画出)中加热到1100℃,使其分解,分解过程中可以观察到:石英管中固体由白色变为黑色,最终变为红色;BaCl2溶液中生成白色沉淀,品红溶液褪色,集气瓶中收集到无色气体。
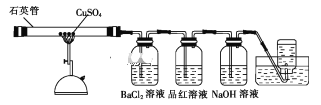
(1)石英主要成分的化学式是_____;高温分解CuSO4固体使用石英管而不使用普通玻璃管的原因是_____。
(2)石英管中剩余红色固体质量为0.72 g,经检测为不含硫元素的纯净物。则该固体的化学式为__。
(3)将BaCl2溶液中生成的白色沉淀过滤并洗涤,向洗涤后的沉淀中加入稀盐酸,无明显现象。
①沉淀的化学式为_____。
②检验沉淀是否洗净的方法是___。
(4)若NaOH溶液足量,则其中发生反应的离子方程式为____。
(5)集气瓶中收集的无色气体是____(填化学式),检验该气体的方法是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+,Mg2+,SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液
A.②⑤④①③B.④①②⑤③
C.④②⑤①③D.①④②⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的合成路线如下,完成下列内容
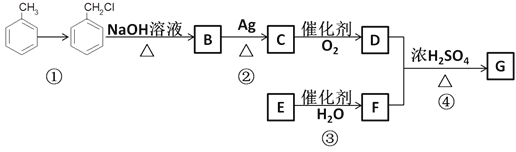
已知:①R—Cl![]() R—OH;②RCHO
R—OH;②RCHO![]() RCOOH;
RCOOH;
③E的产量可衡量一个国家石油化工的发展水平
(1)反应①反应条件为____________。
(2)B中所含官能团名称为___________。
(3)反应②的化学方程式为________________________________________________________。
简述验证是有C生成的操作及现象___________________________。
(4)反应③的反应类型为__________。
(5)反应④的化学方程式为___________________________________________________。
(6)G有很多同分异构体,则满足下列条件的同分异构体有________种。
①含有一个羧基 ②含有一个苯环 ③苯环上有三个取代基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是生产生活中的常见有机物的分子式、结构式、结构简式或名称有关说法正确的是
①![]() ②
②![]() ③
③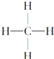 ④
④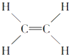 ⑤CH3CH2OH
⑤CH3CH2OH
⑥C6H12O6⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯
A. 能跟溴的四氯化碳溶液发生加成反应并使之褪色的有①②④⑩
B. 投入钠能产生H2的是⑤⑦⑧⑨
C. 属于高分子材料的是⑧⑨⑩
D. 含碳量最高、有毒、常温下为液体且点燃时有浓烟的是①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为 ,分析其结构,并回答下列问题:
,分析其结构,并回答下列问题:
(1)写出其分子式:____________________________________________。
(2)其中含有____个不饱和碳原子,分子中有____个双键。
(3)分子中的极性键有__________(写出2种即可)。
(4)分子中的饱和碳原子有______个,一定与苯环处于同一平面的碳原子有______个。
(5)分子中C—C===O键角约为__________,H—C≡C键角约为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,与14 g氢气的体积相等的氮气的( )
A. 质量为14 g
B. 物质的量为7 mol
C. 体积为22.4 L
D. 物质的量为14 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E 是五种短周期元素,其中A、B、C 在同一周期。0.5molA 元素的原子失去9.03×1023 个电子后,转化为具有与氖原子相同电子层结构的离子,A 元素最高价氧化物的水化物能分别与B、C 元素最高价氧化物的水化物反应,且都生成盐,B 元素原子各层电子数均为偶数,C 元素原子最外层电子数比最内层少一个。D 元素的一种同位素原子中没有中子。E 元素与其它四种元素均不在同一周期,E 的最高价氧化物的水化物是一种强酸。请回答下列问题:
(1)A 离子结构示意图为:_____;E 元素在周期表中的位置是_____;
(2)用电子式表示B 与C 形成化合物的过程:_____;
(3)A 元素最高价氧化物的水化物与 C 元素最高价氧化物的水化物反应的离子方程式是:_____;
(4)E 与D 形成的某种化合物,其水溶液呈碱性,其原因是_____(用离子方程式作答)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com