
【题目】硫和氮的氧化物直接排放会引发严重的环境问题,请回答下列问题:
(1)下列环境问题主要由硫氧化物和氮氧化物的排放引发的是___________。
A.全球变暖 B.酸雨 C.水体富营养化(水华) D.白色污染
(2)SO2的排放主要来自于煤的燃烧。常用石灰石脱硫,其产物可以做建筑材料。
已知:CaCO3(s)=CO2(g)+CaO(s) ΔH=+178.2kJ/mol
SO2(g)+CaO(s)=CaSO3(s) ΔH=-402kJ/mol
2CaSO3(s)+O2(g)=2CaSO4(s) ΔH=-234.2kJ/mol
写出CaCO3与SO2脱硫的热化学反应方程式_____________________________________。
(3)NOx的排放主要来自于汽车尾气,包含NO2和NO,有人提出用活性炭对NOx进行吸附,发生反应如下:
反应a:C(s)+2NO(g)![]() N2(g)+CO2(g) ΔH=-34.0kJ/mol
N2(g)+CO2(g) ΔH=-34.0kJ/mol
反应b:2C(s)+2NO2(g)![]() N2(g)+2CO2(g) ΔH=-64.2kJ/mol
N2(g)+2CO2(g) ΔH=-64.2kJ/mol
对于反应a,在T1℃时,借助传感器测得反应在不同时间点上各物质的浓度如表:
浓度(molL-1) | 时间(min) | |||||
0 | 10 | 20 | 30 | 40 | 50 | |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10min内,NO的平均反应速率v(NO)=___________,当升高反应温度,该反应的平衡常数K___________(选填“增大”、“减小”或“不变”)。
②30min后,只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是___________(填字母)。
A.加入一定量的活性炭 B.通入一定量的NO
C.适当缩小容器的体积 D.加入合适的催化剂
(4)某实验室模拟反应b,在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 α(NO)随温度的变化如图所示:
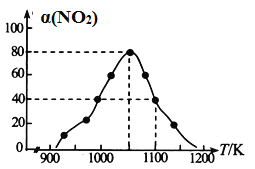
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa 时,该反应的化学平衡常数Kp=________(只列出计算式)(已知:气体分压=气体总压×体积分数)。
【答案】B 2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g) ΔH=-681.8kJ/mol 0.042mol/(Lmin) 减小 BC 1050K前反应未达平衡状态,随着温度升高,反应速率加快,NO2转化率提高 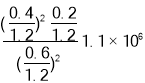 或
或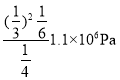
【解析】
(1)硫氧化物和氮氧化物的排放引发酸雨、光化学烟雾等;
(2)已知:①CaCO3(s)═CO2(g)+CaO(s)△H=+178.2kJ/mol,②SO2(g)+CaO(s)═CaSO3(s)△H=-402kJ/mol,③2CaSO3(s)+O2(g )═2CaSO4(s)△H=-234.2kJ/mol,根据盖斯定律计算(①+②)×2+③得到石灰石脱硫的热化学反应方程式;
(3)①0~10min内,NO的平均反应速率v(NO)=![]() ;反应为放热反应升温平衡逆向进行;
;反应为放热反应升温平衡逆向进行;
②30min后,只改变某一条件,反应重新达到平衡,C(s)+2NO(g)![]() N2(g)+CO2(g),依据图表数据分析,平衡状态物质浓度增大,依据平衡常数计算K=
N2(g)+CO2(g),依据图表数据分析,平衡状态物质浓度增大,依据平衡常数计算K=![]() ,平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小溶液体积后加入一定量一氧化氮;
,平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小溶液体积后加入一定量一氧化氮;
(4)①1050kPa前,反应b中NO2转化率随着压强增大而增大的原因,1050KPa前反应未达平衡状态,随着压强增大,反应速率加快;
②在T2℃、在1100 kPa时二氧化氮转化率40%,结合三行计算列式得到;设通入二氧化氮2mol,
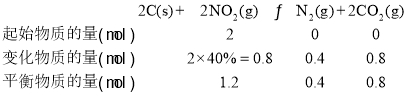
Kp=![]() 。
。
(1)硫氧化物和氮氧化物的排放引发酸雨、光化学烟雾等;
A.全球变暖是二氧化碳,故A错误;
B.硫氧化物和氮氧化物的排放引发硫酸型酸雨和硝酸型酸雨,故B正确;
C.水体富营养化(水华)是磷元素过量排放,故C错误;
D.白色污染是聚乙烯、聚氯乙烯等塑料制品造成,故D错误;
故答案为:B;
(2)已知:①CaCO3(s)═CO2(g)+CaO(s)△H=+178.2kJ/mol,②SO2(g)+CaO(s)═CaSO3(s)△H=-402kJ/mol,③2CaSO3(s)+O2(g )═2CaSO4(s)△H=-234.2kJ/mol,盖斯定律计算(①+②)×2+③得到石灰石脱硫的热化学反应方程式:2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g)△H=-681.8kJ/mol;
(3)①C(s)+2NO(g)N2(g)+CO2(g)△H=-34.0kJ/mol,图表数据得到0~10min内,NO的平均反应速率v(NO)=![]() =
=![]() =0.042mol/(Lmin),反应为放热反应升温平衡逆向进行,平衡常数减小;
=0.042mol/(Lmin),反应为放热反应升温平衡逆向进行,平衡常数减小;
②30min后,只改变某一条件,反应重新达到平衡,C(s)+2NO(g)![]() N2(g)+CO2(g),依据图表数据分析,平衡状态物质浓度增大,依据平衡常数计算K=
N2(g)+CO2(g),依据图表数据分析,平衡状态物质浓度增大,依据平衡常数计算K=![]() ,平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小溶液体积后加入一定量一氧化氮;
,平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小溶液体积后加入一定量一氧化氮;
A.加入一定量的活性炭,碳是固体对平衡无影响,平衡不动,故A错误;
B.通入一定量的NO,新平衡状态下物质平衡浓度增大,故B正确;
C.适当缩小容器的体积,反应前后体积不变,平衡状态物质浓度增大,故C正确;
D.加入合适的催化剂,催化剂只改变化学反应速率,不改变化学平衡,故D错误;
故答案为BC;
(4)①1050 kPa 前,反应b 中NO2转化率随着压强增大而增大的原因,1050kPa前反应未达平衡状态,随着压强增大,反应速率加快,
②在1100 kPa时二氧化氮转化率40%,结合三行计算列式得到;设通入二氧化氮mol;
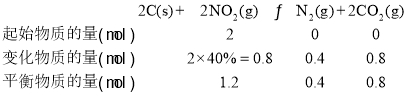
气体总物质的量=1.2mol,Kp=![]() =
=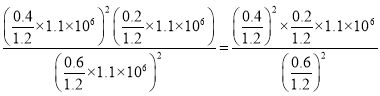 。
。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是![]()
A.明矾和漂白粉常用于自来水净化和杀菌消毒,其作用原理相同
B.![]() 和
和![]() 的漂白原理不同,混合使用效果更好
的漂白原理不同,混合使用效果更好
C.汽车尾气的大量排放不仅会造成酸雨还可能引起光化学烟雾
D.可用浓盐酸酸化的高锰酸钾溶液与过氧化氢反应,证明过氧化氢具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,其主要过程如下图所示。

已知:几种物质中化学键的键能如下表所示。
化学键 | H2O中H—O键 | O2中O=O 键 | H2中H—H键 | H2O2中O—O键 | H2O2中O—H键 |
键能kJ/mol | 463 | 496 | 436 | 138 | 463 |
若反应过程中分解了2 mol水,则下列说法不正确的是
A. 总反应为2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
B. 过程I吸收了926 kJ能量
C. 过程II放出了574 kJ能量
D. 过程Ⅲ属于放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应![]() 为吸热反应,下列对该反应的说法正确的是( )
为吸热反应,下列对该反应的说法正确的是( )
A.X的能量一定低于M的能量,Y的能量一定低于![]() 的能量
的能量
B.因为该反应为吸热反应,故需要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量
D.反应物X和Y的总能量大于生成物M和N的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将Cl2缓慢通入水中至饱和,然后再滴加0.1 mol·L-1的NaOH溶液,整个过程中溶液的pH变化曲线如图所示。下列选项正确的是( )

A. a点所示的溶液中c(H+)=c(Cl-)+c(HClO)+c(OH-)
B. b点所示的溶液中c(H+)>c(Cl-)>c(HClO)>c(ClO-)
C. c点所示的溶液中c(Na+)=c(HClO)+c(ClO-)
D. d点所示的溶液中c(Na+)>c(ClO-)>c(Cl-)>c(HClO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的说法正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式( )看,78g苯中含有碳碳双键数为3NA
)看,78g苯中含有碳碳双键数为3NA
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A原子核内只有1个质子;B原子半径是其所在主族中最小的,B的最高价氧化物对应的水化物的化学式为HBO3;C原子最外层的电子数比次外层的多4;C的简单阴离子与D的阳离子具有相同的电子层结构,两元素可形成化合物D2C;C、E同主族。回答下列问题:
(1)B在元素周期表中的位置为______________________。
(2)B、C、D、E形成的简单离子半径由大到小的关系是________________(用离子符号表示)。
(3)用电子式表示化合物D2C的形成过程______________________。
(4)由A、B、C三种元素形成的常见的离子化合物的化学式为___________,该化合物的水溶液中各离子的浓度由大到小的顺序为______________________。
(5)化合物D2EC3在一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加入等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是
A. 甲、乙中都是铝过量 B. 甲中铝过量,乙中碱过量
C. 甲中酸过量,乙中铝过量 D. 甲中酸过量,乙中碱过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.c(H+)=![]() 的溶液一定呈中性
的溶液一定呈中性
B.将水加热,KW增大,pH不变,仍呈中性
C.向水中加入少量碳酸氢钠固体,溶液的c(H+) 增大,KW不变
D.向0.1mol·L-1醋酸溶液中加水,溶液中水电离产生的c(H+)将减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com