
【题目】pH=1的某溶液X中含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO42-、SO32-、Cl-、NO3-中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如图。下列有关推断不正确的是( )
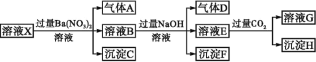
A.溶液X中一定含有NH4+、Al3+、H+、Fe2+、SO42-
B.根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl-
C.沉淀H为Al(OH)3、BaCO3的混合物
D.若溶液X为100 mL,产生的气体A为44.8 mL(标准状况),则X中c(Fe2+)=0.06 mol·L-1
【答案】C
【解析】
pH=1的溶液为强酸性溶液,在强酸性溶液中一定不会存在CO32-、SO32-离子;加入过量硝酸钡生成沉淀,则该沉淀C为BaSO4,说明溶液中含有SO42-离子,生成气体A,则A只能是NO,说明溶液中含有还原性离子,则一定为Fe2+离子,溶液B中加入过量NaOH溶液,沉淀F只为Fe (OH) 3,生成气体D,则D为NH3,说明溶液中含有NH4+离子;溶液E中通入CO2气体,生成沉淀H,则H为Al (OH) 3,E为NaOH和NaAlO2,说明溶液中含有Al3+离子,再根据离子共存知识,溶液中含有Fe2+离子,则一定不含NO3- 离子和SO32-离子,那么一定含有SO42-离子,那么就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,以此进行解答即可。
A、依据分析可知,溶液中一定存在有NH4+、Al3+、Fe2+、SO42-和H+,故A正确;
B、根据上述连续实验不能确定溶液X中是否含有Fe3+和Cl-,故B正确;
C、根据上述分析可知H为Al(OH )3,BaCO3与过量的二氧化碳生成碳酸氢钡,易溶于水,故C错误;
D、生成气体A的离子反应方程式为:3Fe2++NO3- +4H+=3Fe3++NO↑+2H2O,产生的气体A为44.8mL,物质的量为:0.002mol,故n( Fe2+ )= 0.006mol,c(Fe2+)=![]() =0.06mol/L, 故D正确;
=0.06mol/L, 故D正确;
故选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在标准状况下,下列四种气体的关系中,从大到小的是
①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3
A. 体积:④>①>②>③
B. 密度:②>③>④>①
C. 质量:②>①>③>④
D. 氢原子数:①>②>③>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于外围电子层排布为3s23p4的粒子的描述,正确的是( )
A.它的元素符号为O
B.它的核外电子排布式为1s22s22p63s23p4
C.它可与H2生成液态化合物
D.其轨道表示式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组的同学用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,回答下列问题:
(1)用分析天平准确称取该样品5.0g,全部溶于水配制成1000.0mL的溶液。用____(填一仪器名称)量取其中20.00mL放在锥形瓶中,滴加几滴指示剂,待测。该中和滴定中可选用的指示剂是__________________________,(如有几种,可任填一种)滴定终点的现象是___________________________________________________________。
(2)用0.10mol/L的盐酸溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
1 | 20.00 | 24.01 |
2 | 20.00 | 23.99 |
3 | 20.00 | 22.10 |
计算样品中,NaOH的质量百分含量为__________________。
(3)若滴定前,滴定管尖端有气泡,滴定终了气泡消失,将使所测结果______(填“偏高”、“偏低”或“不变”,下同),若读酸式滴定管读数时,滴定前仰视读数,滴定后正确读数,则所测结果_______;
(4)下图为0.10mol/L 25 mL NaOH溶液中逐滴滴加0.10mol/L CH3COOH溶液过程中溶液pH的变化曲线,请回答:
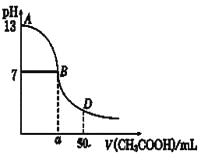
①B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?________区间。(若正确,此问不答)。
②在D点时,溶液中c(CH3COO-)+c(CH3COOH)______2c(Na+)。(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用MnO2和浓盐酸制氯气:MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。
(1)该反应中氧化剂和氧化产物的物质的量之比为_________。
(2)该反应中,若有0.2 mol HCl被氧化,能生成标准状况下Cl2的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为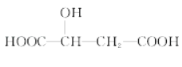 ,下列说法正确的是( )
,下列说法正确的是( )
A.1mol 苹果酸可与 3mol NaOH 发生中和反应
B.苹果酸中能发生酯化反应的官能团有 2 种
C.1mol 苹果酸与足量金属 Na 反应生成生成 1mol H2
D.HOOC—CH2—CH(OH)—COOH 与苹果酸互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如下图所示。

下列说法不正确的是
A. 该催化反应实现了太阳能向化学能的转化
B. 阶段I中,H2O2是氧化产物
C. 每生成1molO2,阶段II中转移电子2 mol
D. 反应的两个阶段均为吸热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断裂1molH2(g)中的H—H键需要吸收436kJ能量,断裂1molI2(g)中的I—I键需要吸收151kJ能量,生成1molHI(g)中的H—I键能放出299kJ能量。下列说法正确的是( )
A.1molH2(g)和1molI2(g)的总能量为587kJ
B.H2(g)+I2(s)![]() 2HI(g) ΔH=-11kJ·mol-1
2HI(g) ΔH=-11kJ·mol-1
C.HI(g)![]()
![]() H2(g)+
H2(g)+![]() I2(g) ΔH=+5.5kJmol-1
I2(g) ΔH=+5.5kJmol-1
D.I2(g)比H2分子稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
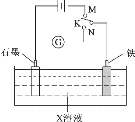
A.K与N连接时,X为硫酸,一段时间后溶液的pH减小
B.K与N连接时,X为氯化钠,石墨电极的电势更高
C.K与M连接时,X为硫酸,一段时间后溶液的pH增大
D.K与M连接时,X为氯化钠,石墨电极反应:4OH--4e-=2H2O+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com