
【题目】下列各原子或离子的电子排布式错误的是( )
A.Na:1s22s22p63s1B.F:1s22s22p5
C.N3:1s22s22p6D.O2:1s22s22p4
科目:高中化学 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂,广泛用于纺织工业。
(1)在一定温度下,将足量SO2气体通入甲酸(HCOOH)和NaOH混合溶液中,即有保险粉生成同时生成一种气体。该反应的化学方程式为_________________________。
(2)保险粉可用于除去废水中的重铬酸根离子(Cr2O72﹣被转化为Cr3+),这是目前除去酸性废水中铬离子的有效方法之一,则每消耗0.2mol保险粉,理论上可除去Cr2O72﹣的物质的量为__________mol
(3)Na2S2O4溶液在空气中易被氧化,某课题小组测定0.050mol·L﹣1Na2S2O4溶液在空气pH变化如下图1;
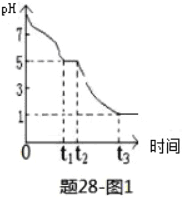

①0-t1段主要生成HSO3﹣,根据pH变化图,推测0-t1发生反应的离子方程式为_______________;
②t3时溶液中主要阴离子是_________,t2-t3阶段pH变小的主要原因是______________________。
③若t1时溶液中Na2S2O4全部被氧化成NaHSO3,此时溶液中c(SO32﹣)—c(H2SO3)=___mol·L﹣1(填准确值,不考虑溶液体积变化)。
(4)利用图2所示装置(电极均为惰性电极)也可使NaHSO3转化为Na2S2O4,并获得较浓的硫酸。
①a为电源的________(填“正极”或“负极”);
②阴极的电极反应式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探索生命现象中的有关微观变化,科学家常以 ![]() C标记的化合物为示踪剂,下列关于
C标记的化合物为示踪剂,下列关于 ![]() C的说法中正确的是( )
C的说法中正确的是( )
A.质量数是6
B.质子数是6
C.电子数是14
D.中子数是14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO和O2转化为NO2的反应机理如下:
①2NO(g)![]() N2O2(g)(快) △H1<0平衡常数K1
N2O2(g)(快) △H1<0平衡常数K1
②N2O2(g)+O2(g)![]() 2NO2(g)(慢) △H2<0平衡常数K2
2NO2(g)(慢) △H2<0平衡常数K2

下列说法正确的是( )
A. 2NO(g)+O2(g)![]() 2NO2(g)的△H=-(△H1+△H2)
2NO2(g)的△H=-(△H1+△H2)
B. 2NO(g)+O2(g)![]() 2NO2(g)的平衡常数K= K1/K2
2NO2(g)的平衡常数K= K1/K2
C. 反应②的速率大小决定2NO(g)+O2(g)![]() 2NO2(g)的反应速率
2NO2(g)的反应速率
D. 反应过程中的能量变化可用图a表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关仪器的使用方法或实验操作正确的是( )
A.用坩埚灼烧干海带制海带灰
B.蒸馏时,温度计水银球插入液面以下
C.用长颈漏斗分离CCl4萃取碘后的水层与有机层
D.用容量瓶配制溶液时,若加水超过刻度线,用胶头滴管吸出多余液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.电解MgCl2浓溶液制取金属MgB.可用铝热反应原理制取金属Mn
C.钠单质可以从TiCl4中置换出TiD.可用NH3还原CuO制备单质Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质的递变情况错误的是( )
A.Li,Be,B原子最外层电子数依次增多
B.N,O,F电负性依次增大
C.P,S,Cl元素最高正价依次升高
D.Na,K,Rb第一电离能逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将钠、铝、铁各1mol分别投入到等体积且同浓度的盐酸中,产生的氢气体积在相同条件下( )
A.钠可能最多
B.铝铁不可能一样多
C.铝一定最多
D.无法判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com