
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A.c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-
B.pH=1的溶液中:Fe2+、NO3-、SO42-
C.水电离出的c(H+)=10-12mol/L的溶液中:Ca2+、Cl-、HCO3-
D.c (Fe3+)=0.1mol/L的溶液中:K+、SO42-、SCN-
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中的每个字母表示一种短周期元素,回答下列问题:
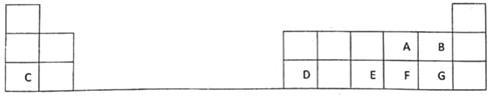
(1)画出A的原子结构示意图________。
(2)A、B、E、F、G五种元素所形成的气态氢化物最稳定的是________(填化学式)。
(3)D在元素周期表中的位置是第3周期________族。
(4)E、F元素的最高价氧化物对应水化物的酸性较强的是: ________(用化学式表示)。
(5)写出C和G形成化合物的电子式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.60gSiO2晶体中含有Si—O键数目为2NA
B.常温常压下,32g16O2中所含的中子数为16NA
C.电解饱和食盐水,阳极上生成22.4L气体时转移的电子数为2NA
D.密闭容器中2molNO与lmolO2充分反应,产物的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物F是一种重要的有机合成中间体,其合成路线如下图所示:
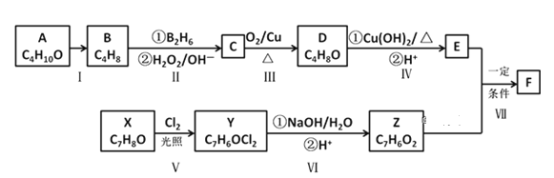
已知:①A的核磁共振氢谱图中显示两组峰
②F的结构简式为:
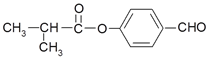
③通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
④R-CH=CH2![]() R-CH2CH2OH
R-CH2CH2OH
请回答下列问题:
(1)A的名称为______________(系统命名法);Z中所含官能团的名称是___________。
(2)反应Ⅰ的反应条件是__________。
(3)E的结构简式为_______________________。
(4)写出反应Ⅴ的化学方程式____________________________________________。
(5)写出反应IV中的化学方程式____________________________________________。
(6)W是Z的同系物,相对分子质量比Z大14,则W的同分异构体中满足下列条件:
①能发生银镜反应,②苯环上有两个取代基,③不能水解,遇FeCl3溶液不显色的结构共有_________种(不包括立体异构),核磁共振氢谱有四组峰的结构为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3溶液可以蚀刻印刷电路板上的Cu。某实验兴趣小组模拟该过程,并回收Cu和蚀刻液的流程如下:
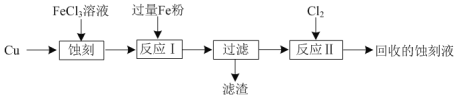
(1)“蚀刻”时的化学反应方程式为____。
(2) 滤渣的成分为____。
(3)“反应Ⅱ”的离子方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸是一种重要的化工原料,完成下列填空:
I、工业上生产硝酸的主要过程如下:
(1)以N2和H2为原料合成氨气。反应为:N2(g)+3H2(g) ![]() 2NH3(g)+Q。
2NH3(g)+Q。
(2)下列措施可以提高H2的转化率的是(填选项序号)_____________。
a.选择适当的催化剂 b.增大压强 c.及时分离生成的NH3 d.升高温度
(3)一定温度下,在密闭容器中充入1molN2和3molH2发生反应。若容器容积恒定,达到平衡状态时,气体的总物质的量是原来的15/16,则N2的转化率α1=_____;若容器压强恒定,达到平衡状态时,N2的转化率为α2,则α2___α1 (填“>”、“<”或“=”)。
II、以氨气、空气为主要原料制硝酸。
(4)氨气催化氧化的催化剂是___________;氨气也可以在纯氧中燃烧生成无毒、无污染的产物,其燃烧方程式为_____________。
(5)在容积恒定的密闭容器中进行反应2NO(g)+O2(g)![]() 2NO2(g)-Q。该反应的反应速率(v)随时间(t)变化的关系如图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)______。
2NO2(g)-Q。该反应的反应速率(v)随时间(t)变化的关系如图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)______。
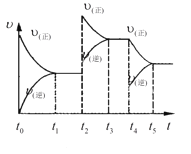
a.在t1-t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施可以是升高温度
c.在t3-t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
d.在t5时,容器内NO2的体积分数是整个过程中的最大值
III、硝酸厂常用如下2种方法处理尾气。
(6)催化还原法:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+ O2(g)→2H2O(g) + 483.6 KJ
N2(g)+ 2O2(g)→2NO2 (g) + 67.7KJ
则H2还原NO2生成水蒸气反应的热化学方程式是_________。
(7)碱液吸收法:用Na2CO3溶液吸收NO2生成CO2。若9.2gNO2和Na2CO3溶液完全反应时转移电子0.1mol,则反应的离子方程式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢是应用广泛的“绿色”氧化剂,酸性条件下稳定,中性或弱碱性条件下易分解.填空:
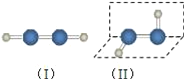
(1)过氧化氢的分子结构如图(Ⅱ),则过氧化氢属于__(极性/非极性)分子.过去曾经有人认为过氧化氢的分子结构也可能是(Ⅰ),选择合理实验方法证明过氧化氢的分子结构为(Ⅱ)__(选填编号).
a.测定过氧化氢的沸点
b.测定过氧化氢分解时的吸收的能量
c.测定过氧化氢中H﹣O和O﹣O的键长
d.观察过氧化氢细流是否在电场中偏转
Na2O2,K2O2以及BaO2都可与酸作用生成过氧化氢.实验室可用稀硫酸和过氧化物在用冰冷却的条件下反应制取过氧化氢.
(2)上述过氧化物中最适合的是__,反应完毕后__(填操作名称)即可得到双氧水.
(3)若反应时没有用冰冷却,会有气体产生,写出反应的化学方程式__.用酸性高锰酸钾溶液滴定双氧水的方法可以测定双氧水的浓度.
(4)取5.00mL 双氧水样品,配制成250mL溶液.此实验过程必须用到的两种主要仪器为__(填仪器名称).
(5)取25.00mL上述溶液,用0.020mol/L的酸性高锰酸钾溶液滴定,看到__,到达滴定终点,消耗高锰酸钾溶液15.50mL.则原双氧水样品中含过氧化氢__ g/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图Ⅰ是NO2(g)+CO(g) ![]() CO2(g)+NO(g)反应过程中能量变化的示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ所示。
CO2(g)+NO(g)反应过程中能量变化的示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ所示。

下列有关说法正确的是
A. 一定条件下,向密闭容器中加入1 mol NO2(g)与1 mol CO(g)反应放出234 kJ热量
B. 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
C. 若X表示温度,则Y表示的可能是CO2的物质的量浓度
D. 若X表示反应时间,则Y表示的可能是混合气体的密度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com