
【题目】异秦皮啶具有抗肿瘤功效,秦皮素具有抗痢疾杆菌功效。它们在一定条件下可发生转化,如图所示。有关说法正确的是
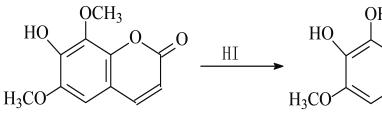
A. 异秦皮啶分子式为C11H10O5
B. 异秦皮啶与秦皮素互为同系物
C. 鉴别异秦皮啶与秦皮素可用FeCl3溶液
D. 1 mol秦皮素最多可与3 mol NaOH反应
【答案】A
【解析】
根据有机物的结构简式判断有机物所含元素种类以及原子个数,可确定有机物的分子式,异秦皮啶含有酚羟基,可发生取代、氧化反应,含有C=O,可发生加成反应,含有酯基,可发生水解反应,含有碳碳双键,可发生加成反应,由官能团的转化可知,异秦皮啶取代反应生成秦皮素,据此答题。
A.异秦皮啶分子式为C11H10O5,故A正确;
B.异秦皮啶与秦皮素中酚羟基的数目不同,结构不相似,不属于同系物,故B错误;
C.二者都含有酚羟基,都可与FeCl3溶液反应发生显色反应,故C错误;
D.秦皮素中含有酚羟基,对位上有1个H可被取代,含有碳碳双键,可发生加成反应,则1mol秦皮素最多可与2molBr2反应,水解产物中含有3个酚羟基和1个羧基,则1mol秦皮素最多可与4molNaOH反应,故D错误。
故选A。


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】氮和碳的化合物与人类生产、生活密切相关。
(1)已知:N2(g)+O2(g)===2NO(g); ΔH=+180.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g); ΔH=-483.6 kJ·mol-1
则反应2H2(g)+2NO(g)===2H2O(g)+N2(g);ΔH=__________。
(2)在压强为0.1 MPa条件,将CO和H2的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0
CH3OH(g) ΔH<0
①下列能说明该反应达到平衡状态的是________________。
a.混合气体的密度不再变化 b.CO和H2的物质的量之比不再变化
c.v(CO)=v(CH3OH) d.CO在混合气中的质量分数保持不变
②T1℃时,在一个体积为5 L的恒压容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.75,则T1℃时,CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数K=_______________________。
CH3OH(g)的平衡常数K=_______________________。

③在T1℃时,在体积为5 L的恒容容器中充入一定量的H2和CO,反应达到平衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。温度不变,当![]() 时,达到平衡状态,CH3OH的体积分数可能是图象中的___________点。
时,达到平衡状态,CH3OH的体积分数可能是图象中的___________点。
(3)用催化转化装置净化汽车尾气,装置中涉及的反应之一为:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)

①探究上述反应中NO的平衡转化率与压强、温度的关系,得到如图1所示的曲线。催化装置比较适合的温度和压强是___________。
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图2所示。则前10 s内,CO和NO百分含量没明显变化的原因是____________。

(4)如图所示的装置能吸收和转化NO2和SO2。
①阳极区的电极反应式为___________________________。
②阴极排出的溶液中含S2O![]() 离子,能将NO2气体转化为无污染气体,同时生成的SO
离子,能将NO2气体转化为无污染气体,同时生成的SO![]() 可在阴极区再生。写出该反应的离子方程式:___________________________。
可在阴极区再生。写出该反应的离子方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在甲、乙、丙、丁四个恒容密闭容器中投入H2和I2,发生反应:H2 (g) +I2 (g)![]() 2HI(g).反应体系中各物质浓度的有关数据如下。
2HI(g).反应体系中各物质浓度的有关数据如下。
容器 | 起始浓度 | 平衡浓度 | |
c(H2)/mol·L-1 | c(I2)/mol·L-1 | c(HI)/mol·L-1 | |
甲 | 0.01 | 0.01 | 0.004 |
乙 | 0.01 | 0.02 | a |
丙 | 0.02 | 0.01 | b |
丁 | 0.02 | 0.02 | —— |
下列判断正确的是
A. HI的平衡浓度:a=b>0.004
B. 平衡时,H2的转化率:丁>甲
C. 平衡时,乙中H2的转化率等于20%
D. 丙中条件下,该反应的平衡常数K=4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
① | ② | ③ |
|
|
|
在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是
A. 对比②③,可以判定Zn保护了Fe
B. 对比①②,K3[Fe(CN)6]可能将Fe氧化
C. 验证Zn保护Fe时不能用①的方法
D. 将Zn换成Cu,用①的方法可判断Fe比Cu活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应2NO(g)![]() N2(g)+O2(g)。若在某温度下达到平衡时C(N2)=0.05mol·L-1,C(O2)=0.05mol·L-1,c(NO)=0.1mol·L-1 该反应的平衡常数为_____________,保持温度不变,将容器体积缩小一半,则平衡常数_________(填增大、减小或不变)。
N2(g)+O2(g)。若在某温度下达到平衡时C(N2)=0.05mol·L-1,C(O2)=0.05mol·L-1,c(NO)=0.1mol·L-1 该反应的平衡常数为_____________,保持温度不变,将容器体积缩小一半,则平衡常数_________(填增大、减小或不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向100 mL某浓度H2A溶液中加入0.1 mol·L-1 NaOH溶液,所得溶液的pH随NaOH溶液体积的变化曲线如图所示,其中b、c为等当点(等当点指的是按某个方程式恰好反应的点)。下列有关说法不正确的是

A. 起始时,c(H2A)=0.1 mol·L-1
B. b点时:c(Na+)> c(A2-)>c(HA-) > c(H+)>c(OH-)
C. b→c段,反应的离子方程式为HA-+OH-===A2-+H2O
D. c→d段,溶液中A2-的水解程度逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】需要加入适当的氧化剂才能实现的反应
A. PCl3→PCl5 B. MnO4- →Mn2+ C. SO3→HSO4- D. CO2→H2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com