
【题目】验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
① | ② | ③ |
|
|
|
在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是
A. 对比②③,可以判定Zn保护了Fe
B. 对比①②,K3[Fe(CN)6]可能将Fe氧化
C. 验证Zn保护Fe时不能用①的方法
D. 将Zn换成Cu,用①的方法可判断Fe比Cu活泼
【答案】D
【解析】分析:A项,对比②③,②Fe附近的溶液中加入K3[Fe(CN)6]无明显变化,②Fe附近的溶液中不含Fe2+,③Fe附近的溶液中加入K3[Fe(CN)6]产生蓝色沉淀,③Fe附近的溶液中含Fe2+,②中Fe被保护;B项,①加入K3[Fe(CN)6]在Fe表面产生蓝色沉淀,Fe表面产生了Fe2+,对比①②的异同,①可能是K3[Fe(CN)6]将Fe氧化成Fe2+;C项,对比①②,①也能检验出Fe2+,不能用①的方法验证Zn保护Fe;D项,由实验可知K3[Fe(CN)6]可能将Fe氧化成Fe2+,将Zn换成Cu不能用①的方法证明Fe比Cu活泼。
详解:A项,对比②③,②Fe附近的溶液中加入K3[Fe(CN)6]无明显变化,②Fe附近的溶液中不含Fe2+,③Fe附近的溶液中加入K3[Fe(CN)6]产生蓝色沉淀,③Fe附近的溶液中含Fe2+,②中Fe被保护,A项正确;B项,①加入K3[Fe(CN)6]在Fe表面产生蓝色沉淀,Fe表面产生了Fe2+,对比①②的异同,①可能是K3[Fe(CN)6]将Fe氧化成Fe2+,B项正确;C项,对比①②,①加入K3[Fe(CN)6]在Fe表面产生蓝色沉淀,①也能检验出Fe2+,不能用①的方法验证Zn保护Fe,C项正确;D项,由实验可知K3[Fe(CN)6]可能将Fe氧化成Fe2+,将Zn换成Cu不能用①的方法证明Fe比Cu活泼,D项错误;答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在105℃、1个大气压时,取两种气态烃1L与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L。有下列组合的混合烃:①C2H4和C3H4 ②CH4和C2H6 ③CH4和C3H4 ④C2H2和C3H6,其中可能符合上述要求的是
A. 只有①②B. 只有①③④C. 只有①③D. 只有②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,已知电离常数:Kb ( N H3·H2O)=1.8×10-5;K![]() (H2C2O4)=5.9×10-2,K
(H2C2O4)=5.9×10-2,K![]() H2C2O4)=6.2×10-5。下列说法正确的是( )
H2C2O4)=6.2×10-5。下列说法正确的是( )
A. (N H4)2C2O4溶液中,c(NH![]() )=2c(C2O
)=2c(C2O![]() )
)
B. 等物质的量浓度的氨水和H2C2O4溶液等体积混合,所得溶液呈碱性
C. pH=11的氨水和pH=3的H2C2O4溶液等体积混合,所得溶液呈酸性
D. 用H2C2O4溶液中和氨水至中性时,溶液中。c(NH![]() )=2c(C2O
)=2c(C2O![]() )+c(HC2O
)+c(HC2O![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会生成副产物HCl,利用下列反应可实现氯的循环利用:
4HCl(g) + O2(g)![]() 2Cl2(g) + 2H2O(g) ΔH=-115.6 kJ/mol
2Cl2(g) + 2H2O(g) ΔH=-115.6 kJ/mol
恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是
A. 氯化氢的转化率不再改变 B. 气体的质量不再改变
C. 断开4 mol H-Cl键的同时生成4 mol H-O键 D. n(HCl)∶n(O2)∶n(Cl2)∶n(H2O)=4∶1∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.58 kJmol-1
CH3OH(g)+H2O(g) △H1=-49.58 kJmol-1
反应Ⅱ:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g)![]() CH3OH(g) △H3=-90.77 kJmol-1
CH3OH(g) △H3=-90.77 kJmol-1
回答下列问题:
(1)反应Ⅱ的△H2=__________,若反应Ⅰ、Ⅱ、Ⅲ平衡常数分别为K1、K2、K3,则K2=________(用K1、K3表示)。
(2)反应Ⅲ自发进行条件是___________(填“较低温度”、“较高温度”或“任何温度”)。
(3)在一定条件下2 L恒容密闭容器中充入3 mol H2和1.5 mol CO2,仅发生反应Ⅰ,实验测得不同反应温度与体系中CO2的平衡转化率的关系,如下表所示。
温度(℃) | 500 | T |
CO2的平衡转化率 | 60℅ | 40℅ |
①T______500℃(填“高于”或“低于”)。
②温度为500℃时,该反应10 min时达到平衡:
a.用H2表示该反应的速率为____________________;
b.该温度下,反应I的平衡常数K=______________。
(4)某研究小组将一定量的H2和CO2充入恒容密闭容器中并加入合适的催化剂(发生反应I、Ⅱ、Ⅲ),测得不同温度下体系达到平衡时CO2的转化率(a)及CH3OH的产率(b),如图所示。
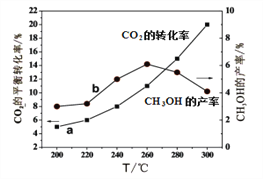
①该反应达到平衡后,为同时提高反应速率和甲醇的生成量,以下措施一定可行的是_____(选填编号)。
A.升高温度 B.缩小容器体积 C.分离出甲醇 D.增加CO2的浓度
②据图可知当温度高于260℃后,CO的浓度随着温度的升高而_________(填“增大”、“减小”、“不变”或“无法判断”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(![]() )中而形成的,电池总反应方程式为:8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是( )
)中而形成的,电池总反应方程式为:8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是( )
A. 电解质溶液中混入水,对电池反应无影响
B. 金属锂作电池的正极,石墨作电池的负极
C. 电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D. 电池工作过程中,金属锂提供的电子与正极区析出的硫的物质的量之比为4∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异秦皮啶具有抗肿瘤功效,秦皮素具有抗痢疾杆菌功效。它们在一定条件下可发生转化,如图所示。有关说法正确的是
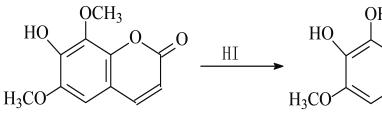
A. 异秦皮啶分子式为C11H10O5
B. 异秦皮啶与秦皮素互为同系物
C. 鉴别异秦皮啶与秦皮素可用FeCl3溶液
D. 1 mol秦皮素最多可与3 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛被视为“空气杀手”,可用如下方法检测:5HCHO+4MnO4-+12H+==4Mn2++5CO2+11H2O。下列说法不正确的是
A. 甲醛中存在极性键
B. CO2的电子式为![]()
C. MnO4-是氧化剂,CO2是氧化产物
D. 当有1.8 g甲醛参加反应时,转移电子的物质的量为0.12mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4 L CCl4中含CCl4分子数为NA
B. 5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等
C. 0.1 mo1·L-1 MgCl2溶液中含Cl-数为0.2NA
D. 3.9 g Na2O2 晶体中含有的离子总数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com