
【题目】把铝粉和某铁的氧化物(xFeO·yFe2O3)粉末配成铝热剂,分成两等份。一份在高温下恰好完全反应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两种情况下生成的气体质量比是5 : 7,则x : y为
A.1∶1B.1∶2C.5∶7D.7∶5
【答案】B
【解析】
第一份中Al与xFeOyFe2O3粉末得到Fe与Al2O3,再与足量盐酸反应,发生反应:Fe+2HCl=FeCl2+H2↑,第二份直接放入足量的烧碱溶液,发生反应:2Al+2NaOH+2H2O=NaAlO2+3H2↑,前后两种情况下生成的气体质量比是5:7,则令第一份、第二份生成氢气物质的量分别为5mol、7mol,根据方程式计算Fe、Al的物质的量,再根据第一份中Al与xFeOyFe2O3反应的电子转移守恒计算xFeOyFe2O3中Fe元素平均化合价,进而计算x、y比例关系。
第一份中Al与xFeOyFe2O3粉末得到Fe与Al2O3,再与足量盐酸反应,发生反应:Fe+2HCl=FeCl2+H2↑,第二份直接放入足量的烧碱溶液,发生反应:2Al+2NaOH+2H2O=NaAlO2+3H2↑,前后两种情况下生成的气体质量比是5:7,令第一份、第二份生成氢气物质的量分别为5mol、7mol,则:
![]()
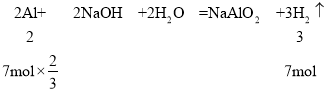
令xFeOyFe2O3中Fe元素平均化合价为a,根据Al与xFeOyFe2O3反应中的电子转移守恒:7mol×![]() ×3=5mol×(a0),解得a=2.8,故
×3=5mol×(a0),解得a=2.8,故![]() =2.8,整理得x:y=1:2,答案选B。
=2.8,整理得x:y=1:2,答案选B。


科目:高中化学 来源: 题型:
【题目】NH3可消除NO的污染,反应方程式为:6NO+4NH3→5N2+6H2O.现有NO与NH3的混合物1mol充分反应,若还原产物比氧化产物多1.4g.则下列判断中正确的是( )
A.产生氮气为5.6 L
B.有0.3 mol NO被还原
C.生成氧化产物2.8 g
D.原混合物中NO与NH3的物质的量之比可能为3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知相同温度下CH3COOH和NH3H2O的电离常数相等,现向10mL浓度为0.1molL﹣1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B.c(NH4+):c(NH3H2O)始终减小
C.c(CH3COOH)与c(CH3COO)之和始终保持不变
D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四川攀枝花蕴藏丰富的钒、钛、铁资源。用钛铁矿渣(主要成分为TiO2、FeO、Fe2O3,Ti的最高化合价为+4)作原料,生产白色颜料二氧化钛的主要步骤如下:
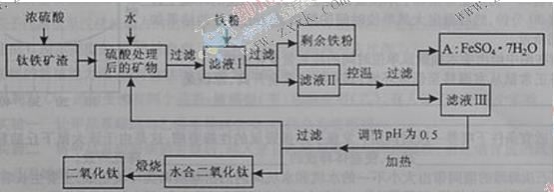
请回答下列问题:
(1)硫酸与二氧化钛反应的化学方程式是____________________________________。
(2)向滤液I中加入铁粉,发生反应的离子方程式为:_________________________、_______________________________________。
(3)在实际生产过程中,向沸水中加入滤液Ⅲ,使混合液pH达0.5,钛盐开始水解。水解过程中不断通入高温水蒸气,维持溶液沸腾一段时间,钛盐充分水解析出水合二氧化钛沉淀。请用所学化学平衡原理分析通入高温水蒸气的作用:_______________________________________________。
过滤分离出水合二氧化钛沉淀后,将滤液返回的主要目的是充分利用滤液中的钛盐、___________、______________、_______________________(填化学式),减少废物排放。
(4)A可用于生产红色颜料(Fe2O3),其方法是:将556a kg A(摩尔质量为278 g/mol)溶于水中,加入适量氢氧化钠溶液恰好完全反应,鼓入足量空气搅拌,产生红褐色胶体;再向红褐色胶体中加入3336b kg A和112c kg铁粉,鼓入足量空气搅拌,反应完成后,有大量Fe2O3附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料。若所得滤液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料_______________________kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,H3AsO4溶液中各含砷粒子分布分数(平衡时该粒子的浓度与各含砷粒子浓度之和的比)与pH的关系如右图所示。下列说法正确的是
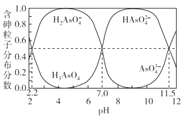
A. H3AsO4的第一步电离常数Ka1>0.01
B. pH=7.0时.溶液中c(AsO43-)=c(H3AsO4)=0
C. 0.1mol·L-1H3AsO4溶液的pH<2
D. pH=12时,c(H+)=3c(AsO43-)+2c(HAsO42-)+c(H2AsO4-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物的结构简式为:![]()
(1)该有机物中所含官能团的名称是________________,________________。
(2)该有机物发生加聚反应后,所得产物的结构简式为__________________。
(3)写出该有机物使溴水褪色的化学方程式____________________________。
(4)写出该有机物发生消去反应的化学方程式(注明反应条件)_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. ![]() 的一溴代物和
的一溴代物和![]() 的一溴代物都有4种(不考虑立体异构)
的一溴代物都有4种(不考虑立体异构)
B. CH3CH=CHCH3分子中的四个碳原子在同一直线上
C. 按系统命名法,化合物 的名称是2,3,4-三甲基-2-乙基戊烷
的名称是2,3,4-三甲基-2-乙基戊烷
D. 丙酸与甲酸甲酯互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1L 0.1mol/L的NaHS溶液中HS-和S2-离子数之和为0.1NA
B.2.0 g H218O与D2O的混合物中所含中子数为NA
C.1 mol Na2O2固体中含离子总数为4NA
D.3 mol Fe在足量的水蒸气中完全反应转移9NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知如表数据。
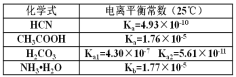
(1)25℃时,pH=11的NaCN溶液中水电离出的c(OH-)=_____molL-1。
(2)25℃时,等浓度的NaCN、Na2CO3溶液、CH3COONa三种溶液的pH值由大到小的顺序为_____。
(3)0.100molL-1NH4HCO3溶液中物质的量浓度最大的离子是_____(填化学式)。
(4)向NaCN溶液中通入少量CO2,所发生反应的化学方程式为_____。
(5)25℃1.10molL-1CH3COOH溶液中,CH3COOH的电离度约为_____。
(6)25℃时等体积等浓度的NaCl与NaCN两溶液中,离子总数NaCl_____NaCN(填“大于”、“小于”或“等于”);
(7)HCN与NaOH反应后的溶液中存在:c(Na+)=c(CN-),该溶液呈_____性(填“酸”“碱”或“中”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com