
【题目】我国自主研发的对二甲苯绿色合成项目取得新进展,其合成过程如图所示。
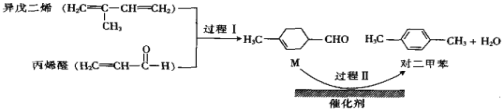
下列说法不正确的是( )
A.M的某种同分异构体含有苯环且能与钠反应放出氢气
B.可用溴水鉴别M和对二甲苯
C.对二甲苯的一氯代物有2种
D.异戊二烯所有碳原子可能共平面
科目:高中化学 来源: 题型:
【题目】下列各有机物同分异构体数目的判断中不正确的是
A | B | C | D | |
分子式 | C6H14 | C4H8Cl2 | C4H9Cl | C3H6 |
数目 | 5 | 8 | 4 | 2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019 年诺贝尔化学奖用于奖励对锂离子电池的发展做出贡献的三位科学家。锂离子电池如今被用于各个领域,使一个无化石燃料的社会成为可能。LiFePO4是新型锂离子电池的正极材料。某小组拟设计以一种锂辉石(主要成分为Li2O Al2O34SiO2,含少量铁、钙、镁)为原料制备纯净的碳酸锂,进而制备LiFePO4的工艺流程:
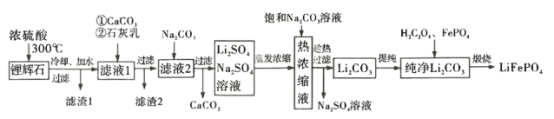
已知:Li2OAl2O34SiO2+H2SO4(浓)![]() Li2SO4+Al2O34SiO2H2O↓回答下列问题:
Li2SO4+Al2O34SiO2H2O↓回答下列问题:
(1)LiFePO4 中铁元素的化合价为_____,铁元素进行焰色反应的颜色是_______(填序号)。
A.无焰色反应 B.黄色 C.紫色 D.砖红色
(2)向滤液 1 中加入适量的 CaCO3 细粉用于消耗硫酸并将 Fe3+转化为红褐色沉淀,若![]() =3,反应的化学方程式为___;滤渣2 的主要成分是 Fe(OH)3、___(填化学式)
=3,反应的化学方程式为___;滤渣2 的主要成分是 Fe(OH)3、___(填化学式)
(3)已知碳酸锂在水中的溶解度随温度升高而减小,上述流程中趁热过滤的目的是__。
(4)流程中加H2C2O4和FePO4,用于煅烧制备 LiFePO4,该反应的化学方程式为____。
(5)若滤液1中c(Mg2+)=0.2 mol/L,向其中加入双氧水和磷酸(设溶液体积增加 1 倍),使Fe3+恰好沉淀完全即溶液中 c(Fe3+)=1.0×10-5 mol/L,此时是否有 Mg3 (PO4)2 沉淀生成?_____(列式计算说明)。已知 FePO4 、Mg3 (PO4)2 的 Ksp 分别为 1.3×10-22、1.0×10-24。(6)一种锂离子电池的反应原理为 LiFePO4![]() Li+FePO4。写出放电时正极电极反应式: ____。
Li+FePO4。写出放电时正极电极反应式: ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)![]() 的分子式为_____________。
的分子式为_____________。
(2)写出![]() 中官能团的名称_________________。
中官能团的名称_________________。
(3)相对分子质量为72且沸点最低的烷烃的结构简式为__________________。
(4)有机物M(![]() )为苯的同分异构体,M的二氯代物的同分异构体有_____种。
)为苯的同分异构体,M的二氯代物的同分异构体有_____种。
(5)聚偏二氯乙烯(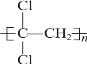 )具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
)具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
(6)写出异丁醛(![]() )与新制的氢氧化铜悬浊液共热的化学方程式:________。
)与新制的氢氧化铜悬浊液共热的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是
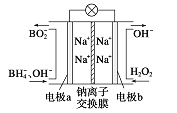
A. 该电池的负极反应为BH4-+8OH--8e-=BO2-+6H2O
B. 电池放电时Na+从b极区移向a极区
C. 每消耗3 mol H2O2,转移的电子为3 mol
D. 电极a采用MnO2作电极材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某实验小组模拟合成氨过程,通过仪器测得正反应速率与时间的图象如图所示,请回答相关问题:

①正反应速率呈现出先增大后减小的原因可能是____。
②v正-t图象中A、B、C、D四点属于平衡状态的是___点。
(2)将HI(g)置于密闭容器中,某温度下发生下列变化:2HI(g)H2(g)+I2(g) △H<0
①该反应平衡常数的表达式为K=____。
②当反应达到平衡时c(I2)=0.5mol/L,c(HI)=4mol/L,则c(H2)为___,HI的分解率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生做如下实验:第一步,在淀粉KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列有关该同学对实验原理的解释和所得结论的叙述不正确的是( )
A. 氧化性:ClO->I2>SO42—
B. 蓝色消失的原因是Na2SO3溶液具有漂白性
C. 淀粉KI溶液变蓝是因为I-被ClO-氧化为I2,I2使淀粉变蓝
D. 若将Na2SO3溶液加入氯水中,氯水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,△H1=-393.5 kJmol-1,△H2=-395.4 kJmol-1,下列说法或表示式正确的是( )
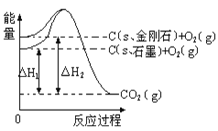
A. C(s、石墨)==C(s、金刚石)△H=+1.9kJmol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:

(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com