
【题目】下列单质或化合物性质的描述正确的是( )
A.NaHSO4水溶液显中性
B.NO2溶于水时发生氧化还原反应
C.SiO2与酸、碱均不反应
D.Fe在足量Cl2中燃烧生成FeCl2和FeCl3
【答案】B
【解析】解:A.NaHSO4在水中的电离方程式为:NaHSO4=Na++H++SO42﹣溶液呈酸性,故A错误;
B.NO2与水反应为3NO2+H2O═2HNO3+NO,反应中氮元素的化合价发生变化,由NO2中+4价升高为HNO3中+5价,由NO2中+4价降低为NO中+2价,NO2既是氧化剂也是还原剂,故B正确;
C.氢氟酸能和二氧化硅发生SiO2+4HF═SiF4↑+2H2O,玻璃中含有二氧化硅,常用此反应在玻璃上刻字;氢氧化钠能和二氧化硅发生2NaOH+SiO2═Na2SiO3+H2O,实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是玻璃中的SiO2与NaOH反应,生成具有粘性的Na2SiO3 , 会粘住瓶塞,故C错误;
D.氯气具有强氧化性,金属铁具有较强的还原性,氯气和金属反应生成高价金属,能将铁氧化成+3价的铁,氯气和金属铁反应的产物是氯化铁,Cl2与铁粉加热时发生反应的化学方程式为2Fe+3Cl2 ![]() FeCl3 , 故D错误;
FeCl3 , 故D错误;
故选B.
A.NaHSO4在水中能电离出氢离子显酸性;
B.NO2与水反应为3NO2+H2O═2HNO3+NO,反应中只有氮元素的化合价发生变化,NO2既是氧化剂也是还原剂;
C.氢氟酸能和二氧化硅反应,氢氧化钠能和二氧化硅反应;
D.氯气和金属反应生成高价金属,能将铁氧化成+3价的铁,氯气和金属铁反应的产物是氯化铁.


科目:高中化学 来源: 题型:
【题目】复合材料是指两种或两种以上材料组合成的一种新型材料。其中一种材料作为基体,另外一种材料作为增强剂,这样可发挥每一种材料的长处,并避免其弱点。下列物质中不属于复合材料的是( )
①聚苯乙烯树脂 ②铝塑管 ③涤棉织品 ④纯棉内衣
A. ①③ B. ①④ C. ②④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 质谱法可以测定物质的相对分子量
B. 物质的实验式就是其分子式
C. 从物质的红外光谱图可以获得分子中含有化学键或官能团的信息
D. 从核磁共振氢谱图可以推知该有机物分子有几种不同类型的氢原子及他们的数目
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如图所示. 
已知:各离子开始沉淀及完全沉淀时的pH如下表所示.
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe2+ | 6.34 | 9.7 |
Fe3+ | 1.48 | 3.2 |
Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)Ksp(ZnS)(选填“>”“<”或“=”).
(2)物质A可使用下列物质中的 .
A.KMnO4
B.O2
C.H2O2
D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在范围之间.
(4)物质B可直接用作氮肥,则B的化学式是 .
(5)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂﹣﹣K2FeO4 , 写出该反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的用途,说法不正确的是 ( )
A. 甲烷是一种热量高、污染小的清洁能源
B. 乙烯最重要的用途是作为植物生长调节剂
C. 乙醇是一种很好的溶剂,能溶解多种有机物和无机物
D. 酯类物质常用作饮料、糖果、香水、化妆品中的香料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl﹣与SO42﹣的物质的量之比为( ) 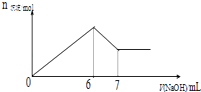
A.2:1
B.2:3
C.6:1
D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等,回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置是第①周期、第②族;PbO2的酸性比CO2的酸性③(填“强”或“弱”).
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为④ .
(3)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为⑤;PbO2也可以通过石墨为电极,Pb(NO3)2与Cu(NO3)2的混合溶液为电解液电解制取,阳极发生的电极反应式为⑥ , 阴极上观察到得现象是⑦;若电解液中不加入Cu(NO3)2 , 阴极发生的电极反应式为⑧ , 这样做的主要缺点是⑨ .
(4)PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重4.0%(即 ![]() ×100%)的残留固体.若a点固体组成表示为PbOx或mPbO2nPbO,列式计算x值和m:n值⑩ .
×100%)的残留固体.若a点固体组成表示为PbOx或mPbO2nPbO,列式计算x值和m:n值⑩ . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2.5L的恒容密闭容器中发生如下反应:CO2(g)+H2S(g)![]() COS(g)+H2O(g)
COS(g)+H2O(g)
实验 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 | |
CO2 | H2S | H2O | |||
I | 607 | 0.11 | 0.41 | 0.01 | |
II | 607 | 0.22 | 0.82 | ||
III | 620 | 0.1 | 0.4 | 6.74×10-3 | |
下列说法不正确的是( )
A. 该反应正反应为吸热反应
B. 607K时,把物质的量均为0.1mol四种反应物加入该反应器中,反应将向正反应方向进行
C. 实验Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D. 实验Ⅲ中,无论是开始还是至化学平衡状态,混合气体的密度始终不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法不正确的是

A. 图中五点Kw间的关系:B>C>A=D=E
B. 若从A点到D点,可采用在水中加入少量酸的方法
C. 若从A点到C点,在温度不变时向水中加入适量NH4Cl固体
D. 若处在B点时,将pH=2的硫酸与pH=10的KOH溶液等体积混合后,溶液显中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com