
【题目】一定温度下用过量铁块与稀硫酸反应制取氢气,采取下列措施:①将铁块换为等质量的铁粉;②加入少量![]() 溶液;③加入少量
溶液;③加入少量![]() 固体;④加入少量水;⑤加热;⑥将稀硫酸换为98%的硫酸,其中可提高反应速率的措施有
固体;④加入少量水;⑤加热;⑥将稀硫酸换为98%的硫酸,其中可提高反应速率的措施有
A.①③④B.①③⑤C.②④⑤D.②⑤⑥
【答案】B
【解析】
①将铁块换为等质量的铁粉,使反应物之间接触面积增大,能够提高化学反应速率;
②加入少量![]() 溶液,溶液中发生反应实质改变,短时间内不再产生氢气,加入溶液使混合溶液体积增大,氢离子浓度降低,产生氢气的化学反应对应速率将降低;
溶液,溶液中发生反应实质改变,短时间内不再产生氢气,加入溶液使混合溶液体积增大,氢离子浓度降低,产生氢气的化学反应对应速率将降低;
③加入少量![]() 固体,因氧化性Cu2+>H+,故铁先与Cu2+反应:Fe+Cu2+=Fe2++Cu,析出的铜单质附着在铁表面,此时装置构成了Fe-稀硫酸-Cu原电池,能够加快化学反应速率;
固体,因氧化性Cu2+>H+,故铁先与Cu2+反应:Fe+Cu2+=Fe2++Cu,析出的铜单质附着在铁表面,此时装置构成了Fe-稀硫酸-Cu原电池,能够加快化学反应速率;
④加入少量水,溶液中氢离子浓度降低,化学反应速率降低;
⑤加热能够提高微粒运动速率,能够加快化学反应速率;
⑥将稀硫酸换为98%的硫酸,溶液中发生的化学反应实质发生了该变,不再产生氢气,且随着反应的进行,铁表面形成致密氧化膜而导致钝化,反应后续几乎停止,化学反应速率降低;
综上所述,答案为B。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 将pH均为a的NaOH溶液和氨水分别加水稀释100倍,pH分别变为b和c,则a、b、c的大小关系为b>c>a
B. 常温下0.1 molL-1 KHA溶液的pH=3,则该溶液中C(A2- )<c(H2A)
C. 室温时 M(OH)2(s)![]() M2+(aq)+2OH-(aq) Ksp=a,则当 c(M2+)=b molL-1 时,溶液的pH为14 +
M2+(aq)+2OH-(aq) Ksp=a,则当 c(M2+)=b molL-1 时,溶液的pH为14 +![]() 1g
1g![]()
D. 0.1 molL-1 Na2CO3溶液:c(OH-)=c(H+)+c(HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.按要求写出下列化学方程式或离子方程式。
(1)铝与氢氧化钠溶液反应的离子方程式_________________________________
(2)7.80g乙炔气体完全燃烧生成二氧化碳和液态水,放出389.9kJ的热量,写出反应的热化学方程式_______________________________
(3)氢氧燃料电池是最常见的燃料电池,电解质溶液通常是KOH溶液,写出负极电极反应式______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】E具有果香味,由常见有机物合成E的路线如图,请回答:

(1)反应①的反应类型_______,C的名称________,F中含氧官能团名称________;
(2)检验物质F所用的试剂为_____。C转化为D所用的试剂可以是__________。
(3)下列关于物质B的说法正确的是________。
A.B为苯的同系物
B.常温常压下物质B呈气态
C.一定条件下,1 mol B最多能与4 mol H2发生加成
D.B既能使KMnO4溶液褪色又能使Br2/CCl4 溶液褪色
(4) E在氢氧化钠溶液中水解的化学方程式是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员利用![]() 水解生成的盐酸和石灰石
水解生成的盐酸和石灰石![]() 含少量
含少量![]() 、
、![]() 、
、![]() 、
、![]() 杂质
杂质![]() 生产医用二水合氯化钙晶体的简化工艺流程为图1:
生产医用二水合氯化钙晶体的简化工艺流程为图1:
已知:![]() 、
、![]() 完全沉淀的pH分别是
完全沉淀的pH分别是![]() 、
、![]() .
.
回答下列问题:
(1)滤渣A的主要成分是____________;操作X的方法为____________.
(2)控制在![]() 时
时![]() 水解的化学方程式为____________.
水解的化学方程式为____________.
(3)![]() 含80%CaCCO3的石灰石理论上最多能生成
含80%CaCCO3的石灰石理论上最多能生成![]() 的质量为____________t,制得的二水合氯化钙晶体中存在的少量杂质可能是____________.
的质量为____________t,制得的二水合氯化钙晶体中存在的少量杂质可能是____________.
(4)尾气中含污染气体![]() ,利用图2所示电化学装置可吸收
,利用图2所示电化学装置可吸收![]() 气体,从而减少大气污染,阳极的电极反应式为____________.
气体,从而减少大气污染,阳极的电极反应式为____________.

(5)制二水合氯化钙晶体所需热量可由甲醇燃烧提供,如图3为一定条件下![]() 与
与![]() 发生反应时,生成CO、
发生反应时,生成CO、![]() 或HCHO的能量变化图
或HCHO的能量变化图![]() 反应物
反应物![]() 和生成物
和生成物![]() 已略去
已略去![]() 则
则![]() 的
的![]() ____________.
____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿是一种重要的铜矿石,主要含有硫化亚铜(Cu2S),还有Fe2O3、SiO2及一些不溶性杂质。一种以辉铜矿石为原料制备硝酸铜晶体的工艺流程如下:

已知:部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Mn2+ | 8.3 | 9.8 |
Cu2+ | 4.4 | 6.4 |
回答下列问题
(1)浸取后得到的浸出液中含有CuSO4、MnSO4。写出浸取时产生CuSO4、MnSO4反应的化学方程式__________。
(2)调节pH的目的是___________,pH的调节范围为___________。
(3)生成MnCO3沉淀的离子方程式为___________。
(4)操作A为___________。
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2(g)═ 2Cu2O(s)+ 2SO2(g)△H=﹣768.2kJ/mol
2Cu2O(s)+ Cu2S(s)═ 6Cu(s)+ SO2(g)△H=" +116.0" kJ/mol
则由Cu2S与O2加热反应生成Cu的热化学方程式为___________。
(6)若用含85% Cu2S(Mr=160)的辉铜矿来制备无水Cu(NO3)2,假设浸取率为95%,调节pH时损Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.6 kg这样的辉铜矿最多能制备__________mol无水Cu(NO3)2。(计算结果精确到小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
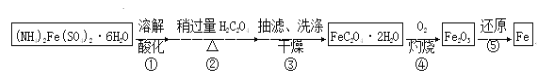
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。
请回答:
(1)下列操作或描述正确的是________。
A.步骤②,H2C2O4稍过量主要是为了抑制Fe2+水解
B.步骤③,采用热水洗涤可提高除杂效果
C.步骤③,母液中的溶质主要是(NH4)2SO4和H2C2O4
D.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(2)如图装置,经过一系列操作完成步骤③中的抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):

开抽气泵→a→b→d→________→c→关抽气泵。
a.转移固液混合物;b.关活塞A;c.开活塞A;d.确认抽干;e.加洗涤剂洗涤
抽滤和普通过滤相比,优点是___________________________________________。
(3) 称取一定量的FeC2O4·2H2O试样,用硫酸溶解,
采用KMnO4滴定法测定,折算结果如下:
n(Fe2+)/mol | n( | 试样中FeC2O4·2H2O的质量分数 |
9.80×10ˉ4 | 9.80×10ˉ4 | 0.980 |
由表中数据推测试样中最主要的杂质是____________________。
(4)实现步骤④必须用到的两种仪器是____________________
(供选仪器:a.烧杯;b.坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶);
该步骤的化学方程式是______________________________________。
(5)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体A、B分别为0.6 mol和0.5 mol,在0.4 L密闭容器中发生反应:3A+BaC+2D,经5 min后,此时C为0.2mol,又知在此反应时间内,D的平均反应速率为0.1 mol·(L·min)-1,下列结论正确的是( )
A.A的平均反应速率为0.1 mol·(L·min)-1B.a值为2
C.B的转化率为50%D.此时,反应混合物总的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出NaHSO4溶液的电离方程式_____; 写出Na2CO3水解的离子方程式_____ ;
(2)25℃时,pH= a的NaOH溶液中, 溶液的C(OH-) =_____ mol/L。
(3)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:(请用相应字母填)
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是______。
②同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是_____。
③若三者pH相同且体积相等,中和NaOH的能力由大到小的顺序是________。
(4)有下列盐溶液:①MgCl2 ②KNO3 ③KClO ④CH3COONH4 ⑤NaCN⑥Fe2(SO4)3,呈酸性的是________,呈碱性的是________,呈中性的是________(用相应的序号填写)。
(5)请写出明矾(K Al(SO4)212H2O)做净水剂净水时的离子方程式____________;
(6)请写出泡沫灭火器(硫酸铝和碳酸氢钠溶液)灭火时发生反应的离子方程式:____________;
(7)物质的量浓度相同的 氯化铵;②碳酸氢铵;③ 硫酸氢铵;④硫酸铵4种溶液中,c(![]() )由大到小的顺序是_____ (请用相应的序号填写)
)由大到小的顺序是_____ (请用相应的序号填写)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com