
【题目】钠离子电池相比锂离子电池具有高安全、长寿命、低成本的特点,有望成为下一代电池。某钠离子电池放电时的总反应为Na(1-x)MO2+NaxCn═NaMO2+nC,如图表示其充电过程。有关该电池的说法错误的是( )
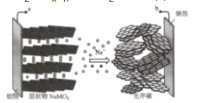
A.充电时,a与外加电源正极相连
B.放电时,外电路电子由b流向a
C.充电时,无序碳上发生的反应为nC+xNa++xe-═NaxCn
D.用该电池电解精炼铜,当电池中迁移1molNa+时,理论上可获得64g纯铜
【答案】D
【解析】
根据题意,该装置为电解池装置,根据电解池的工作原理,以及Na+移动的方向,推出b电极为阴极,a电极为阳极,对电池充电时,电池的正极接电源的正极,电池的负极接电源的负极,据此分析;
A. 根据图示,Na+从左向右移动,根据电解池工作原理,阳离子向阴极区移动,即电极b为阴极,电极a为阳极,电极a与外加电源正极相连,故A说法正确;
B. 充电时,电池的正极接电源的正极,电池的负极接电源的负极,推出放电时电极a为正极,电极b为负极,外电路电子由b流向a,故B说法正确;
C. 根据放电的总反应,推出充电时,无序碳上发生的反应式为nC+xNa++xe-=NaxCn,故C说法正确;
D. 精炼铜时,阴极反应式为Cu2++2e-=Cu,当电池中迁移1molNa+,说明电路中通过1mole-,即获得纯铜的质量为![]() =32g,故D说法错误;
=32g,故D说法错误;
答案:D。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法错误的是
A.常温常压下,4gD2O中含有的电子数为2NA
B.42gC2H4和C4H8的混合气中含有氢原子数为6NA
C.H2O(g)通过Na2O2(s)使其增重bg时,反应中转移的电子数为![]()
D.25℃时,1LpH=1的HCl溶液中含有的H原子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的发展和环保要求不断提高,CO2的捕集利用技术成为研究的重点。
Ⅰ.工业上使用的捕碳剂有NH3和(NH4)2CO3,它们与CO2可发生如下可逆反应:
NH3(l)+H2O(l)+CO2(g)![]() NH4HCO3(aq) ΔH1
NH4HCO3(aq) ΔH1
2NH3(l)+H2O(l)+CO2(g)![]() (NH4)2CO3(aq) ΔH2
(NH4)2CO3(aq) ΔH2
(NH4)2CO3(aq)+H2O(l)+CO2(g)![]() 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
则ΔH3=_________________(用含ΔH1、ΔH2的代数式表示)。
Ⅱ.目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的化学反应方程式为CO2(g)+4H2(g)![]() CH4(g)+2H2O(g),已知:H2的体积分数随温度的升高而增加。
CH4(g)+2H2O(g),已知:H2的体积分数随温度的升高而增加。
(1)该反应的ΔS________0(填“>”“<”或“=”),该反应的ΔH________0(填“>”或“<”)。
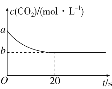
(2)在恒容密闭容器中通入等物质的量的CO2和H2并发生上述反应,T ℃下,CO2物质的量浓度c(CO2)随时间t变化的曲线如图所示。下列能说明反应达到平衡状态的是________(填字母代号)。
A.体系压强保持不变
B.混合气体密度保持不变
C.甲烷和水蒸气的物质的量之比保持不变
D.H2的质量分数保持不变
(3)T℃下,反应前20 s的平均反应速率v(H2)=______________(用含a、b的代数式表示)。
(4)T℃下,该反应的平衡常数K=_________________________(用含a、b的代数式表示)。
(5)若降低温度,反应重新达到平衡,则v(正)________;CO2转化率________(填“增大”“减小”或“不变”)。
Ⅲ.工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图所示:
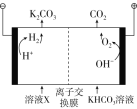
(1)在阳极区发生的反应包括___________________________________和H++HCO3-=CO2↑+H2O。
(2)简述CO32-在阴极区再生的原理:____________________________。
(3)NH3·BH3+3H2O2=NH4BO2+4H2O。下列说法正确的是___________。
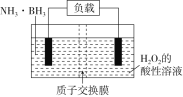
A.电流从左侧电极经过负载后流向右侧电极
B.BO2-通过质子交换膜向正极移动
C.负极附近溶液pH增大
D.正极的反应式为3H2O2+6H++6e-=6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是几种苯的同系物,回答下列问题:
①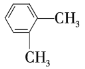 ②
②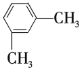 ③
③![]() ④
④![]() ⑤
⑤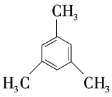 ⑥
⑥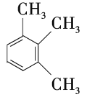 ⑦
⑦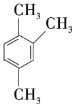
(1)①②③之间的关系是______。
(2)按习惯命名法命名,②的名称为______;按系统命名法命名,③⑥的名称分别为______、______。
(3)以上7种苯的同系物中苯环上的一氯代物只有一种的是______(填序号),④苯环上的一氯代物有______种。
(4)④的同分异构体有多种,除⑤⑥⑦外,写出苯环上一氯代物有2种,且与④互为同分异构体的有机物的结构简式:______,它的系统名称为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在海洋碳循环中,通过如图所示的途经固定碳。下列说法错误的是( )
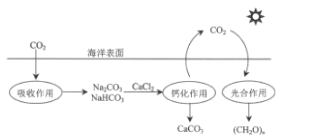
A.该循环过程中未涉及氧化还原反应
B.光合作用能将太阳能转化为化学能
C.钙化作用涉及的离子方程式之一为Ca2++2HCO3-═CaCO3↓+CO2↑+H2O
D.吸收作用中产生HCO3-的途径为CO2+H2OH2CO3,H2CO3HCO3-+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素及其衍生物在医药、农药、染科等领域有广泛用途。某香豆素衍生物Ⅰ具有抗病毒、抗癌的动多种生物活性,其合成路线如图所示:
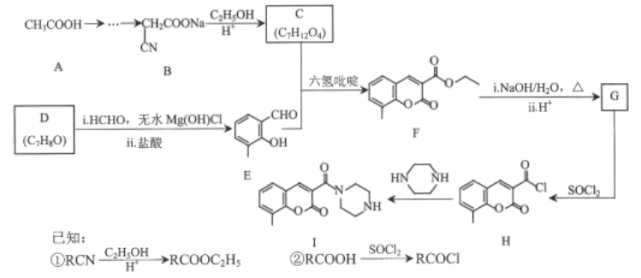 回答下列问题:
回答下列问题:
(1)D的名称是______。F中的含氧官能团的名称是______。
(2)H→I的反应类型为______。
(3)C分子具有对称结构,该化合物的结构简式为______。
(4)F→G中i的化学方程式为______。
(5)E的同分异构体中,满足下列条件的有______种;
①含有苯环
②能发生水解反应
其中核磁共振氢谱有4组峰且峰面积之比为3:2:2:1的结构简式为______(写出一种即可)。
(6)根据上述路线,设计以苯酚、乙醇、丙二酸、甲醛为原料制备![]() 的合成路线______(其他无机试剂自选)。
的合成路线______(其他无机试剂自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有U、V、W、X、Y、Z六种前四周期元素,原子序数依次增大,其相关信息如下表:
元素编号 | 相关信息比 |
U | 所处的周期数、族序数分别与其原子序数相等 |
V | 基态时,电子分布在三个能级上,且各能级中电子数相等 |
W | 基态时, 2p 轨道处于半充满状态 |
X | 自然界中含量最多 |
Y | 是第四周期元素中未成对电子数最多的元素 |
请回答下列问题:
(1)W、X、V第一电离能由大到小顺序:________________________(用元素符号表示)
(2)V的最高价氧化物对应含氧酸中,酸根的立体构型为:_________,中心原子的杂化方式为:_______________;
(3)Y的基态原子的价电子排布图为____________________________;
(4)乙和丙分别是V和X的氢化物,这两种氢化物分子中都含有10个电子。两者沸点的关系为乙______丙(填“>”或“<”),原因是__________________________________________;
(5)V与W原子结合形成的V3W4晶体,其硬度比金刚石大,则V3W4晶体中属于____________晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列6种有机物: ①CH3CH2CH2CH3②![]() ③
③![]() ④
④![]() ⑤
⑤![]() ⑥
⑥![]() 请回答:
请回答:
(1)属于醇类的是_________(填序号).
(2)与①互为同分异构体的是________(填序号).
(3)与④互为同系物的是_________(填序号).
(4)用系统命名法给③命名,其名称为__________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知:①pOH=-lgc(OH-);②N2H4 +H2O![]() N2H5++OH-、N2H5++H2O
N2H5++OH-、N2H5++H2O![]() N2H62++OH-,分别对应有pOH1和pOH2。常温下,将盐酸滴加到N2H4的水溶液中,混合溶液中pOH随离子浓度变化的关系如图所示。下列叙述错误的是
N2H62++OH-,分别对应有pOH1和pOH2。常温下,将盐酸滴加到N2H4的水溶液中,混合溶液中pOH随离子浓度变化的关系如图所示。下列叙述错误的是
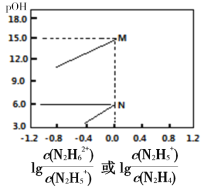
A.曲线M表示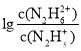 变化关系
变化关系
B.N2H4与硫酸形成的酸式盐的化学式为N2H5HSO4
C.pOH1>pOH2
D.反应N2H5+ + H2O ![]() N2H62+ + OH-的K=10-15
N2H62+ + OH-的K=10-15
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com