
【题目】11.2g 铁粉与足量稀盐酸恰好完全反应.请计算.
(1)生成氢气的物质的量;
(2)这些氢气在标准状况下的体积.
【答案】
(1)解:11.2g金属铁的物质的量为: ![]() =0.2mol,
=0.2mol,
铁与盐酸恰好反应,所得溶液为氯化亚铁溶液,设反应生成氢气的物质的量为xmol,则:
Fe+ | 2HCl | = | FeCl2+ | H2↑ |
1 | 1 | |||
0.2mol | x |
即 ![]() =
= ![]() ,解得:x=0.2mol,
,解得:x=0.2mol,
答:生成氢气的物质的量为0.2mol
(2)解:标准状况下0.2mol氢气的体积为:V(H2)=nVm=0.2mol×22.4L/mol=4.48L,
答:生成的氢气在标准状况下的体积为4.48
【解析】(1)根据n= ![]() 计算出11.2gFe的物质的量,然后根据反应方程式Fe+2HCl=FeCl2+H2↑计算出生成氢气的物质的量;(2)根据V(H2)=nVm计算出生成的氢气在标准状况下的体积.
计算出11.2gFe的物质的量,然后根据反应方程式Fe+2HCl=FeCl2+H2↑计算出生成氢气的物质的量;(2)根据V(H2)=nVm计算出生成的氢气在标准状况下的体积.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】标准盐酸滴定未知浓度氢氧化钠溶液,适宜的指示剂及终点颜色变化是
A. 酚酞,红色变为无色B. 甲基橙,黄色变橙色
C. 酚酞,红色变浅红色D. 甲基橙,黄色变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关生物大分子的叙述,正确的是
A. 组成生物大分子的单体都是以碳链为基本骨架
B. 糖类、蛋白质和核酸都是生物大分子
C. 构成生物大分子核酸的单体是核糖、磷酸和碱基
D. 生物大分子的主要功能是为细胞提供能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)9.8gH2SO4的物质的量是;2.0molH2O的质量是 .
(2)含Al3+5.4g的硫酸铝的物质的量为 , 其中含SO42﹣个.
(3)某二价金属1.6g在氧气中完全燃烧生成2g氧化物,则该金属的相对原子量 .
(4)6.02×1023个CO2与molH2质量相等,与gSO2含有的氧原子数相等.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或两种,现将6.9g样品溶于足量水中,得到澄清溶液,若再加入过量的CaCl2溶液,得到4.5g沉淀,对样品所含杂质的正确判断是( )
A.肯定有KNO3和Na2CO3 , 没有Ba(NO3)2
B.肯定有KNO3 , 没有Ba(NO3)2 , 可能还有Na2CO3
C.肯定没有Na2CO3和Ba(NO3)2 , 可能有KNO3
D.以上判断都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如图转化关系(反应中生成的水已略去). 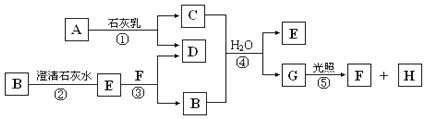
请回答以下问题:
(1)E是(填化学式),G是(填名称);
(2)C物质在日常生活中可作;
(3)写出反应①的化学方程式; C与浓盐酸反应,可以生成A气体,写出反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度下,纯水的c(H+)=2×10- 7 mol·L-1,则此时c(OH-)为______;若温度不变,滴入稀盐酸使c(H+)=5×10- 4 mol·L-1则溶液中由水电离产生的c(H+)为______,此时温度______(填“高于”、“低于”或“等于”)25℃。
(2)已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ/mol
②H2(g)+![]() O2(g)===H2O(g) ΔH2=-242.0 kJ/mol
O2(g)===H2O(g) ΔH2=-242.0 kJ/mol
③CO(g)+![]() O2(g)===CO2(g) ΔH3=-283. 0 kJ/mol
O2(g)===CO2(g) ΔH3=-283. 0 kJ/mol
写出C(s)与水蒸气反应生成CO和H2的热化学方程式:
_________________________________________________。
(3)常温下,取物质的量浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得混合液的pH=12,则原溶液的物质的量浓度为______。(溶液体积变化忽略不计)
(4)常温下,0.l mol·L-1 H3PO4溶液的pH小于7,括号内离子浓度的大小顺序为(H2PO4- 、HPO42- 、PO43- 、OH- 和H +)___________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,有关零排放车载燃料电池叙述正确的是( ) 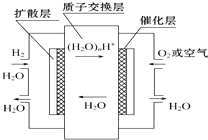
A.正极通入H2 , 发生还原反应
B.负极通入H2 , 发生还原反应
C.总反应式为2H2+O2=2H2O
D.导电离子为质子,且在电池内部由正极定向移向负极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com