
【题目】碳、硫、氮及其化合物在工农业、国防等领域占有重要地位。
(1)已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
若16gCH4和NO2充分反应,生成N2、CO2(g)和H2O(g),共放出热量867kJ,则△H2=___。
(2)工业生产中产生的SO2废气若用Na2SO3溶液吸收,得到浓度均为0.1mol·L-1的Na2SO3、NaHSO3混合溶液,则![]() =__。经测定,所得溶液呈酸性,则溶液中离子浓度由大到小的顺序为___。
=__。经测定,所得溶液呈酸性,则溶液中离子浓度由大到小的顺序为___。
(3)N2O4与NO2之间存在反应N2O4(g)2NO2(g)。在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系v(N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2),其中k1、k2是与反应温度有关的常数。相应的速率-分压强关系如图所示,一定温度下,k1、k2与平衡常数Kp(用平衡分压代替平衡浓度计算)的关系是k1=__,在图上标出的点中,能表示反应达到平衡状态的点为__(填字母代号)。

(4)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成1molN2时,转移的电子为___mol。
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(装置见图1)。反应相同时间NOx的去除率随反应温度的变化曲线如图2所示,在50~250℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是___;当反应温度高于380℃时,NOx的去除率迅速下降的原因可能是___。

【答案】-1160kJ·mol-1 1.5 c(Na+)>c(SO32-)>c(HSO3-)>c(H+)>c(OH-) ![]() K2Kp B、D
K2Kp B、D ![]() 迅速上升段是催化剂活性随温度升高增大,与温度升高共同使NOx去除反应速率迅速增大;上升阶段缓慢主要是温度升高引起的NOx去除反应速率增大但是催化剂活性下降 氨气在该条件下与氧气反应生成NO
迅速上升段是催化剂活性随温度升高增大,与温度升高共同使NOx去除反应速率迅速增大;上升阶段缓慢主要是温度升高引起的NOx去除反应速率增大但是催化剂活性下降 氨气在该条件下与氧气反应生成NO
【解析】
(1)CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ/mol①,CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2②,将方程式①+②得2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O(g)△H=(-574+△H2)kJ/mol;16g甲烷的物质的量是1mol,根据方程式知,2mol甲烷完全反应放出热量(574-△H2)kJ热量,1mol甲烷完全反应放出867kJ热量,据此计算△H2;
(2)浓度均为0.1molL-1的Na2SO3、NaHSO3混合溶液中存在物料守恒,2n(Na)=3n(C);
(3)当达到化学平衡时满足v正=v逆,据此求算化学平衡常数表达式,根据消耗速率2v(N2O4)=v(NO2)判断化学平衡的点;
(4)①NH3与NO2生成N2的反应中,反应方程式为8NH3+6NO2=7N2+12H2O,该反应中生成7 mol N2时,转移的物质的量为8mol×3=24mol,据此计算生成1mol氮气转移电子物质的量;
②在一定温度范围内催化剂活性较大,超过其温度范围,催化剂活性降低;在温度、催化剂条件下,氨气能被催化氧化生成NO。
![]() ,
,![]() ,将方程式
,将方程式![]() 得:
得:![]() ;16g甲烷的物质的量是1mol,根据方程式知,2mol甲烷完全反应放出热量
;16g甲烷的物质的量是1mol,根据方程式知,2mol甲烷完全反应放出热量![]() 热量,1mol甲烷完全反应放出867kJ热量,
热量,1mol甲烷完全反应放出867kJ热量,![]() ,
,![]()
![]() ;
;
![]() 浓度均为
浓度均为![]() 的
的![]() 、
、![]() 混合溶液中存在物料守恒,
混合溶液中存在物料守恒,![]() ;
;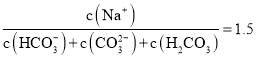 ,等浓度的亚硫酸钠和亚硫酸氢钠溶液中亚硫酸氢根离子电离程度大于其亚硫酸根离子水解,溶液显酸性,离子浓度:
,等浓度的亚硫酸钠和亚硫酸氢钠溶液中亚硫酸氢根离子电离程度大于其亚硫酸根离子水解,溶液显酸性,离子浓度: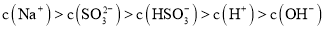 ;
;
![]() 当达到化学平衡时满足
当达到化学平衡时满足![]() ,即消耗速率
,即消耗速率![]() ,又有
,又有![]() ,
,![]() ,则
,则![]() 、
、![]() 与平衡常数
与平衡常数![]() 的关系为
的关系为![]() ;根据
;根据![]() ,则可以表示化学平衡的点为B点和D点;
,则可以表示化学平衡的点为B点和D点;
![]() 与
与![]() 生成
生成![]() 的反应中,反应方程式为
的反应中,反应方程式为![]() ,该反应中生成
,该反应中生成![]() 时,转移的物质的量为
时,转移的物质的量为![]() ,则生成1mol氮气转移电子物质的量
,则生成1mol氮气转移电子物质的量![]() ;
;
![]() 在一定温度范围内催化剂活性较大,超过其温度范围,催化剂活性降低,根据图知,迅速上升段是催化剂活性随温度升高增大,与温度升高共同使
在一定温度范围内催化剂活性较大,超过其温度范围,催化剂活性降低,根据图知,迅速上升段是催化剂活性随温度升高增大,与温度升高共同使![]() 去除反应速率迅速增大;上升阶段缓慢主要是温度升高引起的
去除反应速率迅速增大;上升阶段缓慢主要是温度升高引起的![]() 去除反应速率增大但是催化剂活性下降;在温度、催化剂条件下,氨气能被催化氧化生成NO,当反应温度高于
去除反应速率增大但是催化剂活性下降;在温度、催化剂条件下,氨气能被催化氧化生成NO,当反应温度高于![]() 时,
时,![]() 的去除率迅速下降的原因可能是氨气在该条件下与氧气反应生成NO。
的去除率迅速下降的原因可能是氨气在该条件下与氧气反应生成NO。


 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】以“赏中华诗词、寻文化基因、品生活之美”为基本宗旨的![]() 中国诗词大会
中国诗词大会![]() 不仅弘扬了中国传统文化,还蕴含着许多化学知识,下列诗词分析不正确的是
不仅弘扬了中国传统文化,还蕴含着许多化学知识,下列诗词分析不正确的是![]()
![]()
A.王安石诗句“爆竹声中一岁除,春风送暖入屠苏”,爆竹的燃放涉及氧化还原反应
B.诗句“只要功夫深,铁杵磨成针”,该过程只涉及物理变化
C.杜牧诗句“烟笼寒水月笼沙,夜泊秦淮近酒家”,此处的“烟”指固体小颗粒
D.曹植诗句“煮豆燃豆萁,豆在釜中泣”,这里的能量变化主要是化学能转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g) ![]() 2C(g)+D(g),经2 min后,B的浓度减少了0.6 mol·L-1。对此反应速率的叙述正确的是
2C(g)+D(g),经2 min后,B的浓度减少了0.6 mol·L-1。对此反应速率的叙述正确的是
A.用A表示的反应速率是0.4 mol·L-1·min-1
B.分别用B、C、D表示反应的速率,其比值是3∶2∶1
C.在2 min末时的反应速率,用反应物B来表示是0.3 mol·L-1·min-1
D.在这2 min内用B和C表示的反应速率的值都是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、M、R、W的原子序数依次增大。X原子是周期表中半径最小的原子,Y原子的最外层电子数是其内层电子数的2倍,Z是地壳中含量最高的元素,M+、R2+与Z2-具有相同的电子层结构,W与M组成的化合物是生活中必备的调味品。根据题给信息按要求回答下列问题。
(1)元素Y在元素周期表中的位置为____________________。
(2)M、W各自的最高价氧化物对应水化物相互反应的离子方程式为_____。
(3)为比较M、R的活泼性,将其单质分别投入______(试剂)中,根据反应的剧烈程度,可证明活泼性强的是_______(填元素符号)。
(4)由Y与X组成的质量比为5∶1的有机物的化学式为__________,写出其所有分子的结构简式________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
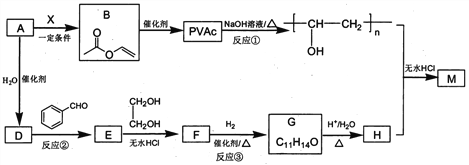
【题目】PVAc是一种具有热塑性的树脂,可合成重要高分子材料M,合成路线如下:
己知:R、Rˊ、Rˊˊ为H原子或烃基
I. R'CHO+ R"CH2CHO![]()
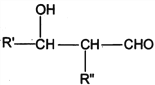
![]()
![]()
II. RCHO+![]()
![]()
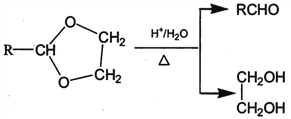
(1)标准状况下,4.48L气态烃A的质量是5.2g,则A的结构简式为___________________。
(2)己知A→B为加成反应,则X的结构简式为_______;B中官能团的名称是_________。
(3)反应①的化学方程式为______________________。
(4)E能使溴的四氯化碳溶液褪色,反应②的反应试剂和条件是_______________________。
(5)反应③的化学方程式为____________________________。
(6)在E→F→G→H的转化过程中,乙二醇的作用是__________________________。
(7)己知M的链节中除苯环外,还含有六元环状结构,则M的结构简式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有浓度均为0.1molL-1的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵。请回答下列问题:
(1)四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)__。
(2)已知T℃,KW=1×10-13,则t℃___25℃(填“>”、“<”或“=”)。在T℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=_。
(3)25℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取aL该盐酸与bL该氢氧化钠溶液反应,恰好完全中和,求:
①若x+y=14,则a/b=__(填数据);
②若x+y>14,则a/b=__(填表达式);
③该盐酸与该氢氧化钠溶液完全中和,两溶液的pH(x、y)的关系式为__(填表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯胺是一种长效缓释有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的4~5倍,下列有关氯胺(NH2Cl)的说法一定不正确的是( )
A.氯胺的水解产物为NH2OH(羟氨)和HCl
B.氯胺的电子式为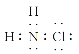
C.氯胺中氯的化合价为+1价
D.氯胺的消毒原理与漂白粉相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是( )

A. 最简单气态氢化物的热稳定性:R>Q B. 最高价氧化物对应水化物的酸性:W<Q
C. 原子半径:T>Q>R D. T的最高价氧化物水化物具有两性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业。
(1)工业上可用氯化钠为原料,通过电解的方法制得NaClO,工业上制取NaClO的离子反应方程式为______________________________电解后的溶液PH____________7(填大于、小于、等于);其原因是_________________________________________(用离子方程式表示)
(2)KAl(SO4)2溶液中质子守恒等式为_______________________________________
(3)某小组同学用下图所示装置探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。
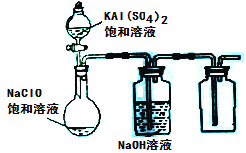
①打开活塞向烧瓶中加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。此时反应的离子方程式为__________________________________。
②将烧瓶中的混合液在阳光照射下,不久烧瓶中有黄绿色气体产生,充分反应后集气瓶中收集到一种无色无味的气体。写出在光照射下混合液中反应的化学方程式是________________________。
(4)若将分液漏斗中的KAl(SO4)2溶液换成硫酸亚铁铵(一种复盐:(NH4)2SO4·FeSO4)溶液,其他不变。打开分液漏斗活塞向烧瓶中滴入足量的硫酸亚铁铵溶液。观察到烧瓶中有红褐色沉淀产生,但是没有观察到黄绿色气体产生。此时烧瓶中发生的氧化还原反应的离子方程式为______________________。
(5)取100mL 0.1mol/L Ba(OH)2溶液,向其中逐滴加入同浓度的KHSO4溶液至Ba2+恰好完全沉淀,此时溶液的PH值为_______________(忽略两溶液混合时的体积变化,混合后溶液的温度为100℃,100℃时Kw=1x10-12)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com