
【题目】镓(Ga)与铝属于同主族元素,金属镓曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备金属镓的流程如下图所示:
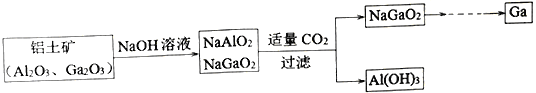
下列判断不合理的是
A. 镓为+3价 B. 碱性:Ga(OH)3>Al(OH)3
C. Ga2O3能与强酸、强碱反应 D. NaGaO2与CO2反应,说明镓的金属性强于铝
科目:高中化学 来源: 题型:
【题目】已知给煤炭加氢可发生反应:C(s)+2H2(g)CH4(g).在VL的容器中投入amol碳(足量),同时通入2amolH2 , 控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示.下列说法正确的是( ) 
A.上述正反应为放热反应
B.在4MPa、1200K时,图中X点v(H2)正>v(H2)逆
C.在5MPa、800K时,该反应的平衡常数为 ![]()
D.工业上维持6MPa1000K而不采用10MPa1000K,主要是因为前者碳的转化率高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:

(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为______.
(2)用电子式表示①与③形成化合物的过程______.:
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是______. ,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:______.
(4)①②③④四种元素的简单离子半径由大到小的顺序是______.(用离子符号和“>”表示)。
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是______.(用化学式和“>”表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋约占地球表面积的71%,具有十分巨大的开发潜力,通过海水的综合利用可获得许多物质供人类使用.
(1)Ⅰ、海水中制得的氯化钠除食用外,还用作工业原料,例如通常以NaCI、CO2和NH3为原料制取纯碱,请写出第一步制取NaHCO3的化学方程式: .
(2)Ⅱ、工业上以浓缩海水为原料提取溴的部分流程如图1:
已知:Br2常温下呈液态,易挥发,有毒:2Br2+3CO32﹣=5Br﹣+BrO3﹣+3CO2 .
①通过步骤①氯气氧化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液,原因是 .
②反应釜2中发生反应的离子方程式为 .
③向蒸馏塔中通入水蒸气加热,控制温度在90℃左右进行蒸馏的原因是 .
(3)Ⅲ、盐卤蒸发冷却后析出卤块的主要成分是MgCI2 , 此外还含有Fe2+、Fe3+、Mn2+等离子.以卤块为原料制得镁的工艺流程如图2(部分操作和条件已略去):
生成氢氧化物沉淀的pH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.1 |
①用NaClO氧化Fe2+得到Fe(OH)3沉淀的离子反应方程式是 .
②步骤③需在HCl保护气中加热进行,请用化学平衡移动原理解释原因 .
③NaClO还能除去盐卤中的CO(NH2)2 , 生成盐和能参与大气循环的物质,除去0.1molCO(NH2)2时消耗NaCIOg.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4mol SO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2+O22SO3测得平衡时混合物总的物质的量为5mol,求:
(1)平衡时各物质的浓度;
(2)平衡时SO2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向2L恒容密闭容器中充入1molCOCl2(g)发生反应:COCl2(g)![]() Cl2(g)+CO(g),反应过程中测得的有关数据如下表:
Cl2(g)+CO(g),反应过程中测得的有关数据如下表:
t/s | 0 | 2 | 4 | 6 | 8 |
N(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列说法不正确的是
A. 使用催化剂能够改变反应速率
B. 达到6s时,反应停止,不再进行
C. 在8s时,反应容器中各物质的浓度不再发生变化
D. 生成Cl2的平均反应速率,0~2s内平均速率比2~4s大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习和研究离不开元素周期表。下表为元素周期表的一部分,表中①-⑩分别代表一种元素。回答下列问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
3 | ⑧ | ⑨ | ⑩ |
(1)上述元素中,有一种元素在自然界中形成的物质种类最多,该元素在周期表中的位置是_______。
(2)⑧、⑨、⑩元素的离子半径由大到小的顺序为________________(用离子符号表示)。
(3)写出由①、⑥、⑧三种元素形成的一种离子化合物的电子式__________________。
(4)上述元素中有一种元素的氧化物和氢氧化物都有两性,面出该元素的原子结构示意图______________;高温条件下,该元素的单质与铁红能发生反应,此反应常用于野外焊接钢轨,则该反应的能量变化可用图__________________表示。(填“甲“或“乙”)
(5)知W+X→Y+Z,且W、X、Y、Z分别是由①、⑤、⑥三种元素中的两种形成的10电子粒子,写出并配平上述反应式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )

A. a和b用导线连接时,铁片上发生的反应为Fe-3e-===Fe3+
B. a和b用导线连接时,铜片上发生的反应为Cu2++2e-===Cu
C. 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D. a和b不连接时,铁片上会有金属铜析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁的主要反应为:CO(g)+ ![]() Fe2O3(s)CO2(g)+
Fe2O3(s)CO2(g)+ ![]() Fe(s) 已知该反应在不同温度下的平衡常数如下:
Fe(s) 已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
下列说法正确的是( )
A.增加Fe2O3固体可以提高CO的转化率
B.该反应的△H<0
C.减小容器体积既能提高反应速率又能提高平衡转化率
D.容器内气体密度恒定时,不能标志反应达到平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com