
【题目】某无色溶液既可能是强酸性又可能是强碱性,在该溶液中一定能大量共存的离子是( )
A.H+ Na+ NO3﹣ SO42﹣
B.Na+ CO32﹣ Cu2+ Cl﹣
C.K+ Na+ Cl﹣ SO42﹣
D.K+ Cl﹣ Ba2+ HCO3﹣
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实骑,能达到实验目的的是
选项 | A | B | C | D |
实验装置 |
|
|
|
|
实验目的 | 完成“喷泉”实验 | 测定中和热 | 制取并收集干燥纯净的NH3 | 制取NO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行两组电解实验。
实验一:已知固体电解质只有特定离子才能移动。按照下图装置研究α-AgI固体电解质导体是Ag+导电还是I-导电;

实验二:用惰性电极电解硫酸铜和盐酸混合液,对产生的气体进行研究。
关于以上实验,下列说法正确的是
A. 实验一:若α-AgI固体是Ag+导电,则通电一段时间后的晶体密度不均匀
B. 实验一:若α-AgI固体是I-导电,则通电一段时间后的晶体密度仍均匀
C. 实验二:若阳极为纯净气体,阴、阳两极产生的气体体积比可能≥1
D. 实验二:若阳极为混合气体,阴、阳两极产生的气体体积比可能≥1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C,D、E、G六种前四周期主族元素,已知A、B、C、D、E五种元素在元素周期表中的位置如图所示。

(1)若非金属元素B的核电荷数为x,则A、B、C、D、E五种元素的核电荷数之和为_________。
(2)若A、B、C、D四种元素的核内质子数之和为56,lmolG的单质与足量盐酸反应,能产生22. 4LH2(在标准状况下);G的阳离子与D的阴离子核外电子层结构相同。
①写出下列元素名称:A_________,B________;
②D的简单离子结构示意图为_________;
③氢化物的沸点:D_________B,简单氢化物水溶液的酸性:B_________C(填“>”“<”或“=”)。
④甲为G、C两元素组成的化合物,用电子式表示甲的形成过程_________。
(3)下列说法正确的是_________(填序号)
A.氢键是极弱的化学键,任何物质中都存在化学键
B.共价化合物中成键原子均满足稀有气体的稳定结构
C.两种非金属元素形成的化合物可能含有离子键
D.化学键断裂,一定发生化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)25℃时,在0.1L 0.2molL﹣1的HA溶液中,有0.001mol的HA电离成离子,则该溶液的pH= .
(2)25℃时,若向0.1mol/L氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol/L,则c(SO42﹣)= .
(3)室温下,若向0.1mol/L氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是 .
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
化学式 | 电离常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×l0﹣7、K2=5.6×10﹣11 |
回答下列问题
25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为 .
向NaCN溶液中通入少量CO2 , 所发生反应的化学方程式为: .
(5)常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是( )
A. 表示1 LpH=2的CH3COOH溶液加水稀释至V L,pH随lgV的变化
表示1 LpH=2的CH3COOH溶液加水稀释至V L,pH随lgV的变化
B. 表示不同温度下水溶液中H+和OH﹣浓度的变化的曲线,图中温度T2<T1
表示不同温度下水溶液中H+和OH﹣浓度的变化的曲线,图中温度T2<T1
C.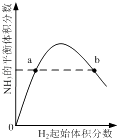 表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率小于b点
表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率小于b点
D. 表示同一温度下,在不同容积的容器中进行反应2NO2(g)2NO(g)+O2(g),O2的平衡浓度与容器容积的关系
表示同一温度下,在不同容积的容器中进行反应2NO2(g)2NO(g)+O2(g),O2的平衡浓度与容器容积的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有以下各组微粒或物质:A.正丁烷和异丁烷 B.金刚石、石墨和C60 C.冰和干冰 D.35Cl和37Cl E.NO和NO2;其中,互为同分异构体的有__________(填编号,以下同);互为同素异形体的有__________。
(2)现有:①干冰 ②金刚石 ③NH4Cl ④Na2S四种物质,按下列要求回答(填序号):熔化时不需要破坏化学键的是____________;既存在离子键又存在共价键的是____________。
(3)向一个容积为2 L的密闭容器中充入7 mol SO2和4 mol O2,在一定温度和压强下,发生如下反应:2SO2(g)+O2(g) 2SO3(g),经4 s后达到平衡状态,测得SO2的物质的量是3 mol,则达到平衡状态时O2的转化率为__________;平衡时SO3的物质的量浓度_______。
(4) NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25 ℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可用于合成除草剂和杀虫剂。一定条件下,恒容密闭容器中,发生反应H2S(g)+CO2(g) ![]() COS(g)+H2O(g),能充分说明该反应已经达到化学平衡状态的是
COS(g)+H2O(g),能充分说明该反应已经达到化学平衡状态的是
A. 正、逆反应速率都等于零
B. H2S、CO2、COS、H2O的浓度相等
C. H2S、 CO2、COS、H2O的浓度不再变化
D. H2S、CO2、COS、H2O在密闭容器中共存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com