
����Ŀ��ij��ѧ��ȤС�����������ʵ�顣
ʵ��һ����֪��������ֻ���ض����Ӳ����ƶ���������ͼװ���о���-AgI�������ʵ�����Ag�����绹��I-���磻

ʵ������ö��Ե缫�������ͭ��������Һ���Բ�������������о���
��������ʵ�飬����˵����ȷ����
A. ʵ��һ������-AgI������Ag+���磬��ͨ��һ��ʱ���ľ����ܶȲ�����
B. ʵ��һ������-AgI������I-���磬��ͨ��һ��ʱ���ľ����ܶ��Ծ���
C. ʵ�����������Ϊ�������壬������������������������ȿ��ܡ�1
D. ʵ�����������Ϊ������壬������������������������ȿ��ܡ�1
���𰸡�D
��������ʵ��һΪ���װ�ã����缫���������������ܽ��Ag+����Ag+���磬Ag+��������������ͨ��һ��ʱ���ľ����ܶȾ��ȣ���A����B������I-���磬����I-������������ͨ��һ��ʱ���ľ���I-���ˣ��ܶȲ����ȣ���B����ʵ����У��ö��Ե缫�������ͭ��������Һ���������Һʱ��������Ӧ�����ǣ�2Cl����2e��=Cl2����4OH����4e��=2H2O+O2����������Ӧ�����ǣ�Cu2++2e��=Cu��2H++2e��=H2�������ݵ�ʧ�����غ��֪��������Ϊ��������Cl2ʱ�������Ͽ��ܲ��������壬Ҳ������H2���ɣ���H2�����ʵ�����С��Cl2�����ʵ�������C��������Ϊ�������Cl2��O2ʱ�������Һ��Cu2+�Ƚ϶࣬���������ܲ��������壬�����Һ��Cu2+�Ƚ��٣���ʱ��H2���ɣ�����������������������ϵ���ܡ�1����D��ȷ����ѡD��


 Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹ����¯���ȣ�����ʹ�������ʾ������ȡ�����һ�¡��ٶȿ졢��Ч�ʸߵ��ŵ㡣�乤��ԭ����ͨ���¯�ڵ������Լ��ں��ȵĸ�Ƶ�ı���糡�ķ���ˮ���������Ѹ�ٰڶ���������ЧӦ��������Ϊ(����)
A. ˮ���Ӿ��м��Թ��ۼ� B. ˮ�����Ǽ��Է���
C. ˮ���⡢����Ԫ����� D. ˮ�������й��õ��Ӷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����״��ij��÷����ǣ�CO(g)+2H2(g)=CH3OH(g) ��H1=-90.8 kJ/mol��
��֪��2H2(g)+O2(g)=2H2O(1) ��H2=-571.6 kJ/mol
H2(g)+![]() O2(g)=H2O(g) ��H3=-241.8 kJ/mol
O2(g)=H2O(g) ��H3=-241.8 kJ/mol
�����й�˵����ȷ����
A. H2��ȼ����Ϊ241. 8 kJ/mol
B. CH3OH(g)+O2(g)=CO(g)+2H2O(g) ��H=-392. 8 kJ/mol
C. ��![]() ���ȱ�ʾ���Ӹ���Ҳ�ܱ�ʾ���ʵ���
���ȱ�ʾ���Ӹ���Ҳ�ܱ�ʾ���ʵ���
D. δע���¶Ⱥ�ѹǿʱ����H��ʾ��״���µ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A�Ľṹ��ʽΪ ![]() ������ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D�������ʣ�
������ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D�������ʣ� 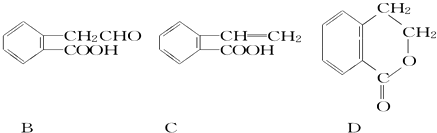
��1��B�к��������ŵ������� ��
��2��A��C�ķ�Ӧ��������A��D�л�Ϊͬ���칹����� ��
��3����A����B�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.���ֽⷴӦһ������������ԭ��Ӧ
B.�û���Ӧһ����������ԭ��Ӧ
C.�е��ʲμӵĻ��Ϸ�Ӧһ����������ԭ��Ӧ
D.û�е������ɵķֽⷴӦһ������������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
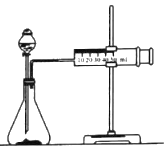
����Ŀ����ѧ��Ӧ������������ѧ��Ӧ���п����̶ȵ���������ijѧ��Ϊ��̽��þ�������ᷴӦ�����з�Ӧ���ʵı仯��������ͼװ�òⶨһ��ʱ���ڷ�Ӧ�ų����������������ϡ��������Ϊ100mL�����Է�Ӧ����Һ����ı仯����ʵ���¼���±����ۼ�ֵ����
ʱ��(min) | l | 2 | 3 | 4 | 5 | 6 |
�������(mL)����״���� | 1 | 50 | 120 | 232 | 288 | 310 |
(1)����ͼ��ʾ��ʵ����Ʒ�⣬����Ҫ��һ��ʵ��������_________��
(2)ʵ��ǰ������װ�������Եķ�����_________��
(3)װ�����������ã�0��lminʱ����������ȴ���ٵ�ԭ����_________��
(4)��Ӧ��������ʱ�����_________min(�0��1��1��2��2��3��3��4����4��5����5��6������ԭ����_________����Ӱ�췴Ӧ�������صĽǶȽ��ͣ���
(5)3��4minʱ��Σ��������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����Ϊ_________������Һ������䣩��
(6)���ڷ�Ӧ̫�죬�����������ʱ���ÿ��ƣ�����������������Һ�зֱ��������������Һ���Լ�����Ӧ���ʣ�����Ϊ�����е���_________������Ӧ��ĸ����
A������ˮ B��KCl��Һ C��KNO3��Һ D��CuSO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����������ʯī������1 L 1 molL��1ʳ��ˮ�У�����˵����ȷ���ǣ������� 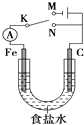
A.�����K��N���ӣ������������ḯʴ
B.�����K��N���ӣ�������Ӧʽ��4OH����4e��=2H2O+O2��
C.�����K��M���ӣ���ʯī������ͭ������ʵ�������϶�ͭ
D.�����K��M���ӣ�������������28 L����״������ʱ��������1 mol NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ�ȿ�����ǿ�����ֿ�����ǿ���ԣ��ڸ���Һ��һ���ܴ�������������ǣ� ��
A.H+ Na+ NO3�� SO42��
B.Na+ CO32�� Cu2+ Cl��
C.K+ Na+ Cl�� SO42��
D.K+ Cl�� Ba2+ HCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ճ������г��������ӵ�ʳ����������������������������Ҷ��������������������Ʒ������ĵ⡢����������Ӧ����Ϊ�� ��
A.Ԫ��B.����C.����D.������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com