
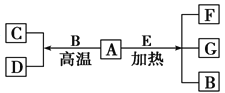
����Ŀ����1����������������뵪ѭ�����ϳɰ���ҵ���Dz�����ֶ�֮һ������Ȼ��Ϊԭ�Ϻϳɰ����µ��������ʵķ�������������ȾС���ɱ��͵�����ŵ�������̴�����ͼ1��ʾ��

����д������Ȼ���Ʊ������Ļ�ѧ����ʽ��_________________________________��
��д���ϳ�����[CO (NH2) 2]��Ӧ�Ļ�ѧ����ʽ��__________________________��
��д��O2��NH3���д�������������Ӧ����NH4NO3��H2O�Ļ�ѧ����ʽ��______��
��ÿ����1molNH4NO3������ҪNH3______mol����Ҫ������ЩNH3��������ҪCH4____mol��
��2����ѧ���ѻ�ü��������о������N4���ӣ���ṹΪ�������壨��ͼ2������֪����1molN-N������193kJ����������1molN��N������941kJ��������1molN4����ת��ΪN2ʱҪ�ͷ�______kJ������
���𰸡� CH4+2H2O![]() CO2+4H2 CO2+2NH3
CO2+4H2 CO2+2NH3![]() CO��NH2��2+H2O 2NH3+2O2
CO��NH2��2+H2O 2NH3+2O2![]() NH4NO3+H2O 2 0.75 724
NH4NO3+H2O 2 0.75 724
����������1����CH4ת��������������CO2��H2������ʽΪ��CH4+2H2O![]() CO2+4H2���ʴ�Ϊ��CH4+2H2O
CO2+4H2���ʴ�Ϊ��CH4+2H2O![]() CO2+4H2��
CO2+4H2��
��������̼�Ͱ�����Ӧ�������أ�����ԭ���غ㣺CO2+2NH3![]() CO��NH2��2+H2O���ʴ�Ϊ��CO2+2NH3
CO��NH2��2+H2O���ʴ�Ϊ��CO2+2NH3![]() CO��NH2��2+H2O��
CO��NH2��2+H2O��
��O2��NH3��Ӧ����NH4NO3������ԭ���غ㷴Ӧ�Ļ�ѧ����ʽΪ2NH3+2O2![]() NH4NO3+H2O���ʴ�Ϊ��2NH3+2O2
NH4NO3+H2O���ʴ�Ϊ��2NH3+2O2![]() NH4NO3+H2O��
NH4NO3+H2O��
��NH4NO3��2NH3��ÿ����1mol NH4NO3������Ҫ2molNH3�����ݷ�ӦCH4+2H2O![]() CO2+4H2��N2+3H2
CO2+4H2��N2+3H2![]() 2NH3����֪����2molNH3��Ҫ����0.75mol���ʴ�Ϊ��2��0.75��
2NH3����֪����2molNH3��Ҫ����0.75mol���ʴ�Ϊ��2��0.75��
��2���ӽṹͼ�пɿ�����һ��N4�����к���6��N-N�������ݷ�Ӧ�ȵ��ڷ�Ӧ����ܼ��ܼ���������ܼ��ܣ���N4��g��=2N2��g����H������H=6��193 kJmol-1-2��941 kJmol-1=-724 kJmol-1���ʴ�Ϊ��724��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ��Һһ�������Ե���
A��c(NH4+)=c(C1-)��NH4Cl ��Һ
B��c(H+)=1��10-7mol��L-1����Һ
C��pH=7����Һ
D�������½�pH=3������pH= 11�ļ�������Ϻ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��G����ѧ��ѧ�������ʣ�A��DΪ���ʣ�G�Ǻ�AԪ�ص��������塣��֪��A(s)+B(g)=C(g)+D(g) ��H= +131.4 kJmol-1��ijͬѧʵ���֪��4 g A����������Ӧ����43.8 kJ��������
��1��д��AԪ�ص�����________��
��2������֪��
A(s)+O2(g)=G(g)��H= ��393.6 kJmol-1
C(g)+ O2(g)=G(g)��H=��283 kJmol-1
D(g)+ O2(g)=B(g)��H=��242 kJmol-1�ɴ��жϡ���Ϊ283 kJmol-1+242 kJmol-1>393.6 kJmol-1������Aȼ��ʱ������B���Էų����������������˵���Ƿ���ȷ��___________��������_____________________��
��3��д��A+O2��C���Ȼ�ѧ����ʽ��__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������̿�(MnO2)��������(FeS2)������������̣�MnSO4��,����һ�������ȡ����������(EMD)�Ĺ�����������:
I.�����̿���������ᰴһ���������뷴Ӧ���У����裬���ȱ��·�Ӧһ��ʱ�䡣
II.��Ӧ���м���MnO2��CaCO3�Լ����ټ���Na2S��Һ��������Һ�е��ؽ�����
III.���ˣ�����Һ�м��뾻������һ���������ٹ��ˣ��õ�����MnSO4��Һ��
IV.������MnSO4��Һ������ۣ�����Ƶ�EMD��
��ش���������:
(1)����I�н��衢���ȵ�Ŀ����________�������������з�Ӧ�����ӷ���ʽ:
![]() FeS2+
FeS2+![]() MnO2+
MnO2+![]() _____=
_____=![]() Mn2++
Mn2++![]() Fe2++ S + SO42-+
Fe2++ S + SO42-+![]() ____
____
(2)����CaCO3������ҺpH����pH=5���Ӷ����������������CaCO3������ԭ��:________����������ӷ���ʽ���ͣ�
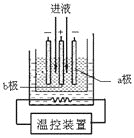
(3)����IV������ͼ��ʾ�ĵ��װ�õ�⾫�Ƶ�MnSO4��Һ������EMD����__��(�a����b��)������EMD�ĵ缫��Ӧʽ��_________��
(4)EMD����������п�̵�صIJ��ϡ���֪����п�̵�صķ�ӦʽΪ:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2��
���й��ڼ���п�̵�ص�˵����ȷ����_______(����ĸ���)��
A.����п�̵���Ƕ��ε��
B.����п�̵�ؽ���ѧ��ת��Ϊ����
C.������ӦΪ:2MnO2+2H2O+2e-=2MnOOH+2OH-
D.����п�̵�ع���ʱ��������MnO2�����·����Zn��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�����ĸ���������ԭ�Ӹ������ɴ�С��˳�����е���
��0.5 mol���� ����״����22.4 L���� ��4 ��ʱ9 mLˮ ��0.2 mol����
A. �٢ܢۢ� B. �ܢۢڢ�
C. �ڢۢܢ� D. �٢ܢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�̬ԭ�ӻ����ӵĵ����Ų�ʽ������ǣ��� ��
A. K��1s22s22p63s23p64s1 B. F-��1s22s22p6
C. 26Fe��1s22s22p63s23p63d54s3 D. Kr��1s22s22p63s23p63d104s24p6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���縺�ԵĴ�СҲ������Ϊ�жϽ����Ժͷǽ�����ǿ���ij߶ȣ����й��ڵ縺�Եı仯������ȷ����
A. ���ڱ���ͬ����Ԫ�ش����ң�Ԫ�صĵ縺��������
B. ���ڱ���ͬ����Ԫ�ش��ϵ��£�Ԫ�صĵ縺��������
C. �縺��Խ������Խǿ
D. �縺��ԽС���ǽ�����Խǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ������������ֶ�����Ԫ�أ���ԭ����K����M���������ȣ���ԭ�ӵĺ������������ԭ�Ӻ����������1����ԭ�ӵ������������Ǵ�����������2������ԭ�Ӻ˵�����ȱ�ԭ�Ӻ˵������2����ش�
��1������________Ԫ�أ���Ԫ�����ƣ�����С����ͬ�����������ڱ��е�λ��Ϊ______________��
��2������________Ԫ�أ�д������ͬ�����������Ԫ�ض�Ӧ��ĵ���ʽ___________________��
��3������________Ԫ�أ�����������Ӧˮ����Ļ�ѧʽ��_________________��
��4������________Ԫ�أ����붡����Ԫ���γɼ������Ӽ����й��ۼ����ʵĻ�ѧʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ԫ�������ڱ��е����λ�����±�����������������Ӧˮ������ǿ��ˮ�ԣ��Ͷ���ͬһ���ڣ���ԭ������������ڲ������ͬ�������������ж���ȷ���ǣ�������
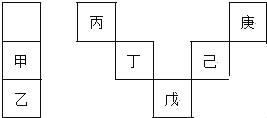
A. �������ԭ���������28
B. ��̬�⻯����ȶ��ԣ�����������
C. �����£��������γɵĻ�����������ˮ
D. ������������ﲻ���κ��ᷴӦ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com