
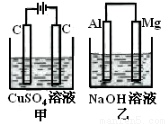
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当电路中通过的电子都是0.1mol时,下列说法正确的是( )
A.相同条件下产生气体的体积:V甲=V乙
B.溶液pH值变化:甲减小乙增大
C.溶液的质量变化:甲减小乙增大
D.电极反应式:甲中阴极:Cu2++2e—= Cu, 乙中负极:Mg - 2e—= Mg2+
C
【解析】
试题分析:甲是电解池,乙是原电池。对于甲,在阳极发生反应4OH—-4e-= O2↑+2H2O当电路中通过的电子是0.1mol时,产生气体0.025mol.对于乙:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,若转移电子0.1mol,则产生气体的物质的量为0.05mol,因此相同条件下产生气体的体积V甲<V乙。错误。B.对于甲,反应的总方程式为:2CuSO4+2H2O 2Cu+ O2↑+2H2SO4,随着电解的进行,溶液的酸性增强,所以溶液pH值减小;对于乙,反应的总方程式是:2Al+2NaOH+2H2O=2NaAlO2+3H2↑随着电解的进行,溶液的碱性减弱,所以溶液pH值减小。错误。C.根据电解的总方程式可知:两个装置中溶液的质量变化:甲减小乙增大。正确。D.电极反应式:甲中阴极:Cu2++2e—= Cu, 乙中负极:2Al - 6e—+8OH-= 2AlO2-++3H2↑+4H2O。错误。
2Cu+ O2↑+2H2SO4,随着电解的进行,溶液的酸性增强,所以溶液pH值减小;对于乙,反应的总方程式是:2Al+2NaOH+2H2O=2NaAlO2+3H2↑随着电解的进行,溶液的碱性减弱,所以溶液pH值减小。错误。C.根据电解的总方程式可知:两个装置中溶液的质量变化:甲减小乙增大。正确。D.电极反应式:甲中阴极:Cu2++2e—= Cu, 乙中负极:2Al - 6e—+8OH-= 2AlO2-++3H2↑+4H2O。错误。
考点:考查原电池、电解池的反应原理及应用的知识。


科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:填空题
(12分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a |
|
| |||||||||||||||
b |
|
|
| c | d | e | f |
| |||||||||
g | h | i | j |
| k | l | m | ||||||||||
n |
|
|
|
|
| o | p |
|
|
|
|
|
|
|
|
|
|
试回答下列问题:
(1)元素p为26号元素,请写出其基态原子外围电子排布式: 。
(2)c与a形成6个原子组成分子结构简式: ,
该分子是: (填“极性”或“非极性”)分子。
(3)表中O、P两元素的部分电离能数据列于下表:
元 素 | O | P | |
电离能 kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态O2+再失去一个电子比气态P2+再失去一个电子难。对此,你的解释是 ;
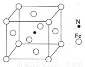
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
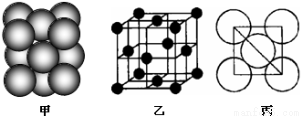
晶胞中i原子的配位数为 ,一个晶胞中i原子的数目为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:选择题
下列过程需要克服分子间作用力的是( )
A.HCl气体溶于水 B.液氯汽化
C.氯化镁受热熔化 D.二氧化硅受热熔化
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三5月校质检理综化学试卷(解析版) 题型:选择题
对于可逆反应mA(g) + nB(g)  pC(g) + qD(g),若其它条件都不变,探究催化剂对反应的影响,可得到如下两种v-t图象。下列判断正确的是( )
pC(g) + qD(g),若其它条件都不变,探究催化剂对反应的影响,可得到如下两种v-t图象。下列判断正确的是( )
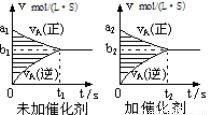
A.b1>b2 ,t1>t2
B.两图中阴影部分面积一定相等
C.A的平衡转化率(II)大于(Ⅰ)中A的转化率
D.若m+n<p+q,则压强变化对正反应速率的影响程度比逆反应速率影响程度大
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省漳州市八校高三第四次联考理综化学试卷(解析版) 题型:简答题
(13分)近现代战争中,制造坦克战车最常用的装甲材料是经过轧制和热处理后的合金钢,热处理后整个装甲结构的化学和机械特性和最大限度的保持一致。钢中合金元素的百分比含量为:铬0.5~1.25 镍0.5~1.5 钼0.3~0.6 锰0.8~1.6 碳0.3
(1)铬元素的基态原子的价电子层排布式是 。
(2)C元素与其同主族下一周期元素组成的晶体中,C原子的杂化方式为 .
(3)Mn和Fe的部分电离能数据如表:
元 素 | Mn | Fe | |
电离能 /kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
根据表数据,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是 。
(4)镍(Ni)可形成多种配合物,且各种配合物有广泛的用途。
某镍配合物结构如右图所示,分子内含有的作用力
有 (填序号)。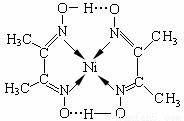
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
组成该配合物分子且同属第二周期元素的电负性由大到小的顺序是 。
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是
(6)铁能与氮形成一种磁性材料,其晶胞结构如右图所示,则该磁性材料的化学式为
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省漳州市八校高三第四次联考理综化学试卷(解析版) 题型:选择题
化学与生产、生活、社会密切相关。下列说法中不正确的是( )
A.“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致。
B.绿色化学的核心是从源头上消除工业生产对环境的污染。
C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈。
D.华商科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的二氧化硅。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
在相同的条件下测得①NaHCO3 ②CH3COONa ③NaClO三种溶液pH相同,则它们的物质的量浓度由大到小的顺序是
A.①>②>③ B.③>②>① C.②>①>③ D.③>①>②
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。据此判断这四种金属活动性由大到小的顺序是
A.①③②④ B.①③④② C.③④②① D.③①②④
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省南平市毕业班质量检查理综化学试卷(解析版) 题型:推断题
(15分)实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
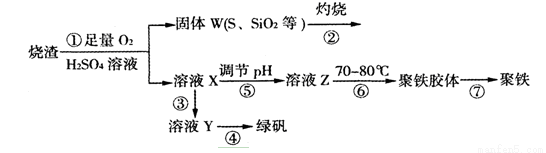
(1)将过程②中的产生的气体通入下列溶液中,溶液会褪色的是 ;
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为: ;
(3)过程③中,需加入的物质是 ;
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有 ;
(5)过程⑤调节pH可选用下列试剂中的 (填选项序号);
A.稀硫酸 B.CaCO3 C.NaOH溶液
(6)过程⑥中,将溶液Z加热到70一80℃,目的是 ;
(7)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2.700g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥,称量,得固体质量为3.495g。若该聚铁主要成分为[(Fe(OH)(SO4)]n,则该聚铁样品中铁元素的质量分数为 。(假设杂质中不含铁元素和硫元素)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com