
【题目】下列实验装置示意图、实验现象及结论均正确的是( )
A | B | C | D | |
实验 |
|
|
|
|
现象 | 产生能使带火星小木条复燃的气体 | 两试管中均颜色变化 | 试管中有淡黄色沉淀产生 | 钠表面有气泡生成 |
结论 | FeCl3是H2O2分解的催化剂 | 单质氧化性:Cl2>Br2>I2 | 非金属性Cl>S | 1 mol乙醇与足量钠反应生成3 mol氢气 |
A.AB.BC.CD.D
【答案】C
【解析】
A.两个试管中反应温度不同,且一个滴加了FeCl3溶液,一个没有滴加FeCl3溶液,有两个变量,因此不能证明FeCl3是H2O2分解的催化剂,A错误;
B.向分别盛有NaBr、KI溶液的试管中滴加氯水,两个试管中均颜色变化,说明二者都发生了化学反应,可证明物质的氧化性:Cl2>Br2;Cl2>I2,但不能比较Br2、I2的氧化性强弱,B错误;
C.KMnO4具有强的氧化性,在室温下能将HCl氧化产生Cl2,在试管中发生置换反应:Cl2+Na2S=2NaCl+S↓,看到试管中有淡黄色沉淀产生,因此可证明元素的非金属性:Cl>S,C正确;
D.将金属Na放入盛有乙醇的试管中,看到金属钠表面有气泡生成,证明乙醇与钠发生反应产生了氢气,但由于乙醇中含有烃基H原子和羟基H原子,因此不能由此证明反应产生氢气的物质的量的关系,D错误;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】无水AlCl3易升华,可用作有机合成的催化剂等.工业上用铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下:

(1)氧化炉中Al2O3、Cl2和C反应的化学方程式______.
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式______.
(3)为了测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,再洗涤、灼烧、冷却、称重、得其质量为0.32g。
①写出上述测定过程中涉及的离子方程式:______、__________。
②AlCl3产品的纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
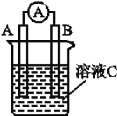
【题目】 (1)如图所示,若溶液C为浓硝酸,电流表指针发生偏转,B电极材料为Fe,A电极材料为Cu,则B电极的电极反应式为_________,A电极的电极反应式为____________;反应进行一段时间后溶液C的酸性会____(填“增强”“减弱”或“基本不变”)。
(2)我国首创以铝—空气—海水电池作为能源的新型海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是______(填化学名称),负极反应为___________;正极反应为_________。
(3)熔融盐电池具有高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,其负极反应式为2CO+2CO32---4e-![]() 4CO2,则正极反应式为_____,电池总反应式为______。
4CO2,则正极反应式为_____,电池总反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4![]() CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4![]() NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气在氧气中燃烧产生淡蓝色火焰。在反应过程中,破坏1 mol氢气中的化学键消耗的能量为Q1kJ,破坏1 mol氧气中的化学键消耗的能量为Q2KJ,形成1 mol水中的化学键释放的能量为Q3kJ。下列关系式中正确的是
A.2Q1+Q2 <2Q3B.Q1+Q2>Q3C.Q1+Q2< Q3D.Q1+Q2> 2Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A的产量是衡量一个国家石油化工生产水平的重要标志,以A为主要原料合成一种具有果香味的物质E的生产流程如下:
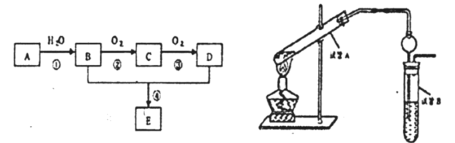
(1)有机物C的名称是_______________
(2)写出B→C的化学方程式________________
(3)请写出B+D→E的化学方程式________________
(4)试管A中加少许碎瓷片的目的是_______________
(5)试管B中试剂的作用是____________________
(6)右边试管接有一个球状物代替了长导管,其作用为______________
(7)从制备乙酸乙酯所得的混合物中分离提纯乙酸乙酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是_____________(填字母)

(8)酯化反应是一一可逆反应, 为提高乙醇的利用率,可采取的措施是_______________。(任写一种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中对应关系正确的是
A | CH3CH3+Cl2 | 均为取代反应 |
B | 由油脂得到甘油 | 均发生了水解反应 |
C | Cl2+2Br=2Cl+Br2 | 均为单质被还原的置换反应 |
D | 2Na2O2+2H2O+4NaOH+O2↑ | 均为水作还原剂的氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某学生用0.1 mol·L-1H2SO4溶液滴定0.1 mol·L-1NaOH溶液,中和后加水至100 mL。若滴定终点的判定有误差:①少滴了一滴H2SO4溶液;②多滴了一滴H2SO4溶液(1滴为0.05 mL),则①和②两种情况下所得溶液的pH之差是( )
A. 4B. 4.6C. 5.4D. 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对一些实验事实的理论解释正确的是( )
选项 | 实验事实 | 理论解释 |
A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
B | SO2为V形分子 | SO2分子中S原子采用sp3杂化 |
C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com