
【题目】NA代表阿伏加德罗常数,下列叙述正确的是
A. 0.1 mol丙烯酸中含有双键的数目为0.1NA
B. 常温常压下,Cu-Zn原电池中,正极产生1.12 L H2时,转移的电子数应为0.1NA
C. 一定条件下定容容器中充入3molH2(g)和1 mol N2(g)发生反应:H2(g)+ N2(g)![]() 2NH3(g);△H= -QkJ/mol,当该反应放出0.25QkJ的热量时,容器中的氢分子数共有2.25 NA
2NH3(g);△H= -QkJ/mol,当该反应放出0.25QkJ的热量时,容器中的氢分子数共有2.25 NA
D. 在50 g质量分数为46%的乙醇水溶液中,含有的氢原子总数为3NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下表列出了除去物质中所含杂质的方法,其中错误的是( )
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A | CO | CO2 | 通过足量的NaOH溶液,干燥 |
B | NaCl | 泥沙 | 溶解、过滤、蒸发结晶 |
C | NaOH溶液 | Na2CO3 | 加入稀盐酸至不再产生气泡 |
D | Cu(NO3)2 | AgNO3 | 加入过量的铜粉,过滤 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于电解NaCl水溶液,下列叙述正确的是 ( )
A. 电解时在阳极得到氯气,在阴极得到金属钠
B. 若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
C. 若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
D. 电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度和压强下,30 L某种气态纯净物中含有6.02×1023 个分子,这些分子由1.204 ×1024个原子构成,下列有关说法中不正确的是( )
A. 该温度和压强可能是标准状况
B. 标准状况下该纯净物若为气态,其体积是 22.4 L
C. 该气体分子为双原子分子
D. 若在该条件下O2为气态,则此时1 mol O2的体积为30 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种重要的工业盐,也常用于鱼类、肉类等食品的染色和防腐。易溶于水,微溶于乙醇。某化学兴趣小组对亚硝酸钠进行多角度探究:
I.亚硝酸钠的制备

(1)实验中用恒压滴液漏斗,相比于普通分液漏斗,其显著优点是___________。
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的化学反应方程式__________________。
Ⅱ.探究亚硝酸钠与硫酸反应气体产物的成分
已知:①NO+NO2+2OH-=2NO2-+2H2O ②气体液化的温度:NO2 为21℃、NO为 -152℃

(3)反应前应打开弹簧夹,先通入一段时间的氮气,目的是___________________。
(4)为了检验装置A中生成的气体产物,仪器的连接顺序为(按左→右连接)为A、C、_______、_______、_______。
(5)在关闭弹簧夹,打开分液漏斗活塞,滴入70%的硫酸后, A中产生红棕色气体。
①确认A中产生气体含有NO,依据的现象是____________________________。
②装置E的作用是__________________________________________________。
(6)如果没有装置C,对实验结论造成的影响是________________________。
(7)通过上述实验探究过程,可得出装置A中反应的离子方程式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数的值。下列说法正确的是( )
A. 标准状况下,22.4 L NO与11.2 L O2混合后气体的体积约为22.4 L
B. 1 L 0.2 mol·L-1 Al2(SO4)3溶液中的离子总数为NA
C. 标准状况下,22.4 L H2O所含原子个数大于3NA
D. 含4 mol HCl的浓盐酸跟足量MnO2加热反应,可制得Cl2的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四支试管中分別盛有固体NaBr、NaCl、Na2SO3、Cu,分别向这四支试管中加入适量浓硫酸,部分现象如图所示:
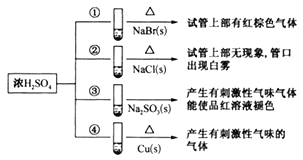
下列判断正确的是( )
A. 反应①和②的现象说明还原性:Br->Cl-
B. 浓硫酸与NaCl不反应,白雾是浓硫酸吸水所致
C. 反应③现象说明氧化性:浓硫酸>Na2SO3
D. 反应④的现象除产生刺激性气味的气体外,溶液中还析出蓝色晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com