
| A. | 5mol,10mol | B. | 6mol,2mol | C. | 8mol,4mol | D. | 8mol,2mol |
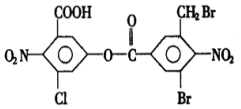
分析 由结构可知,分子中含-COOH、-COOC-、-Cl、-Br均与NaOH反应,且水解生成的酚-OH与NaOH反应,生成的有机物中共有2个-COONa,可与氢氧化钠反应生成碳酸钠,以此来解答.
解答 解:由结构可知,分子中含-COOH、-COOC-、-Cl、-Br均与NaOH反应,且水解生成的酚-OH与NaOH反应,
则1mol该化合物中-COOH、-COOC-、-Cl、-Br消耗NaOH为5mol,水解生成的3mol酚-OH又消耗NaOH3mol,则充分反应后最多可消耗氢氧化钠的物质的量为8mol,生成的有机物中共有2个-COONa,由题给信息可知,液蒸干得到的固体产物再与足量的干燥碱石灰共热,又消耗氢氧化钠的物质的量为2mol.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质及应用,题目难度不大.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Fe做还原剂 | B. | FeO做氧化剂 | ||
| C. | 铁元素的化合价降低 | D. | 铁元素化合剂升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 无机化合物可根据其组成和性质进行分类,
无机化合物可根据其组成和性质进行分类,| 物质类别 | 酸 | 碱 | 盐 | 酸性 氧化物 | 碱性 氧化物 |
| 化学式 | ①H2SO4、H2SO3、HNO3、H2CO3 ②H2S | ③NaOH、KOH、NH3.H2O ④Ba(OH)2 | ⑤Na2CO3 ⑥Na2SO3、NaNO3、K2SO4、K2CO3、KNO3 | ⑦SO2 ⑧-- | ⑨-- ⑩-- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
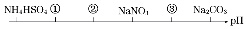 相同温度,相同浓度下的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分別为( )
相同温度,相同浓度下的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分別为( )| A. | NH4Cl、(NH4)2SO4、CH3COONa | B. | (NH4)2SO4、NH4Cl、CH3COONa | ||
| C. | (NH4)2SO4、NH4Cl、NaOH | D. | CH3COONa、NH4Cl、(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

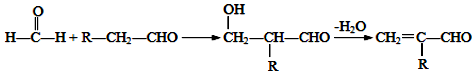
 .
.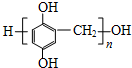 (写出一种即可).
(写出一种即可).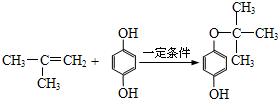 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它可能能使酸性高锰酸钾溶液褪色 | |
| B. | 一氯代物可能只有一种 | |
| C. | 分子结构中甲基的数目可能是0、1、2 | |
| D. | 等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 溶液的pH=9时,溶液中存在下列关系:c(HCO3-)>c(NH4+)>c(NH3•H2O)>c(CO32-) | |
| B. | NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3•H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| C. | 由图可知,往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 | |
| D. | 通过分析可知常温下Ka1(H2CO3)>Kb(NH3•H2O)>Ka2(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
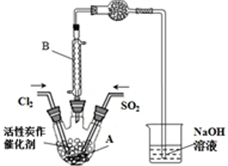 已知:SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H=-a kJ•mol-1
已知:SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H=-a kJ•mol-1| SO2Cl2 | Cl2 | SO2 | |
| 熔点/℃ | -54.1 | -101 | -72.4 |
| 沸点/℃ | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生剧烈水解 | / | / |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com