
| A. | 它可能能使酸性高锰酸钾溶液褪色 | |
| B. | 一氯代物可能只有一种 | |
| C. | 分子结构中甲基的数目可能是0、1、2 | |
| D. | 等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8 |
分析 A.某有机物分子式为C4H8,H原子是C原子2倍,则该有机物可能是单烯烃或环丁烷;
B.如果是环丁烷,只有一种氢原子,氢原子种类决定其一氯代物种类;
C.该物质可能是环丁烷、1-甲基环丙烷、1-丁烯或2-丁烯;
D.设烃的化学式为CxHy,等质量的烃耗氧量=$\frac{m}{12x+y}×$(x+$\frac{y}{4}$)=$\frac{m}{4}×(1-\frac{8}{12+\frac{y}{x}})$.
解答 解:A.某有机物分子式为C4H8,H原子是C原子2倍,则该有机物可能是单烯烃或环丁烷,如果是烯烃,则与乙烯是同系物,能使酸性高锰酸钾溶液褪色,故A正确;
B.如果是环丁烷,只有一种氢原子,氢原子种类决定其一氯代物种类,所以如果是环丁烷,其一氯代物只有一种,故B正确;
C.该物质可能是环丁烷(无甲基)、1-甲基环丙烷(一个甲基)、1-丁烯(一个甲基)或2-丁烯(2个甲基),所以分子结构中甲基的数目可能是0、1、2,故C正确;
D.设烃的化学式为CxHy,等质量的烃耗氧量=$\frac{m}{12x+y}×$(x+$\frac{y}{4}$)=$\frac{m}{4}×(1-\frac{8}{12+\frac{y}{x}})$,根据式子知,如果$\frac{y}{x}$越大相同质量时耗氧量就越多,所以等质量的CH4和C4H8,分别在氧气中完全燃烧,CH4的耗氧量大于C4H8,故D错误;
故选D.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生发散思维能力及分析判断能力,注意:单烯烃和环烷烃通式相同,易错选项是D,要结合数学运算来分析解答,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO→Cu(OH)2 | B. | CaCO3→CaCl2 | C. | Na2SO4→NaCl | D. | Mg(NO3)2→KNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
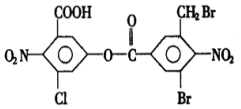
| A. | 5mol,10mol | B. | 6mol,2mol | C. | 8mol,4mol | D. | 8mol,2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳在高温下和二氧化碳的反应 | B. | 碳不完全燃烧 | ||
| C. | 氯化铵与氢氧化钡晶体的反应 | D. | 铝和氧化铁在高温下的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、Cl-、SO42- | B. | Cu2+、Cl-、NO3-、OH- | ||
| C. | Ca2+、Na+、CO32-、NO3- | D. | K+、Fe3+、NO3-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在放电时,正极发生的反应是Pb+SO42-═PbSO4+2e- | |
| B. | 在放电时,该电池的负极材料是铅板 | |
| C. | 在充电时,电池中硫酸的浓度不断变小 | |
| D. | 在充电时,阳极发生的反应是PbSO4+2e-═Pb+SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com