
下列各组物质:① O2和O3; ② 12C和14C;③ CH3CH2CH2CH3和(CH3)2CHCH3;④乙烷和丁烷;⑤ CH3CH2CH2CH(C2H5)CH3和 CH3CH2CH2CH(CH3)C2H5。
互为同系物的是 ,互为同分异构体的是 ,互为同位素的是 ,互为同素异形体的是 ,是同一物质的是 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
Fe(OH)3胶体在生活中有重要应用,利用FeCl3和沸水反应制备的Fe(OH)3胶体中常混有FeCl3和HCl。已知胶体不能透过半透膜,而小分子和离子可以透过半透膜。试回答下列有关问题:
(1)实验室制取Fe(OH)3胶体的方法是________,用________方法除去胶体中的浑浊物;根据________现象证明胶体已经制成。
(2)检验溶液中存在Fe3+和H+的方法是__________________________________________
(3)除去胶体中混有的FeCl3和HCl的方法是:_________________________________。
(4)如何用实验的方法证明胶体和Cl-已经分离?___________________________。
(5)鉴别Fe(OH)3胶体和FeCl3溶液最简单的方法是_________________________________。
(6)高铁酸钠(Na2FeO4)的氧化性比KMnO4更强,它是一种备受关注的新型净水剂,请指出Na2FeO4净水的原理,并说明该净水剂有何优越性_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铁和铝是两种重要的金属,它们的单质及其化合物有着各自的性质。
(1)现配制100mL 0.01mol?L-1 FeCl3溶液,配制过程中需要的玻璃仪器除量筒、胶头滴管、烧杯外,还需要 ,配制过程中除需用FeCl3固体、蒸馏水外,还需要的试剂有 。将已配制好的溶液滴入沸水中并煮沸一段时间,可得到红褐色液体,该反应的离子方程式为 ,此液体具有的性质是 (填字母)。
a.光束通过该液体时形成光亮的“通路”
b.向该液体中加入AgNO3溶液,无沉淀产生
c.将该液体进行过滤,可得到红褐色固体
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(2)在隔绝空气的条件下,用镁条引燃Fe3O4粉末和铝粉的均匀混合物,使其充分反应。
①向充分反应后的剩余固体中加入足量的NaOH溶液,有大量气泡产生,所得剩余固体中除铁外还含有的固体物质是 (填化学式)。
②已知:3Fe(s)+2O2(g)=Fe3O4(s) △H=?1118 kJ·mol-1
2Al(s)+3/2O2(g)=Al2O3(s) △H=?1675.7 kJ·mol-1
则铝与Fe3O4发生反应生成铁和Al2O3的热化学方程式为
。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有下列十种物质:①H2 ②铝 ③CaO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 | | | | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
(1)从三种不同分类标准回答,“铜绿”属于哪类物质?___________________________。
(2)请写出②处的离子方程式。______________________________________________________________,
(3)上述转化过程中属于氧化还原反应的是_________(填序号,下同),属于复分解反应的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(11分)Ⅰ.分类法是化学学习的一种十分有效的方法,它可以使我们从不同角度对同一知识做更加深入的了解,人们根据不同的标准,即使同一物质也可能被划在不同的类别中。现有如下物质①MgCl2②HCl ③SO2 ④ NO2 ⑤K2CO3 ⑥ Cl2 ⑦CaO ⑧ NaOH
请根据下列标准,对上述物质进行分类:
(1)既含离子键又含共价键的物质是 (填代号,下同)。
(2)只含共价键且为非电解质的是 。
(3)含有共价键的化合物是 。
Ⅱ.向某恒容的密闭容器中加入A、B、C三种气体,如图所示是一定条件下三种气体的物质的量随时间的变化情况。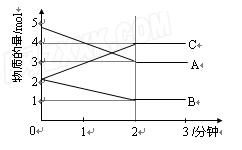
(1)写出该密闭容器发生反应的化学方程式为 。
(2)2分钟后A、B、C各物质的量不再随时间的
变化而变化,其原因是____ 。
(3)下列情况能说明该反应达到化学反应限度的是 。
A.该容器的压强不再发生变化;
B.单位时间内生成A的物质的量与生成C的物质的量相同;
C.该容器中气体的密度不再改变;
D.容器中A的物质的量与C的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式或化学方程式书写正确的是 ( )
A.实验室用氯化铵与消石灰制氨气 NH4++OH- NH3↑+H2O NH3↑+H2O |
| B.将CO2通入BaCl2溶液中 H2O +CO2+Ba2+ =BaCO3↓+2H+ |
| C.少量SO2通入加漂白粉的水溶液中 SO2+H2O+Ca2++3ClO- = CaSO4↓+2HClO+Cl- |
D.用H2还原MgO H2+MgO  Mg+H2O Mg+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.能使淀粉-KI试纸显蓝色的溶液中:K+、SO42-、S2-、SO32- |
| B.含有0.1mol·L-1Fe2+的溶液:Na+、ClO-、SO42-、Cl- |
| C.c(H+)/c(OH-)=1012的溶液中:Al3+、NH4+、NO3-、K+ |
| D.含有0.1mol·L-1HCO3-的溶液:Na+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③同位素:1H、2H、3H;干冰、液氯都是非电解质
④电解质:明矾、冰醋酸、纯碱; 同素异形体:C60、金刚石、石墨
⑤根据分散系的稳定性大小将混合物分为胶体、溶液和浊液
| A.只有②④ | B.只有②③⑤ | C.只有①②④ | D.只有②③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com