

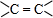 ;葡萄糖分子中官能团有羟基、醛基,相应的电子式为
;葡萄糖分子中官能团有羟基、醛基,相应的电子式为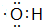 、
、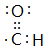 ,故答案为:
,故答案为: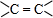 ;
;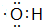 、
、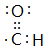 ;
;| H+ |
| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| △ |
 +(2n-1)H2O,
+(2n-1)H2O,| H+ |
| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| △ |
 +(2n-1)H2O.
+(2n-1)H2O.


科目:高中化学 来源: 题型:
| ||
| ||
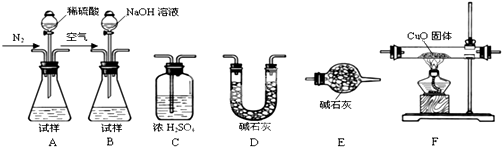

查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如表所示.下列说法不正确的是
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如表所示.下列说法不正确的是| A、元素X与元素Z的最高正化合价之和的数值等于8 |
| B、离子Y2-和Z3+的核外电子数和电子层数均相同 |
| C、元素W的最高价氧化物对应的水化物的酸性比Q的弱 |
| D、元素X的气态氢化物的稳定性大于元素Y的气态氢化物的稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
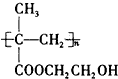 制成超薄镜片,其合成路线可以是:
制成超薄镜片,其合成路线可以是:
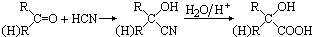
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na和O2 |
| B、Ca(OH)2溶液和CO2 |
| C、Zn和稀硫酸 |
| D、AlCl3和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | A | B | C | D |
| 强电解质 | KNO3 | H2SO4 | BaSO4 | HNO3 |
| 弱电解质 | HF | CaCO3 | HClO | NH3 |
| 非电解质 | SO2 | CS2 | H2O | C2H5OH |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.14g | B、1.6g |
| C、2.82g | D、4.36g |
查看答案和解析>>
科目:高中化学 来源: 题型:
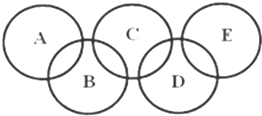 如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为
如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为 ,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:
,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com