
【题目】下列关于各图的说法,正确的是( ) 
A.①中阴极处能产生使湿润淀粉KI试纸变蓝的气体
B.②中待镀铁制品应与电源正极相连
C.③中钢闸门应与外接电源的正极相连
D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】糖类的组成、结构和用途,下列关于糖类的说法正确的是( )
A.糖类物质的组成都符合Cm(H2O)n
B.单糖就是分子组成简单的糖
C.含有醛基的糖就是还原性糖
D.淀粉、纤维素都是多糖,其分子式相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氮肥样品可能含有NH4HCO3,NH4Cl、NH4NO3中的一种或几种,称取该样品1.000克,溶于水配成100mL溶液、将溶液分成两等份依次完成如下实验:
①向一份溶液中加入10mL 0.2mol/L的盐酸与之充分反应,可收集到标准状况下的CO2气体44.8mL(设产生的CO2全部逸出)。
②向另一份溶液中加入足量的6mol/L氢氧化钠溶液,加热,产生的气体(设产生的NH3全部逸出)至少需要25mL 0.15mol/L的硫酸才能被完全反应。下列说法正确的是
A. 1.000g样品中一定含有NH4HCO3 0.316克
B. 向①反应所得的溶液中加入硝酸酸化的硝酸银溶液,若有白色沉淀生成,说明原样品中一定含有NH4C1
C. 原样品的含氮量为21%
D. 无需另外再设计实验验证,就能确定原样品中是否含有NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在自来水消毒和工业上砂糖、油脂的漂白与杀菌过程中,亚氯酸钠(NaClO2)发挥着重要的作用.下图是生产亚氯酸钠的工艺流程图: 
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO23H2O;
②常温下,Ksp(FeS)=6.3×10﹣18;Ksp(CuS)=6.3×10﹣36;Ksp(PbS)=8×10﹣28
③Ⅲ装置中电解硫酸钠溶液,阳极区生成氧气同时产生硫酸,阴极区生成氢气同时产生氢氧化钠.
(1)I中发生反应的离子方程式为 .
(2)从滤液中得到NaClO23H2O晶体的所需操作依次是(填写序号).
a.蒸馏 b.蒸发浓缩 c.过滤 d.冷却结晶 e.灼烧
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2 . 表是25℃时HClO2及几种常见弱酸的电离平衡常数:
弱酸 | HClO2 | HF | H2CO3 | H2S |
Ka/molL﹣1 | 1×10﹣2 | 6.3×10﹣4 | K1=4.30×10﹣7 | K1=9.1×10﹣8 |
①常温下,物质的量浓度相等的NaClO2、NaF、NaHCO3、Na2S四种溶液的pH由大到小的顺序为(用化学式表示);
②Na2S是常用的沉淀剂.某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是;常温下,当最后一种离子沉淀完全时(该离子浓度为10﹣5molL﹣1)此时体系中的S2﹣的浓度为 .
(4)Ⅲ装置中若生成气体a的体积为1.12L(标准状况),则转移电子的物质的量为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L(标况)CO2和3.6g水蒸气,对于组成判断正确的是( )
A.一定有甲烷
B.一定有乙烯
C.一定有乙炔
D.一定有乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A.1 mol乙醇燃烧生成3 mol水
B.1 mol乙醇可以生成1 mol乙醛
C.1 mol乙醇跟足量的金属钠作用得0.5 mol氢气
D.乙醇的分子式为C2H6O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式是: 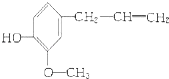 该物质不应有的化学性质是( ) ①可以燃烧
该物质不应有的化学性质是( ) ①可以燃烧
②可以跟溴加成
③可以将KMnO4酸性溶液还原
④可以跟NaHCO3溶液反应
⑤可以跟NaOH溶液反应
⑥可以发生消去反应.
A.①③
B.③⑥
C.④⑥
D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写及解释均正确的是
A. 0.1mol/L 的 Na2S溶液中 c(S2-)<0.1mol/L 的原因:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
B. 实验室制备氢氧化铁胶体:Fe3++3H2O![]() Fe(OH)3+3H+
Fe(OH)3+3H+
C. 水中加入NaOH:H2O+H2O![]() H3O++OH-加入NaOH,消耗溶液中的H3O+平衡右移
H3O++OH-加入NaOH,消耗溶液中的H3O+平衡右移
D. 在碳酸钠溶液中通入CO2气体,CO32-+H2O![]() HCO3-+OH-,CO2 消耗OH- 促使平衡正向移动
HCO3-+OH-,CO2 消耗OH- 促使平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于相同质量的SO2和SO3 , 下列说法:①硫元素的质量比为5:4 ②分子数之比为5:4③原子总数之比为15:16④同温同压下的两种气体体积之比为5:4.其中正确的是( )
A.①②③④
B.①②④
C.只有③
D.其它组合
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com