
【题目】钼及其合金在冶金、环保和航天等方面有着广泛的应用。
(1)Mo可被发烟硝酸及氢氟酸氧化为MoO2F2和MoOF4(少量),硝酸本身被还原为NO2,则该反应中氧化剂与还原剂的物质的量之比为_________。
(2)已知:2Mo(s)+3O2(g)=2MoO3(s) △H1;
2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g) △H2;
MoS2(s)+2 O2(g)=Mo(s)+2SO2(g) △H3
则△H3=_________(用含△H1、△H2的代数式表示)
(3)电氧化法提纯钼的原理:将辉钼矿(MoS2)放入装有食盐水的电解槽中,用惰性电极电解,MoS2被氧化为MoO42-和SO42-
①辉钼矿应放入电解槽的_________(填“阴极区”或“阳极区”)。
②阴极的电极反应式为___________________________。
(4)碳酸钠作固硫剂并用氢还原辉钼矿的原理为MoS2(s)+4H2(g)+2Na2CO3(s) ![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
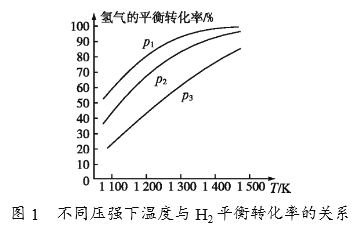
①由图1可知,该反应△H______(填“>”或“<”)0,p1、p2、p3由大到小的顺序为_______________________。
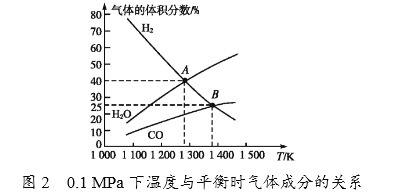
②由图2可知,A点时H2的平衡转化率为____________。
③B点对应的平衡常数K=__________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(MPa)2。
【答案】6:1 ![]() (△H2-△H1) 阳极区 2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-) > p3>p2>p1 50% 0.01
(△H2-△H1) 阳极区 2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-) > p3>p2>p1 50% 0.01
【解析】
(1)在反应中N的化合价从+5→+4降低1价,Mo从0→+6升高6价,根据氧化还原反应中化合价升降总数相等,必有6个硝酸中N降低6×1=6价,同时有1个Mo升高1×6=6价,即6个硝酸和1个Mo同时反应,即氧化剂有6摩尔硝酸反应时,就有1摩尔还原剂钼反应,因此氧化剂与还原剂的物质的量之比为6:1,故答案为6:1;
(2)根据盖斯定律2Mo(s)+3O2(g)=2MoO3(s)①;2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g)②;MoS2(s)+2 O2(g)=Mo(s)+2SO2(g)③,(②式-①式)÷2=③式,所以△H3=![]() (△H2-△H1),故答案为
(△H2-△H1),故答案为![]() (△H2-△H1);
(△H2-△H1);
(3)将辉钼矿(MoS2)放入装有食盐水的电解槽中,用惰性电极电解,MoS2被氧化为MoO42-和SO42-,所以辉钼矿应放入电解槽的阳极,故答案为阳极区;阴极区放电的阳离子为钠离子和氢离子,放电顺序氢离子在钠离子之前,阴极氢离子放电的电极反应为2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-),故答案为2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-);
(4)①由图1相同压强下,温度升高,氢气转化率增大,则平衡正向移动,又因为温度升高平衡向吸热反应方向移动,所以该反应正向吸热,△H>0,故答案为>;根据反应方程式MoS2(s)+4H2(g)+2Na2CO3(s) ![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)可知该反应正向为气体体积增大的方向,在相同温度下,压强越大氢气的转化率越小,由图1可知:在相同温度下p1下氢气的转化率最大,所以p1压强最小,p3下氢气的转化率最小,所以p3压强最大,所以p3>p2>p1,故答案为p3>p2>p1
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)可知该反应正向为气体体积增大的方向,在相同温度下,压强越大氢气的转化率越小,由图1可知:在相同温度下p1下氢气的转化率最大,所以p1压强最小,p3下氢气的转化率最小,所以p3压强最大,所以p3>p2>p1,故答案为p3>p2>p1
②由MoS2(s)+4H2(g)+2Na2CO3(s) ![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),设A混合气体的总物质的量为1mol,则A点时H2的物质的量为0.4mol,H2O的物质的量为0.4mol,则变化的H2的物质的量为0.4mol,A点时H2的为平衡转化率为α(H2)=
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),设A混合气体的总物质的量为1mol,则A点时H2的物质的量为0.4mol,H2O的物质的量为0.4mol,则变化的H2的物质的量为0.4mol,A点时H2的为平衡转化率为α(H2)=![]() =50%,故答案为50%
=50%,故答案为50%
③B点时H2、CO的体积分数均为25%,混合气体为H2、CO、H2O,则H2O的体积分数为1-25%-25%=50%,B点对应的平衡常数K=![]() =0.01,故答案为0.01
=0.01,故答案为0.01


科目:高中化学 来源: 题型:
【题目】杂志Joule中题为“Li—CO2 Electrochemistry:A New Strategy for CO2 Fixation and Energy Storage”的文章,阐述关于电化学技术固定CO2新的反应途径。下图是采用新能源储能器件将CO2转化为固体产物,实现CO2的固定和储能灵活应用的装置。储能器件使用的Li—CO2电池组成为钌电极/CO2—饱和LiClO4—DMSO电解液/锂片。下列说法错误的是
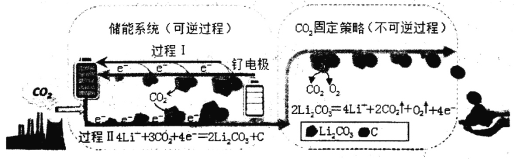
A.钌电极为负极,其电极反应式为:2Li2CO3+C—4e-=== 3CO2+4Li+
B.Li—CO2电池电解液由LiClO4—DMSO溶于水得到
C.这种电化学转化方式不仅减少CO2的排放,还可将CO2作为可再生能源载体
D.CO2的固定中,每生成1.5mol气体,可转移2mole-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象和解释或结论都一定正确的是( )
选项 | 实验操作 | 实验现象 | 解释或结论 |
A | 某钾盐溶于盐酸后,产生无色无味气体,将其通入澄清石灰水 | 有白色沉淀出现 | 该钾盐是 |
B | 将少量的溴水分别滴入 | 下层分别呈无色和紫红色 | 还原性: |
C | 将充满 | 红棕色变深 | 反应 |
D | 将 | 溶液变浑浊,继续通入该气体,浑浊消失 | 该溶液是 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是一种绿色能源。如图所示,某同学设计一个甲醇燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.

根据要求回答相关问题:
(1)写出负极的电极反应式__________________________________.
(2)铁电极为______(填“阳极”或“阴极” ),石墨电极(C)的电极反应式为______________.
(3)若在标准状况下,有2.24L氧气参加反应,丙装置中阴极析出铜的质量为______g。假设乙装置中溶液足量,若在标准状况下有448mL氧气参加反应,则乙装置中阳离子交换膜左侧溶液质量将增加_______g.
(4)若将乙装置中两电极位置互换,其他装置不变,此时乙装置中发生的总反应式________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种有机物中:A.CH4;B.CH2=CH2;C.CH3CH2OH;D.CH3COOH;E.淀粉。
(1)C分子中含有的官能团的名称是_____;
(2)A分子的结构式是_____;
(3)水溶液显酸性的是_____(填编号);
(4)可用于合成聚乙烯塑料的是_____(填编号),化学反应方程式为_____________________ ;
(5)通常用于检验碘单质的是_____(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是( )
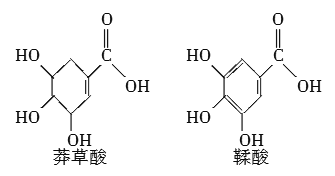
A.两种酸都能与溴水发生加成反应
B.两种酸与三氯化铁溶液都能发生显色反应
C.鞣酸分子与莽草酸分子相比多了两个碳碳双键
D.等物质的量的两种酸与足量的金属钠反应产生氢气的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(g)+nB(g)=eC(g)+fD(s) △H。若按反应物的化学计量数比投料,在一定条件下进行反应,该反应达到平衡时C的气体体积分数与温度、压强的关系如图所示。下列叙述正确的是
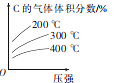
A.该反应的△H >0
B.该化学方程式中m+n>e+f
C.加入催化剂可加快正反应速率,逆反应速率不变
D.往平衡后的恒压容器中再充入一定量C,达到新平衡时,C的浓度与原平衡时的相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期W、X、Y、Z、Q五种元素的原子序数依次递增,W和Z位于同一主族。已知W的氢化物可与Q单质在光照条件下反应生成多种化合物,且Y、Q形成一种共价化合物,X的最高价氧化物对应的水化物可与Y单质反应产生常见的还原性气体单质E。下列说法正确的是
A.X、Y、Q对应简单离子的半径逐渐减小
B.工业上可用电解X、Q元素组成的化合物的饱和溶液制备Q单质
C.Y、Q形成的化合物是非电解质
D.工业用W与Z的最高价氧化物反应制取Z单质,同时得到W的最高价氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化铬的化学式为 CrO5,从其结构发现含有 2 个过氧键,结构如图, 下列说法不正确的是

A.CrO5可能具有强氧化性
B.CrO5 溶于水可能放出氧气
C.CrO5 稳定性较低,易分解
D.CrO5 中 Cr 的化合价为+10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com