
| A.2H2+O2=2H2OΔH=-142.9 kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1 |
| C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1 |
科目:高中化学 来源:不详 题型:单选题
 。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是| A.a=b |
| B.混合溶液的pH=7 |
C.混合溶液中, |
D.混合溶液中, |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.鼓励汽车、家电“以旧换新”,可提高能源利用效率,与环境保护基本无关系 |
| B.农村大力发展沼气,将废弃的秸秆转化为清洁高效的能源 |
| C.镁铝合金可用作制造飞机的材料 |
| D.氢氧燃料电池要广泛地应用于实际生产、生活中,高容量储氢材料的研制是需解决 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
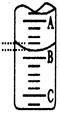
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合前CH3COONa溶液中由水电离出来的c(OH—)>1×10-7 mol·L-1 |
| B.混合前NaCl溶液中:c(Na+) + c(OH—)= c(Cl-)+c(H+) |
| C.混合溶液中 :c(Cl-) >c(CH3COOH) >c(OH—) |
| D.混合溶液中:c(Cl-) + c(CH3COO-) =0.1mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=9 | B.c(OH-)≈10-5 mol·L-1 |
| C.pH≈7 | D.c(OH-)<10-7 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-488.3 kJ/mol | B.+488.3 kJ/mol |
| C.-191 kJ/mol | D.+191 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 CH3OCH3(g) + 3H2O(g)
CH3OCH3(g) + 3H2O(g)| 投料比[n(H2) / n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com