
| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |


科目:高中化学 来源:不详 题型:填空题
| A.100mL蒸馏水中; | B.100mL 0.2 mol·L-1AgNO3溶液中; |
| C.100 mL 0.1 mol·L-1AlCl3溶液中; | D.100mL 0.1 mol·L-1盐酸溶液中。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
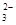 )+c(HCO
)+c(HCO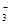 )]
)]| A.①④ | B.②③ | C.①③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH | B.NaHSO4 | C.HC1 | D.NH4NO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(CH3COOH)=0.01mol·L-1 |
| B.c(H+)=c(CH3COO-) |
| C.加水稀释100倍后,溶液pH=4 |
| D.醋酸的电离常数为Ka,CH3COO-的水解常数为Kh,则Ka·Kh=Kw |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.X曲线是NaOH溶液滴定盐酸,Y曲线是NaOH溶液滴定醋酸 |
| B.当NaOH溶液体积为10mL时,把甲和乙溶液混合,则存在C(Cl-) =C(Na+)>C(CH3COOH)>C(H+)>C(CH3COO-) |
| C.当滴定到pH=7的甲、乙溶液中溶液中存在:C(Cl-)= C(CH3COO-) |
| D.当NaOH溶液体积为20mL时,甲、乙溶液存在C(Cl-)= C(CH3COOH) + C(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2H2+O2=2H2OΔH=-142.9 kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1 |
| C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H++OH- ΔH=Q(Q>0)的平衡,下列叙述一定正确的是
H++OH- ΔH=Q(Q>0)的平衡,下列叙述一定正确的是| A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小 |
| B.将水加热,Kw增大,pH减小 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.向水中加入少量固体硫酸钠,c(H+)=10-7 mol·L-1,Kw不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

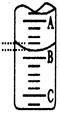
| A.22.30 mL | B.22.35 mL | C.23.65 mL | D.23.70 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com