
| A、x+y<z |
| B、平衡向正反应方向移动 |
| C、B的转化率升高 |
| D、C的体积分数下降 |


科目:高中化学 来源: 题型:
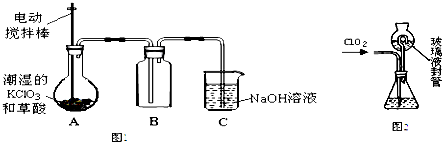
查看答案和解析>>
科目:高中化学 来源: 题型:
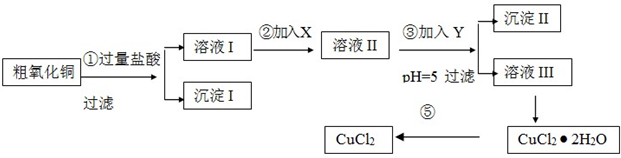
| 氧化剂 | 调节pH的物质 | ||
| A | 双氧水 | E | 氨水 |
| B | 高锰酸钾 | F | 碱式碳酸铜 |
| C | 氯水 | G | 氧化铜 |
| D | 硝酸 | H | 氢氧化铜 |
| 物质 | 开始沉淀时pH | 完全沉淀时pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 5.2 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
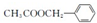 是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成,其中一种合成路线如下:
是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成,其中一种合成路线如下: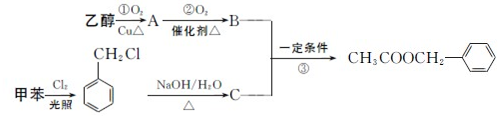
查看答案和解析>>
科目:高中化学 来源: 题型:
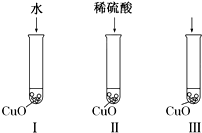 氧化铜是一种黑色固体,可溶于稀硫酸.某化学兴趣小组为探究稀硫酸中哪种粒子能使氧化铜溶解,该小组同学提出如下假设:
氧化铜是一种黑色固体,可溶于稀硫酸.某化学兴趣小组为探究稀硫酸中哪种粒子能使氧化铜溶解,该小组同学提出如下假设:查看答案和解析>>
科目:高中化学 来源: 题型:
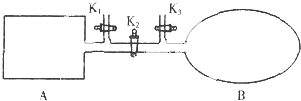
| A、到达平衡时A和B中NO2气体体积分数相同 |
| B、若在A、B中再充入与初始量相等的NO2,则达到平衡时A、B中NO2转化率都增大 |
| C、若气球的体积不再改变,表明B中反应已达到平衡 |
| D、室温下,若设法使A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时B中气体的颜色较深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③⑤⑥⑦ | B、②⑤⑦⑥ |
| C、①③⑤⑥⑦ | D、③④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热时苏打较稳定,小苏打不稳定,易分解 |
| B、相同温度下,小苏打较苏打易溶于水 |
| C、苏打是发酵粉的主要成分之一,也用于治疗胃病 |
| D、小苏打常用作洗涤剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com