
【题目】某研究小组为探究不溶性固体X的组成和性质,进行了如下实验。已知X是一种仅含有四种元素的具有固定成的盐类物质,H由碘元素和另外一种元素组成,图中所有气体体积均在标准状况下测定。
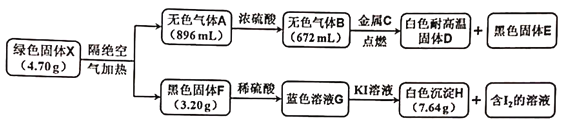
请回答下列问题:
(1)写出X的化学式__________;
(2)写出C的原子结构示意图___________;组成E元素的某种核素常用于考古断代,该原子核内中子数为8,写出该校素的原子符号___________。
(3)C在装有B的集气瓶中燃烧,其实验现象为___________;并写出相应的化学方程式___________。
(4)已知H能与含NaClO的碱性溶液反应生成NaIO3和蓝色絮状沉淀,试写出该反应的离子方程式____________________________。
【答案】Cu(OH)2·3CuCO3 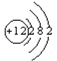 146C 剧烈燃烧,发出耀眼白光,产生白烟,有黑色固体生成 2Mg+CO2
146C 剧烈燃烧,发出耀眼白光,产生白烟,有黑色固体生成 2Mg+CO2![]() 2MgO+C 2CuI+7ClO-+2OH-+H2O=2Cu(OH)2+2IO3-+7Cl-
2MgO+C 2CuI+7ClO-+2OH-+H2O=2Cu(OH)2+2IO3-+7Cl-
【解析】
绿色固体X隔绝空气加热得到无色气体A,通过浓硫酸变为无色气体B,减少的为生成的水蒸气,金属C与B反应生成白色耐高温固体D和黑色固体E,推断D为MgO,E为C,则C为Mg,B为CO2;分解生成的黑色固体F加入稀硫酸反应得到蓝色溶液G为硫酸铜溶液,则黑色固体F为CuO,蓝色溶液G加入KI溶液反应生成白色沉淀H和含I2的溶液,结合氧化还原反应得到碘离子被铜离子氧化为碘单质,铜离子被还原为CuI,H为CuI,结合元素守恒计算分析判断X的化学式。
绿色固体X4.70g隔绝空气加热得到无色气体A的体积896mL,通过浓硫酸无色气体B体积为672mL,减少的为生成的水蒸气,体积=896mL-672mL=224mL,金属C在无色气体B中点燃反应生成白色耐高温固体D和黑色固体E,推断D为MgO,E为C,则C为Mg,B为CO2,物质的量n(CO2)=0.672L÷22.4L/mol=0.03mol,n(H2O)=0.224÷22.4L/mol=0.01mol,分解生成的黑色固体F质量为3.20g,加入稀硫酸反应得到蓝色溶液G为硫酸铜溶液,则黑色固体F为CuO,其物质的量n(CuO)=3.20g÷80g/mol=0.04mol,蓝色溶液G加入KI溶液反应生成白色沉淀H7.64g,和含I2的溶液,结合氧化还原反应得到碘离子被铜离子氧化为碘单质,铜离子被还原为CuI,H为CuI,其物质的量n(CuI)=7.64g÷191g/mol=0.04mol,则X组成元素为Cu、C、H、O元素,其中4.70gX中含C元素物质的量0.03mol,H元素物质的量=0.01mol×2=0.02mol,Cu元素物质的量=0.04mol,氧元素物质的量=(4.70g-0.03mol×12g/mol-0.02mol×1g/mol-0.04mol×64g/mol)÷16g/mol=0.11mol,n(Cu):n(H):n(C):n(O)=0.04:0.02:0.03:0.11=4:2:3:11,化学式Cu4H2C3O11,分解产物分析得到化学式为Cu(OH)2·3CuCO3;
(2)镁的原子序数是12,则Mg的原子结构示意图为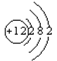 ;组成E元素的某种核素常用于考古断代,该元素是碳元素,该原子核内中子数为8,则质量数是6+8=14,因此该核素的原子符号为146C;
;组成E元素的某种核素常用于考古断代,该元素是碳元素,该原子核内中子数为8,则质量数是6+8=14,因此该核素的原子符号为146C;
(3)镁在装有二氧化碳的集气瓶中燃烧,反应的化学方程式为2Mg+CO2![]() 2MgO+C,则其实验现象为剧烈燃烧,发出耀眼白光,产生白烟,有黑色固体生成;
2MgO+C,则其实验现象为剧烈燃烧,发出耀眼白光,产生白烟,有黑色固体生成;
(4)已知H能与含NaClO的碱性溶液反应生成NaIO3和蓝色絮状沉淀,沉淀是氢氧化铜,碘元素被氧化为碘酸根离子,则该反应的离子方程式为2CuI+7ClO-+2OH-+H2O=2Cu(OH)2+2IO3-+7Cl-。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】咖啡酸苯乙酯![]() 是一种天然抗癌药物。在一定条件下能发生如下转化。
是一种天然抗癌药物。在一定条件下能发生如下转化。
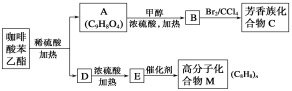
请回答下列问题:
(1)A分子中的官能团是_______________________________。
(2)高分子化合物M的结构简式是_______________________________。
(3)写出A→B反应的化学方程式:_________________________。A→B的反应类型为__________。
(4)E→M的反应方程式为_____________________;B→C的反应类型为__________。
(5)A的同分异构体有很多种,其中同时符合下列条件的同分异构体有________种。
①苯环上只有两个取代基 ②能发生银镜反应③能与碳酸氢钠溶液反应 ④能与氯化铁溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨和硝酸都是重要的工业原料。
(1)标准状况下,将500 L氨气溶于水形成1 L氨水,则此氨水的物质的量浓度为__mol· L-1(保留三位有效数字)。工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为__。
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为__。
下列反应中的氨与氨氧化法中的氨作用相同的是__。
A.2Na+2NH3===2NaNH2+H2↑ B.2NH3+3CuO===3Cu+N2+3H2O
C.4NH3+6NO===5N2+6H2O D.HNO3+NH3===NH4NO3
工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH﹣===NO2-+NO3-+H2O和NO+NO2+2OH﹣===□ +H2O(配平该方程式)。______________
(3)向27.2 g Cu和Cu2O的混合物中加入某浓度的稀HNO3500 mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1 L 1 mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2 g。
①Cu与稀HNO3反应的离子方程式为__。
②Cu与Cu2O 的物质的量之比为__。
③HNO3的物质的量浓度为__mol·L-1。
(4)有H2SO4和HNO3的混合溶液20 mL,加入0.25 molL﹣1Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液呈中性)。则原混合液中H2SO4的物质的量浓度为__mol·L-1,HNO3的物质的量浓度为__mol·L-1。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素a、b、c、d的原子序数依次增大,a和b的价电子数之和等于c和d的最外层电子数之和,这四种元素组成两种盐b2da3和bca2。在含该两种盐的混合溶液中滴加盐酸,产生白色沉淀的物质的量与盐酸体积的关系如图所示。下列说法正确的是( )

A. 原子半径:b>c>a>d B. 气态氢化物热稳定性:a>d
C. d的氧化物常用于太阳能电池 D. 工业上电解c的氯化物冶炼单质c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素元素是非金属性很强的一类元素,能形成多种物质。
(1)氯气能氧化许多种还原剂,同时在适当条件下又可发生自身氧化还原反应。
①将足量的氯气通入到H2S溶液中,再向所得的溶液中加入用盐酸酸化的BaCl2溶液可得到白色沉淀,写出前一个反应的离子方程式:____________________________。
②将0.1molCl2缓慢通入到amL、浓度为2mol/L的KOH溶液中,二者恰好反应完,测得溶液c(ClO-)∶c(ClO3-)∶c(Cl-)=2∶1∶7,则a=______________。
(2)KClO3是一种重要的氧化剂,工业上制备KClO3的方法之一如下:
![]()
①写出电解时反应的化学方程式:_______________________________。
②相同温度下,两种氯酸盐的溶解度相对大小:NaClO3___________KClO3(填“>”或“<”)。
③KClO3在MnO2的催化作用下加热分解生成氧气的反应历程如下,请填写空白处:
2KClO3+2MnO2![]() 2KMnO4+Cl2↑+O2↑;
2KMnO4+Cl2↑+O2↑;
2KMnO4![]() K2MnO4+MnO2+O2↑,
K2MnO4+MnO2+O2↑,
K2MnO4+Cl2![]() O2↑+___________+___________。
O2↑+___________+___________。
反应结束后将固体混合物分离开的主要操作是__________________________。
(3)已知Cl2O是酸性氧化物,将Cl2O通入到水中可得到一种酸性溶液,请写出该溶液具有的除酸性外的一种化学性质______________。若将该气体通入到NaOH溶液中恰好完全反应,则溶液中各离子浓度由大到小的顺序为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用硫铁矿(FeS2)焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),流程如下:
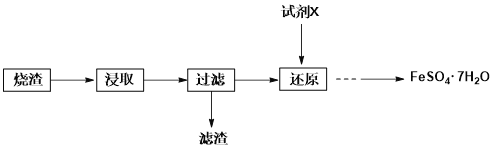
(1)试剂X可能为______________。
A.双氧水 B.酸性高锰酸钾 C.浓硫酸 D.SO2
(2)从还原后溶液中得到产品,应进行的操作是___________、____________、过滤、洗涤、干燥。
(3)七水合硫酸亚铁(FeSO4·7H2O)在医学上常用作补血剂。某课外小组通过以下实验方法测定某补血剂中亚铁离子的含量。
步骤a:取10片补血剂样品除去糖衣、研磨、溶解、过滤,将滤液配成500 mL溶液;
步骤b:取上述溶液25mL于锥形瓶中,逐渐滴加0.0500 mol/L的酸性KMnO4溶液,至恰好完全反应,记录消耗的酸性KMnO4溶液的体积(假定药品中其他成分不与酸性KMnO4反应);
步骤c:重复步骤b2~3次,平均消耗酸性KMnO4溶液20.00mL。
已知:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,则该补血剂中亚铁离子的含量为_____mg/片。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型电池的开发与使用在现代社会中已很普遍,一种水煤气燃料电池的能量转化率可达90%以上。下列说法正确的是
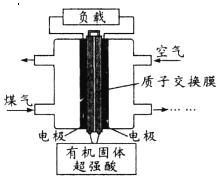
A. 总反应为2CO+O2==2CO2
B. 负极反应为H2-2e—==2H+、CO-2e—+H2O==CO2+2H+
C. 电路中通过4 mol电子,正极消耗22.4 L(标准状况)空气
D. 有机固体中的H+在放电时向正极移动,造成正极pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
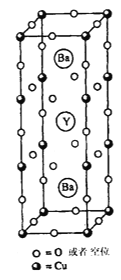
【题目】1911年,科学家发现汞在4.2K以下时电阻突然趋近于零——即低温超导性。1986年,科学家又发现了Nb3Ge在23K下具有超导性。1987年2月,赵忠贤及合作者独立发现了在液氮温区(沸点77 K)的高温超导体,其晶胞如图所示,元素组成为Ba-Y-Cu-O(临界温度93 K),推动了国际高温超导研究。赵忠贤院士获得2016年度国家最高科学技术奖。
回答下列问题:
(1)铌Nb位于第五周期,Nb的外围电子排布式为4d45s1,Nb位于_______族
(2)下列关于Ge元素叙述正确的是______(从下列选项中选择)
A.Ge晶体属于准金属,且为共价晶体 B.Ge属于p区的过渡金属
C.Ge的第一电离能比As、Se均要小 D.Ge的电负性比C大
(3)Ge(CH3)2Cl2分子的中心原子Ge的杂化方式是______________
(4)NH3也常作致冷剂,其键角_______(填“大于”或“小于”)109°28′,NH3的沸点(239.6 K)高于N2沸点的主要原因是___________________________
(5)图示材料的理想化学式(无空位时)为___________________,若Y(钇)元素的化合价为+3,则Cu的平均化合价为_______
(6)金属铜属于面心立方最密堆积,其晶胞中Cu原子的最近距离为a cm,金属铜的晶体密度为ρ g/cm3,阿伏伽德罗常数为NA,则铜的相对原子质量为________ (只含一个系数,用a、ρ、NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年11月30日第21届联合国气候大会在巴黎召开,会议的一项主题是温室气体减排。如图是科学家正在研发的实现CO2和H2合成甲醇的燃烧电池。下列叙述正确的是
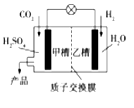
A.乙槽中反应生成水
B.甲槽中的电极反应式为:CO2+6e-+5H2O=CH3OH+6OH-
C.质子从乙槽通过质子交换膜进入甲槽
D.放电过程中,乙槽的电极附近溶液的pH升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com