
【题目】现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过分析比较,认为无需检验就可判断其中必有的两种物质是 和 。(填化学式)
(2)为了确定X,现将(1)中的两种物质记为A和B,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕色沉淀,向该沉淀中滴入稀硝酸,沉淀部分溶解,最后留有白色沉淀不再溶解。则:
①X为 。
A.SO32-B.SO42- C.CH3COO-D.SiO32-
②A中的化学键类型为
③将0.02mol的A与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为 (精确到0.1g)。
④利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论
(3)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀硫酸,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的 (填相应的离子符号)。有关反应的离子方程式为
【答案】(1)Na2CO3和 Ba(OH)2;
(2)①B ②离子键和共价键 ③6.1g ④分别取少量D、E溶液于试管中,分别滴加过量的Ba(OH)2溶液,产生白色沉淀的其中含有Mg2+,先产生白色沉淀,后沉淀又溶解的含有Al3+;
(3)![]()
![]()
【解析】试题分析:(1)根据离子共存进行判断,CO32-与Al3+、Mg2+、Ba2+、Fe3+不能大量共存,因此CO32-只能与Na2+组合,即Na2CO3,OH-与Al3+、Mg2+、Fe3+不能大量共存,因此OH-与Ba2+进行组合,即Ba(OH)2;(2)当C与B的溶液混合时,产生红褐色沉淀和无色无味气体,应是发生双水解反应,因此B为Na2CO3,C中含有Fe3+,则A为Ba(OH)2,当C与A的溶液混合时产生棕色沉淀,向沉淀中滴入稀硝酸,沉淀部分溶解,最后白色沉淀不再溶解,说明最后沉淀是BaSO4,即C为Fe2(SO4)3,选项B正确;②根据上述推断A为Ba(OH)2,属于离子化合物,含有离子键和共价键;③发生反应是3Ba(OH)2+Fe2(SO4)3=2Fe(OH)3↓+3BaSO4↓,根据投入量,氢氧化钡不足,硫酸铁过量,因此生成沉淀的质量为0.02×2×107/3+0.02×3×233/3g≈6.1g;④利用Al(OH)2表现两性,既能和酸反应又能与强碱反应的性质,而氢氧化镁只能与酸反应,进行检验,操作是:分别取少量D、E溶液于试管中,分别滴加过量的Ba(OH)2溶液,产生白色沉淀的是Mg2+,先产生白色沉淀,后溶解的是Al3+;(3)滴加稀硫酸后管口有红棕色气体产生,此气体为NO2,说明溶液中含有NO3-,其反应方程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,2NO+O2=2NO2。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.反应热是1 mol物质参加反应时的能量变化
B.当反应放热时ΔH>0,反应吸热时ΔH<0
C.任何条件下,化学反应的焓变都等于化学反应的反应热
D.在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓的差值来决定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
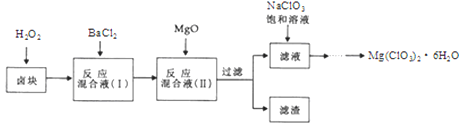
已知:
①.卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②.四种化合物的溶解度(S)随温度(T)变化曲线如图所示。回答下列问题:
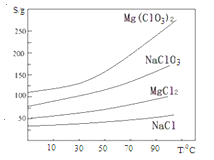
(1).过滤时主要的玻璃仪器有
(2).加入BaCl2的目的是除去杂质离子,检验已沉淀完全的方法是
(3).加入H2O2溶液的作用是: ;加入MgO的作用是
(4).滤渣的主要成分为 。
(5).向滤液中加入NaClO3饱和溶液后,发生反应的化学方程式为:MgCl2 + 2NaClO3 = Mg(ClO3)2↓ + 2NaCl,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为① ;②趁热过滤;③ ;④过滤、洗涤、干燥。
(6).产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2: 取10.00 mL于锥形瓶中,加入10.00 mL稀硫酸和20.00mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.l000 mol·L-1K2Cr2O7溶液滴定剩余的Fe2+至终点,此过程中反应的离子方程式为:Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ +6Fe3++7H2O。
步骤4:将步骤2、3重复两次,计算得平均消耗K2Cr2O7溶液15.00 mL。
①写出步骤2中发生反应的离子方程式(还原产物为Cl-)
②产品中Mg(ClO3)2·6H2O的质量分数为 【Mg(ClO3)2·6H2O的相对分子质量为299,列出表达式即可)】
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)A、B、C、D、E、F、G为原子序数依次递增的7种短周期主族元素。A、B元素的最高正价与最低负价的代数和均为零;C元素是植物生长三大营养元素之一;D的单质具有强氧化性,D的氢化物形成的酸常用于雕刻玻璃;E原子核外K层电子数与M层电子数相等;F原子的价电子数等于电子层数的两倍。请回答下列问题 :
(1)CD3的电子式为______________;
(2)用离子方程式表示G的非金属性比F强______________;
(3)C与E形成的化合物溶解于水中的反应方程式为______________;
(4)C的氢化物与G的单质以物质的量之比1:3反应,生成二元化合物X和一种气体,该气体遇氨气产生“白烟”,则X的化学是为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.己知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质.(部分反应物、生成物及反应条件己略去)
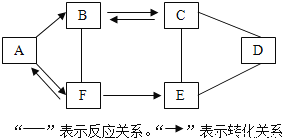
请回答:
(1)写出A、D、F的化学式:A______,D______ ,F________。
(2)写出C物质的一种用途___________,C与E反应的化学方程式是___________。
(3)图中物质相互间发生的反应.未涉及的基本反应类型是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com