
【题目】某学习小组用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备Fe3O4纳米材料的流程示意图如下:


已知:步骤⑤中,相同条件下测得Fe3O4的产率与R( )的关系如图所示。
)的关系如图所示。
(1)为提高步骤①的反应速率,可采取的措施是_______________(任写一点) 。
(2)步骤②中,主要反应的离子方程式是________________________。
(3)浊液D中铁元素以FeOOH形式存在。步骤④中,反应的化学方程式是___________________;步骤④中,反应完成后需再加热一段时间除去剩余H2O2目的是____________________________
(4)⑤反应的离子方程式为_________________ ;步骤⑤中的“分离”包含的步骤有______________________。
(5)设浊液D中FeOOH的物质的量为amol,滤液B中的铁元素的物质的量为bmol。为使Fe3O4的产率最高,则![]() =_________。(填数值,小数点后保留3位)
=_________。(填数值,小数点后保留3位)
【答案】 搅拌、适当升高温度 2Fe3+ + Fe = 3Fe2+ 2Fe(OH)2 +H2O2=2FeOOH + 2H2O 加热使其分解除去,防止其在步骤⑤中继续氧化+2价铁元素 2FeOOH+Fe2++2OH-![]() Fe3O4+2H2O 过滤、洗涤 0.636
Fe3O4+2H2O 过滤、洗涤 0.636
【解析】(1)这是在溶液中进行的反应,为了提高反应速率,可采用搅拌,或适当升高温度,或者适当增大盐酸的浓度;
(2)由铁泥的主要成分为Fe2O3、FeO和少量Fe可知,在与盐酸反应后的滤液A中有FeCl3、FeCl2及剩余的HCl,所以加入铁粉后的反应有:2Fe3+ + Fe = 3Fe2+和Fe+2H+=Fe2++H2↑,其中主要的反应为2Fe3+ + Fe = 3Fe2+;
(3)浊液C为Fe(OH)2,而浊液D为FeOOH,所以步骤④的反应方程式为2Fe(OH)2 +H2O2
=2FeOOH + 2H2O,反应完成后继续加热,是为了除去H2O2,防止在与滤液B(即FeCl2)混合时氧化Fe2+;
(4)根据转化关系可知,步骤⑤中反应物为浊液D中的FeOOH和滤液B中的Fe2+,结合反应环境,可写出反应的离子方程式为2FeOOH+Fe2++2OH-![]() Fe3O4+2H2O;为了除去纳米Fe3O4中的浊液杂质,可用过滤、洗涤的方法进行分离;
Fe3O4+2H2O;为了除去纳米Fe3O4中的浊液杂质,可用过滤、洗涤的方法进行分离;
(5)已知浊液D中FeOOH的物质的量为amol,即Fe3+的物质的量为amol,滤液B中的铁元素的物质的量为bmol,则与浊液D中FeOOH反应的Fe2+的物质的量为(b-a)mol,由图象可知当Fe3O4的产率最高时,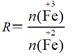 =1.75=
=1.75=![]() ,则
,则![]() =0.636。
=0.636。


科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下均能通过一步反应实现的是( )
A. NaAlO2(aq)![]() AlCl3
AlCl3![]() Al2O3 B. N2
Al2O3 B. N2![]() NO2
NO2![]() HNO3
HNO3
C. NaCl(饱和)![]() NaHCO3
NaHCO3![]() Na2CO3 D. FeS2
Na2CO3 D. FeS2![]() SO3
SO3![]() H2SO4
H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用可再生的物质制备乙酸乙酯的绿色合成路线之一如图所示: 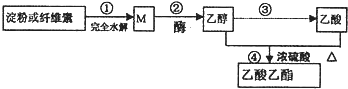
下列说法正确的是( )
A.常温下,M能与银氨溶液发生反应
B.④的反应类型属于酯化反应,不属于取代反应
C.用饱和碳酸钾溶液能鉴别乙醇、乙酸和乙酸乙酯
D.淀粉和纤维素的化学式均为(C6H10O5)n , 二者互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 22.4 L O2中含有氧分子的个数为NA
B. 24 g Mg与足量氧气反应失去的电子数为2NA
C. 28 g N2中含有氮原子的个数为NA
D. 1 mol·L-1 MgCl2溶液中含有氯离子个数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加碘盐的主要成分是NaCl,还添加了适量的KIO3。下列说法中正确的是 ( )
A. KIO3和NaCl为离子化合物,均只含离子键
B. KIO3中阳离子的结构示意图为![]()
C. 23Na37Cl中质子数和中子数之比是8∶7
D. 次碘酸的结构式为H—O—I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)漂白粉或漂粉精的有效成分是______(填化学式);
写出将氯气通入冷的消石灰中制取漂白粉的方程式____。
(2)![]() 的水溶液俗称_____,是制备硅胶和木材防火剂的原料。
的水溶液俗称_____,是制备硅胶和木材防火剂的原料。
(3)________是制造光导纤维的重要原料,生产普通玻璃和水泥都用到的原料是__。
(4)NO2是______色有毒气体,NO2与水反应的方程式为___________,标准状况下67.2L NO2与水反应转移电子______mol。
(5)中国的瓷器驰名世界,制备陶瓷是以黏土[主要成分Al2Si2O5(OH)4]为原料,经高温烧结而成。若以氧化物形式表示黏土的组成,应写为:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】少量杂质(括号内为杂质),选用试剂和分离方法能达到实验目的的是
混合物 | 试剂 | 分离方法 | |
A | 乙烷(乙烯) | (H+)KMnO4 | 洗气 |
B | 乙醇(H2O) | 新制CaO | 蒸馏 |
C | 苯(苯酚) | 溴水 | 过滤 |
D | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置来分离CO2和CO混合气体并干燥,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为()
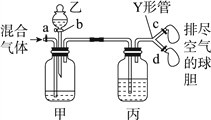
甲 | 乙 | 丙 | |
A | 饱和NaHCO3溶液 | 12 mol·L-1盐酸 | 18.4 mol·L-1 H2SO4 |
B | 饱和Na2CO3溶液 | 2 mol·L-1 H2SO4 | 饱和NaOH溶液 |
C | 饱和NaOH溶液 | 2 mol·L-1 H2SO4 | 18.4 mol·L-1 H2SO4 |
D | 18.4 mol·L-1 H2SO4 | 饱和NaOH溶液 | 18.4 mol·L-1 H2SO4 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com