
����Ŀ����1��8.5g���������Ӻ��еĵ�����ĿΪ_______��
��2��3.1gNa2X����Na0.1mol����Na2X��Ħ������Ϊ______��X�����ԭ������Ϊ_______��
��3����1gCO2�к���x��ԭ�ӣ����ӵ������ɱ�ʾΪ_______��
��4��������ء� ��������������ɵĻ����Һ������c(H)0.1mol/L��c(Fe3)0.3mol/L��c(SO42)0.6mol/L����c(K)Ϊ_______��
��5����ͬ���ʵ�����Ũ�ȵ��Ȼ��ơ��Ȼ�þ���Ȼ�����Һ���ֱ�����������Һ��Ӧ�������ɳ���������֮��Ϊ3��2��1ʱ��������������Һ�������Ϊ_______��
���𰸡�5NA ��3.011024 62g/mol 16 ![]() mol��1 0.2mol/L 9��3��1
mol��1 0.2mol/L 9��3��1
��������
(1)���������Ӻ���10�����ӣ�����n��![]() ��
��![]() ���㣻
���㣻
(2)����n(Na2X)��![]() n(Na+)�����Na2X�����ʵ�����Ȼ����M��
n(Na+)�����Na2X�����ʵ�����Ȼ����M��![]() ������Ħ�����������Ħ����������X�����ԭ��������
������Ħ�����������Ħ����������X�����ԭ��������
(3)����n��![]() ���������̼���ʵ���������ԭ�����ʵ���Ϊ������̼��3�����ٸ���N��nNA���㰢���ӵ�������
���������̼���ʵ���������ԭ�����ʵ���Ϊ������̼��3�����ٸ���N��nNA���㰢���ӵ�������
(4)���ݵ���غ��֪��c(K+)+c(H+)+3c(Fe3+)��2c(SO42��)���ݴ˼���c(K+)��
(5)������Ag++Cl����AgCl������NaCl��MgCl2��AlCl3����������Һ��Ӧ����AgCl�����ʵ����ֱ�Ϊ3mol��2mol��1mol�������������غ����NaCl��MgCl2��AlCl3�����ʵ������ٸ���V��![]() ��֪����ҺŨ����ȣ������֮ͬ�ȵ������ʵ���֮�ȡ�
��֪����ҺŨ����ȣ������֮ͬ�ȵ������ʵ���֮�ȡ�
(1)8.5g���������ӵ����ʵ���Ϊ��![]() ��0.5mol�����е��ӵ����ʵ���Ϊ��0.5mol��10��5mol�����еĵ�����Ϊ5NA��
��0.5mol�����е��ӵ����ʵ���Ϊ��0.5mol��10��5mol�����еĵ�����Ϊ5NA��
(2)n(Na2X)��![]() n(Na+)��0.1mol��
n(Na+)��0.1mol��![]() ��0.05mol��M(Na2X)��
��0.05mol��M(Na2X)��![]() ��62g/mol��Na2X����Է�������Ϊ62��X�����ԭ������Ϊ��62��23��2��16��
��62g/mol��Na2X����Է�������Ϊ62��X�����ԭ������Ϊ��62��23��2��16��
(3)1g CO2�����ʵ���Ϊ��![]() ��
��![]() mol������x��ԭ�ӣ���
mol������x��ԭ�ӣ���![]() mol��3��NA��x������NA��
mol��3��NA��x������NA��![]() mol��1��
mol��1��
(4)���ݵ���غ��֪��c(K+)+c(H+)+3c(Fe3+)��2c(SO42��)����c(K+)+0.1mol/L+3��0.3mol/L��2��0.6mol/L����ã�c(K+)��0.2mol/L��
(5)��ͬŨ�ȵ�NaCl��MgCl2��AlCl3������Һ�ֱ�����������Һ��Ӧ�������ɳ���������֮��Ϊ3��2��1����NaCl��MgCl2��AlCl3����������Һ��Ӧ����AgCl�����ʵ����ֱ�Ϊ3mol��2mol��1mol�������������غ㣬��n(NaCl)��3mol��n(MgCl2)��![]() ��1mol��n(AlCl3)��
��1mol��n(AlCl3)��![]() ��
��![]() mol���ٸ���V��
mol���ٸ���V��![]() ��֪����ҺŨ����ȣ������֮ͬ�ȵ������ʵ���֮�ȣ���V(NaCl)��V(MgCl2)��V(AlCl3)��3mol��1mol��
��֪����ҺŨ����ȣ������֮ͬ�ȵ������ʵ���֮�ȣ���V(NaCl)��V(MgCl2)��V(AlCl3)��3mol��1mol��![]() mol��9��3��1��
mol��9��3��1��


 ���100��1�ž�ϵ�д�
���100��1�ž�ϵ�д� ��ĩ�óɼ�ϵ�д�
��ĩ�óɼ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������A��B��C��D�����л�����й���Ϣ��
A | ����ʹ������Ȼ�̼��Һ��ɫ���ڱ���ģ��Ϊ ������ˮ��һ�������·�Ӧ�����л���C |
B | ����C��H����Ԫ����ɣ������ģ��Ϊ |
C | ����C��H��O����Ԫ����ɣ�������Na��Ӧ����������NaOH��Һ��Ӧ������Cu�������Ҽ�������������O2��Ӧ |
D | ����C��H��O����Ԫ����ɣ������ģ��Ϊ ������C��Ӧ������Է�������Ϊ100���� |
�ش��������⣺
��1��A��������Ȼ�̼��Һ��Ӧ���������������___��
��2��B���������____(�����)��
����ɫ��ζҺ�� ���ж� �۲�����ˮ ���ܶȱ�ˮ�� ��������KMnO4��Һ����ˮ��Ӧ��ɫ ���κ������²���������Ӧ ������ˮ��Ϻ�Һ��ֲ����ϲ�ʳȺ�ɫ��
��3����B�Ʊ��������Ļ�ѧ����ʽ____��
��4��D��C��Ӧ��������Է�������Ϊ100�������÷�Ӧ�ķ�Ӧ����Ϊ___���仯ѧ����ʽΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������谷(�ṹ��ʽ��ͼ��ʾ)��һ����Ҫ�Ļ���ԭ�ϣ���������ȼ����ˮ���ˮ���߷��Ӻϳɵ�����һЩ��������ȴ��ţ���м��������谷�����������Ʒ�ĺ�����������˵����ȷ����
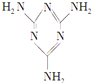
A. �����谷��һ�ֵ�����B. �����谷���Ǹ߷��ӻ�����
C. �����谷�����к���̼̼˫��D. �����谷�ķ���ʽΪC3H6N6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2��I2��һ���������ܷ�����Ӧ��H2(g)+I2(g)![]() 2HI(g) ��H=��a kJ��mol-1��֪������˵����ȷ���ǣ� ��
2HI(g) ��H=��a kJ��mol-1��֪������˵����ȷ���ǣ� ��

A.H2��I2��HI�����еĻ�ѧ�����ǷǼ��Թ��ۼ�
B.��ͬ�����£�1 mol H2(g)��1 mol I2(g)��������С��2 mol HI(g)��������
C.�Ͽ�2 mol HI�����еĻ�ѧ����������ԼΪ(c+b+a)kJ
D.���ܱ������м���2 mol H2(g)��2 mol I2(g)����ַ�Ӧ��ų�������Ϊ2a kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������ĵ��볣�����±���

����������ȷ����
A. �������NaClO��Һ����ܹ�������Ӧ��HF+NaClO=HClO+NaF
B. ���ʵ���Ũ����ͬ�Ģ�NaF��Na2CO3��NaClO������Һ��pH����>��>��
C. Na2CO3��Һ����������ᷢ����Ӧ
D. ����CO2ͨ��NaClO��Һ�е����ӷ�Ӧ��CO2+H2O+2ClO-= CO32-+2HClO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Fe2+��I-��Br-����Һ��ͨ������Cl2,��Һ�и������ӵ����ʵ����仯��ͼ��ʾ�������й�˵����ȷ����( )
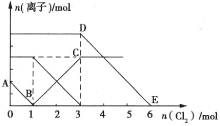
A.�߶�BC����Cl-���ʵ����ı仯���
B.ԭ�����Һ��c(FeBr2)=6mol��L-1
C.��ͨ��2mol Cl2ʱ,��Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.ԭ��Һ��n(Fe2+):n(I-):n(Br-)=2:2:3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(ClO2)����������ˮ�������Դ���Ϊԭ������C1O2�Ĺ�����Ҫ�����������ξ��ƣ����������NaC1��Һ����C1O2����ȡ��������������ͼ��
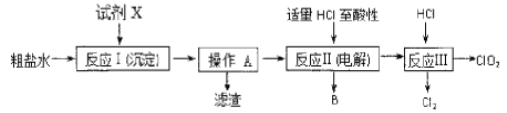
�ṩ���Լ�������Na2CO3��Һ������K2CO3��Һ��NaOH��Һ��BaCl2��Һ��Ba(NO3)2��Һ
��1����ʳ��ˮ�к���Ca2+��Mg2+��![]() �����ʡ����Ӳ���ʱ��������ˮ���ȼ���������Լ�X��ѡ���Լ�X���������Լ������μ�˳������Ϊ��__________________________(�ѧʽ)��
�����ʡ����Ӳ���ʱ��������ˮ���ȼ���������Լ�X��ѡ���Լ�X���������Լ������μ�˳������Ϊ��__________________________(�ѧʽ)��
��2�����������У���ʳ��ˮ���ض������µ��õ��������������ᷴӦ����C1O2����Ӧ���Ļ�ѧ����ʽΪ______________��
��3��ClO2�ܲ��ȶ������������ƣ�������ˮ���յõ�ClO2��Һ��Ϊ�ⶨ������Һ��ClO2�ĺ���������������ʵ�飺
����1��ȷ��ȡClO2��Һ10��00 mL��ϡ�ͳ�100 mL������
����2����ȡV1 mL�������뵽��ƿ�У�����������pH��2��0������������KI���壬ҡ�ȣ��ڰ�������30���ӡ�����֪ClO2+I��+H+==I2+Cl��+H2Oδ��ƽ��
����3���Ե�����Һ��ָʾ������c mol��L-1Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2mL��(��֪��![]() )
)
��ȷ��ȡ10��00 mL ClO2��Һ�IJ���������__________________��
����������3�еζ��յ��������__________________________��
����ʵ����ʹ�õ�Na2S2O3����Һ�������������������ʣ���ʵ����_________(����ƫ��������ƫ����������Ӱ����)
�ܸ�����������ɼ����ԭC1O2��Һ��Ũ��Ϊ_________mol��L-1(�ú���ĸ�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����84����Һ������Чɱ�����H1N1�Ȳ�����ijͬѧ������ һƿ��84����Һ����������������Ϻ�����Һ��װ˵���õ� ������Ϣ����84����Һ����25%NaC10��1000 mL���ܶ� 1. 192 g/cm 3,ϡ��100��(�����)��ʹ�á������������Ϣ�����֪ʶ�ش��������⣺
��1���á�84����Һ����NaClO�����ʵ���Ũ��Ϊ________ mol/L��
��2����ͬѧȡ100 mLϡ�ͺ������Һ����������ϡ�ͺ���Һ�� c(Na+)Ϊ_______mol/L��
��3����ͬѧ���ĸá�84����Һ�����䷽������NaClO��������480 mL��4. 0 mol/L NaClO������Һ������˵����ȷ����________�������)��
A.����ƿ������ˮϴ����Ӧ��ɺ����������Һ����
B.���ù������ƷNaClO�����ƣ����ܵ��½��ƫ��
C.��Ҫ����NaClO���������Ϊ143. 0 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽ��������������Na2SO4��ˮ��ԭ����ͼ��ʾ�����ö��Ե缫��ab��cd��Ϊ���ӽ���Ĥ����ֱ���糡�������£���Ĥ�м��Na+��SO42-��ͨ�����ӽ���Ĥ�������˸��������ӱ��赲���ܽ����м���ҡ�����������ȷ����

A. ͨ����м���ҵ�SO42-����������Ǩ�ƣ���������ҺpH����
B. �÷��ڴ�����Na2SO4��ˮʱ���Եõ�NaOH��H2SO4��Ʒ
C. ������ӦΪ2H2O�C4e�C=O2+4H+����������ҺpH����
D. ����·��ͨ��1mol���ӵĵ���ʱ������0.5mol��O2����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com