
【题目】清洗和制绒是硅晶片制作的重要步骤之一,硅片化学清洗的主要目的是除去硅片表面杂质(如某些有机物,无机盐,金属、Si、SiO2粉尘等)。常用的化学清洗剂有高纯水、有机溶剂、双氧水、浓酸、强碱等。其中去除硅的氧化物,通常用一定浓度的HF溶液,室温条件下将硅片浸泡1至数分钟。制绒是在硅片表面形成金字塔形的绒面,增加硅对太阳光的吸收。单晶制绒通常用NaOH、Na2SiO3等混合溶液在75~90℃反应25~35 min,效果良好。回答下列问题
Ⅰ.(1)写出晶片制绒反应的离子方程式__________,对单晶制绒1990年化学家Seidel提出了一种的电化学模型,他指出Si与NaOH溶液的反应,首先是Si与OH一反应,生成SiO44一,然后SiO44一迅速水解生成H4SiO4。基于此原理分析反应中氧化剂为_______。
Ⅱ.在工业中利用镁制取硅:2Mg+SiO2![]() 2MgO+Si,同时有副反应发生:2Mg+Si
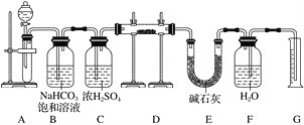
2MgO+Si,同时有副反应发生:2Mg+Si![]() Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:
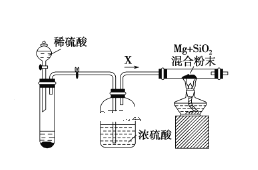
(2)由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
a.Na2SO3 b.锌粒 c.纯碱
(3)实验开始时,必须先通入X气体,再加热反应物,其理由是________,当反应开始后,移走酒精灯反应能继续进行,其原因是____________。
【答案】Si+2OH-+H2O=SiO32-+2H2↑ NaOH b 让氢气排尽装置内的空气,避免空气中的成分对实验的影响 该反应为放热反应,可以利用自身放出的热量维持反应进行
【解析】
镁为活泼金属,在空气中点燃可以和氧气或二氧化碳或水反应,在工业上利用镁制取硅,需要排尽装置中的空气,实验中应通入气体X作为保护气,X有稀硫酸制得,根据题干信息分析,用锌和稀硫酸制得的氢气排尽装置中的空气,氢气和空气的混合气体燃烧后会发生爆炸,所以反应开始前应先通入氢气排尽装置中的空气,X为氢气,用浓硫酸干燥,当反应开始后,移走酒精灯反应能继续进行,说明反应为放热反应。
(1)硅单质和氢氧化钠溶液反应生成硅酸钠和气氢气,反应的离子方程式为:Si+2OH- +H2O=SiO32-+2H2↑,在反应中,氢氧根离子中的氢得到电子生成氢气,则在反应中氧化剂应该是NaOH;
(2)镁可以和二氧化碳反应生成氧化镁和碳,镁和氢气不反应,因此用氢气做保护气,选用的药品为稀硫酸和锌粒,再用浓硫酸干燥,所以试管中的固体药品为锌粒。装置中有空气,若不用氢气排除,氢气和氧气的混合气体点燃会爆炸,所以开始前用氢气排除装置中的空气,镁和二氧化硅的反应为加热,停止加热后,反应的条件由反应放出的热量维持。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】常温,向20 ml0.1mol/L的CH3COOH溶液中滴加等浓度的NaOH溶液,已知由水电离出的氢氧根离子浓度c水(OH-)随滴入的NaOH溶液的体积变化如图所示,下列说法错误的是( )
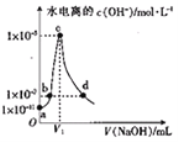
A. 常温下,醋酸的电离常数约为1×10-5
B. b、d两点溶液中均存在c(Na+)=c(CH3COO-)
C. V1=20
D. c点溶液存在:c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法正确的是
A. 1 mol硫单质在过量氧气中燃烧产生NA个SO3分子
B. 标准状况下,22.4 L SO3中含有氧原子数为3NA
C. 标准状况下,18 g H2O中含有氧原子数为NA
D. 5.4 g铝单质与足量NaOH溶液反应,转移电子数为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验过程中需注重环境保护,下列操作不会引起空气污染的是
A. 加热KMnO4制氧气的试管,用浓盐酸洗涤
B. 用稀硝酸洗涤做过银镜实验的试管
C. 硝酸亚铁和硫酸废液一同倒入废液缸
D. 将打破的水银温度计用硫粉覆盖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①R-NO2![]() R-NH2;②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。以下是用苯作原料制备一系列化合物的转化关系图:
R-NH2;②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。以下是用苯作原料制备一系列化合物的转化关系图:
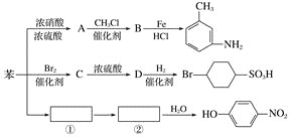
(1)A转化为B的化学方程式是______________________________。
(2)图中“苯→①→②”省略了反应条件,请写出①②物质的结构简式:①__________,②_______。
(3)苯的二氯代物有________种同分异构体。
(4)有机物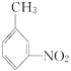 的所有原子________(填“是”或“不是”)在同一平面上。
的所有原子________(填“是”或“不是”)在同一平面上。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)。
回答下列问题:
(1)装置A中液体试剂选用________________。
(2)装置B的作用是_________。装置E中碱石灰的作用是________。
(3)装置D中发生反应的化学方程式是__________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 X、Y、Z、W 原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主族。下列说法正确的是
A. 原子半径:r(W) > r(Z) > r(Y)
B. 由X、Y 组成的化合物中均不含共价键
C. Y 的最高价氧化物的水化物的碱性比Z的弱
D. X 的简单气态氢化物的热稳定性比W的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
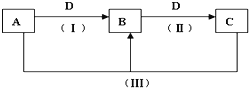
(1)若A、B、C的焰色反应均为黄色,A的水溶液能使酚酞溶液呈红色,C为发酵粉的主要成分之一,D的过度排放会造成温室效应。
①B的化学式为_____;
②反应Ⅲ的离子方程式是_______。
(2)写出Na2O2做防毒面具时涉及到的化学反应的化学方程式:____________、__________。
(3)写出Al(OH)3受热分解的化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.010 mol/L的这四种溶液pH与该元素原子半径的关系如图所示。下列说法正确的是
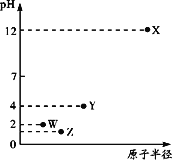
A. 简单离子半径:X>Y>Z>W
B. Y元素存在同素异形体
C. 气态氢化物的稳定性:Z>W>Y
D. X和Y的最高价氧化物对应的水化物恰好中和时,溶液呈中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com