
【题目】下列图示与对应的叙述相符的是![]()
![]()
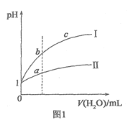

A.图1表示相同温度下![]() 的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B.图2中在b点对应温度下,将![]() 的
的![]() 与
与![]() 的NaOH溶液等体积混合后,溶液显中性
的NaOH溶液等体积混合后,溶液显中性
C.图1中,b点酸的总浓度大于a点酸的总浓度
D.图2中纯水仅升高温度,就可以从a点变到c点
【答案】B
【解析】
A.醋酸是弱电解质,在水溶液里存在电离平衡,加水稀释促进醋酸电离,氯化氢是强电解质,完全电离,导致稀释过程中,醋酸中氢离子浓度大于盐酸,所以pH变化小的为醋酸,即II为醋酸,溶液的导电性与溶液中离子浓度成正比,a点导电能力大于b,故A错误;
B. 图2中b点![]() ,中性溶液
,中性溶液![]() ;将
;将![]() 的硫酸与
的硫酸与![]() 的NaOH溶液等体积混合后,氢离子浓度和氢氧根离子浓度相同,等体积混合溶液呈中性,故B正确;
的NaOH溶液等体积混合后,氢离子浓度和氢氧根离子浓度相同,等体积混合溶液呈中性,故B正确;
C.图1中,b点为盐酸,a点为醋酸,因起点两种酸的pH值相同,故醋酸的浓度大于盐酸的,所以b点酸的总浓度小于a点酸的总浓度,故C错误;
![]() 仅升温促进水的电离,氢离子浓度和氢氧根离子浓度均增大,且氢离子浓度和氢氧根离子浓度相同,所以纯水仅升高温度,不可以从a点变到c点,故D错误。
仅升温促进水的电离,氢离子浓度和氢氧根离子浓度均增大,且氢离子浓度和氢氧根离子浓度相同,所以纯水仅升高温度,不可以从a点变到c点,故D错误。
故选B。


科目:高中化学 来源: 题型:
【题目】机动车排放的污染物主要有碳氢化合物、一氧化碳和氮氧化物等。
I.汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知: C(s)+O2(g) =CO2(g) △H1 = 393.5kJ·mol1
2C(s)+O2(g) =2CO(g) △H2 = 221.0 kJ·mol1
N2(g)+O2(g) =2NO(g) △H 3 =+180.5 kJ·mol1
CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是_________________________。
(2)研究CO和NO的催化反应,用气体传感器测得在某温度下、一定体积的密闭容器中,不同时间NO和CO浓度如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(104mol·L1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(103mol·L1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
① 前4 s内的平均反应速率υ(CO) =______mol·L1·s1。
② L、X可分别代表压强或温度。下图A表示L一定时,NO(g)的平衡转化率随X的变化关系。X代表的物理量是______。判断L1、L2的大小关系______,并简述理由:______________________________。

(3)实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2) ·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数______(填“>”、“<”或“=”)k逆增大的倍数。
②若在2 L的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则k正︰k逆 =__________。(保留一位小数)
II. 有人利用反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH = 34.0 kJ·mol1,用活性炭对NO进行吸附。现在密闭容器中加入足量的C和一定量的NO气体并在催化剂作用下发生反应,经相同时间测得NO的转化率随温度的变化如图B所示。由图可知最高转化率对应温度为450℃。低于450℃时,NO的转化率______(填“是”或者“不是”)对应温度下的平衡转化率,判断理由是________________________;高于450OC时,NO的转化率降低的可能原因是___________(填标号)
N2(g)+CO2(g) ΔH = 34.0 kJ·mol1,用活性炭对NO进行吸附。现在密闭容器中加入足量的C和一定量的NO气体并在催化剂作用下发生反应,经相同时间测得NO的转化率随温度的变化如图B所示。由图可知最高转化率对应温度为450℃。低于450℃时,NO的转化率______(填“是”或者“不是”)对应温度下的平衡转化率,判断理由是________________________;高于450OC时,NO的转化率降低的可能原因是___________(填标号)
A.催化剂活性降低 B.平衡常数变小 C. 反应活化能增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加徳罗常数的值,下列说法正确的是
A.电解精炼铜时转移了NA个电子,阳极溶解了32g铜
B.室温下,pH=3的NH4Cl溶液中,由水电离的OH-浓度为10-11mol/L
C.12.0g熔融的NaHSO4中含有的阳离子数为0.1NA
D.常温下,1mol/LFe2(SO4)3溶液中,Fe3+和SO42-的离子总数是NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A.向0.1mol/LCH3COOH溶液中加入少量水,溶液中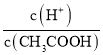 减小
减小
B.将CH3COONa溶液从20℃升温至30℃,溶液中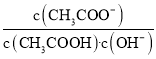 增大
增大
C.向盐酸中加入氨水至中性,溶液中c(NH4+):c(Cl-)>1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中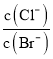 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关W、X、Y、Z、R五种元素的叙述正确的是( )
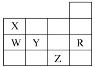
A. 常温下,Z的单质为气态物质
B. Y、Z的阴离子的电子层结构都与R原子的相同
C. W的氢化物的稳定性要比X的强
D. Y的元素的非金属性比W元素强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素,它们均为短周期元素。已知A是非金属性最强的元素,且E与A同族;金属B的原子核内质子数比前一周期的同族元素多8,其单质不能从CuSO4溶液中置换出Cu;C元素有三种同位素,Cl、C2、C3,C1的质量数分别为C2、C3的1/2和1/3;D的气态氢化物溶于水后显碱性。
(1)写出B元素的离子结构示意图__________;C2粒子的符号:__________;
(2)B、E两种元素形成化合物的电子式:___________;
(3)A、E两种元素形成的氢化物沸点较高的是:____________(用化学式表示),其原因是__________________________;
(4)写出D的气态氢化物与其最高价氧化物的水化物反应的离子方程式________;
(5)写出D的氢化物(过量)与E的单质发生氧化还原反应生成一种单质和一种盐的化学方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数大于4的主族元素Xm+、Yn-的离子核外电子层结构相同,则关于X、Y两元素的叙述正确的是
A. X的原子序数小于Y的原子序数 B. X、Y的核电荷数之差是(m-n)
C. X和Y处于同一周期 D. Y元素与X元素的族序数之差是8-(m+n)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 是原子序数依次增大的五种短周期元素,且
是原子序数依次增大的五种短周期元素,且![]() 是元素周期表中原子半径最小元素,
是元素周期表中原子半径最小元素,![]() 、
、![]() 相邻,
相邻,![]() 元素可以与
元素可以与![]() 、
、![]() 、
、![]() 元素分别形成甲、乙、丙三种物质,且甲、乙均为10电子化合物,丙为18电子双原子化合物。
元素分别形成甲、乙、丙三种物质,且甲、乙均为10电子化合物,丙为18电子双原子化合物。![]() 元素原子的最外层电子数与核外电子层数相等。已知:甲+丙→丁。下列说法正确的是
元素原子的最外层电子数与核外电子层数相等。已知:甲+丙→丁。下列说法正确的是
A.简单离子半径:![]()
B.![]() 与
与![]() 两种元素共同形成的10电子微粒有3种
两种元素共同形成的10电子微粒有3种
C.![]() 元素在元素周期表中的位置是第二周期第ⅡA族
元素在元素周期表中的位置是第二周期第ⅡA族
D.丁物质由非金属元素组成,只含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mLNaOH溶液中逐滴加入![]() 醋酸溶液,滴定曲线如图所示。下列判断正确的是
醋酸溶液,滴定曲线如图所示。下列判断正确的是
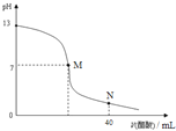
A.在M点,两者恰好反应完全
B.滴定前,酸中![]() 等于碱中
等于碱中![]()
C.NaOH溶液的物质的量浓度为![]()
![]()
D.在N点,c(CH3COO-)> c(Na+)>c(H+)> c(CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com