
【题目】下列关于化学反应限度的说法中正确的是
A.改变外界条件不能改变化学反应的限度
B.当某反应在一定条件下达到反应限度时即达到了化学平衡状态
C.当某反应体系中气体的压强不再改变时,该反应一定达到了反应限度
D.当某反应达到限度时,反应物和生成物的浓度一定相等
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在100 ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液的pH=________。
(2)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的主要离子方程式为_______________________________________,由水电离出的
c(OH-)=________mol·L-1。
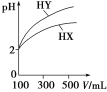
(3)体积均为100 mL、pH均为2的一元酸HX、HY,加水稀释过程中pH与溶液体积的关系如图所示,则HX是________(填“强酸”或“弱酸”),理由是_________________________。
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离平衡常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25 ℃时,等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,溶液的pH由大到小的顺序为______________________(填化学式)。
②25 ℃时,在0.5 mol·L-1的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列常见物质的俗名与化学式对应正确的是
A. 熟石灰—— Ca(OH)2B. 铁红—— Fe3O4
C. 光导纤维—— SiD. 酒精—— CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.硫酸、纯碱、碳酸氢钠和生石灰分别属于酸、碱、盐和氧化物
B.用丁达尔效应区别FeCl3溶液和Fe(OH)3胶体
C.生石灰与水混合的过程只发生物理变化
D.H2O、CH3COOH、Cu(NH3)4SO4均含有氧,都是氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有弱酸HA及其钠盐NaA的混合溶液,在化学上可用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
(1)现将0.04 mol·L-1HA溶液和0.02 mol·L-1NaOH溶液等体积混合,得到缓冲溶液。
①若HA为HCN,则该溶液显碱性,该溶液显碱性的原因是___________________,溶液中c(Na+)__________c(CN-)(填“<”、“=”或“>”),你得出该结论的依据是________________________。
②若HA为CH3COOH,则该溶液显酸性。溶液中所有的离子按浓度由大到小排列为_______________________。
(2)Na2HPO4/Na3PO4的混合溶液可以将体系的pH稳定在11.3~13.3之间,是一种常用的缓冲溶液。下列有关该缓冲溶液的说法或关系式错误的是__________。
A.加入少量强碱,发生反应:HPO![]() +OH-===PO
+OH-===PO![]() +H2O
+H2O
B.加入少量强酸,发生反应:HPO![]() +H+===H2PO
+H+===H2PO![]()
C.c(Na+)+c(H+)=c(OH-)+c(H2PO![]() )+2c(HPO
)+2c(HPO![]() )+3c(PO
)+3c(PO![]() )
)
D. ![]() c(Na+)>c(PO
c(Na+)>c(PO![]() )+c(HPO
)+c(HPO![]() )+c(H2PO
)+c(H2PO![]() )+c(H3PO4)>
)+c(H3PO4)> ![]() c(Na+)
c(Na+)
(3)一定浓度的NaHCO3和Na2CO3的混合溶液也是一种缓冲溶液,写出在这种溶液中加入少量NaOH或盐酸时发生反应的离子方程式:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和。甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1 mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M。
请回答下列问题:
(1)戊离子的结构示意图为________。
(2)戊的单质与X反应生成的Y和Z的物质的量之比为2∶4,反应中被氧化的物质与被还原的物质的物质的量之比为________。
(3)写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:__________________。
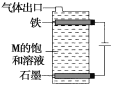
(4)按如图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:____________________________。将充分电解后所得溶液逐滴加入酚酞溶液中,观察到的现象是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的元素(不考虑稀有气体的原子半径);Y的单质呈黄色,常见于火山口附近。下列说法正确的是

A. 氧化物的水化物酸性:Y<Z
B. 简单离子半径:W<X<Z
C. W的简单气态氢化物的沸点高于同族其它元素的简单气态氢化物
D. 将标况下等体积的Z单质与Y的低价氧化物同时通入品红溶液中,品红溶液迅速褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L的密闭容器中,发生3A(g)+B(g)2C(g)的反应,若最初加入A和B都是4mol,1min内,测得υ(A)=1.2mol·L﹣1·min﹣1,则此时容器中B的物质的量是
A. 1.6mol B. 2.8mol C. 3.2mol D. 3.6mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com