
【题目】下列指定反应的化学方程式或离子方程式书写正确的是
A.1—溴丙烷与氢氧化钾的乙醇溶液共热:CH3CH2CH2Br+KOH![]() CH3CH2CH2OH+KBr
CH3CH2CH2OH+KBr
B.将乙酸乙酯、H218O和稀硫酸充分混合并加热:CH3COOCH2CH3+H218O![]() CH3COOH+CH3CH218OH
CH3COOH+CH3CH218OH
C.甲烷碱性燃料电池的负极反应式:CH4-8e-+8OH-=CO2+6H2O
D.用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-![]() CH3COO-+NH4++3NH3+2Ag↓+H2O
CH3COO-+NH4++3NH3+2Ag↓+H2O
【答案】D
【解析】
A. 1—溴丙烷与氢氧化钾的乙醇溶液共热,主要发生消去反应,正确的方程式为CH3CH2CH2Br+KOH![]() CH3CH=CH2↑+KBr+H2O,A错误:
CH3CH=CH2↑+KBr+H2O,A错误:
B. 将乙酸乙酯、H218O和稀硫酸充分混合并加热,发生水解反应,H218O中的18O应进入乙酸中,正确的方程式为CH3COOCH2CH3+H218O![]() CH3CO18OH+CH3CH2OH,B错误;
CH3CO18OH+CH3CH2OH,B错误;
C. 甲烷碱性燃料电池的负极反应式应为:CH4-8e-+10OH-=CO32-+7H2O,C错误;
D. 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-![]() CH3COO-+NH4++3NH3+2Ag↓+H2O,D正确。
CH3COO-+NH4++3NH3+2Ag↓+H2O,D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】美托洛尔可用于治疗各类型高血压及心绞痛,其一种合成路线如下:

已知:①CH3COCH2R![]() CH3CH2CH2R
CH3CH2CH2R
② B- F苯环上均只有两个取代基
回答下列问题:
(1)A的化学名称是___,C中含氧官能团的名称是___
(2)E→F的反应类型是___,G的分子式为___。
(3)D的结构简式为___。
(4)反应B→C的化学方程式为___
(5)芳香族化合物W是G的同分异构体,W能发生水解反应,核磁共振氢谱有4组峰,峰面积之比为9:3:2:2,写出一种符合要求的W的结构简式:___.
(6)4一苄基苯酚(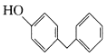 )是一种药物中间体,请设计以苯甲醇和苯酚为原料制备4-苄基苯酚的合成路线:______(无机试剂任用)。
)是一种药物中间体,请设计以苯甲醇和苯酚为原料制备4-苄基苯酚的合成路线:______(无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验设计和操作中必须十分重视安全问题和环境保护问题。下列实验问题处理方法不正确的是( )
①配制稀硫酸时,可先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸
②在气体发生装置上直接点燃一氧化碳气体时,必须先检验一氧化碳气体的纯度。最简单的方法是用排空气的方法收集一试管气体,点燃气体,听爆鸣声
③实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
④给试管中的液体加热时不时移动试管,以免暴沸伤人
⑤不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
A.②③B.②⑤C.③④D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灼热的焦炭与水蒸气反应所得产物为H2、CO和少量CO2,为了检验产物中的H2和CO(设气体均被充分吸收),设计如下实验装置。下列有关说法错误的是
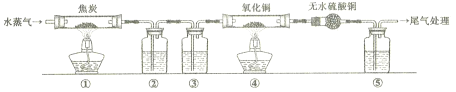
A. 为了实验安全,应先点燃①处酒精灯,后点燃④处酒精灯
B. ②、③、⑤中依次盛装氢氧化钠溶液、浓硫酸和澄清石灰水
C. ④中黑色固体变红色,即可证明产物中一定含有H2和CO中的一种或两种
D. 若用碱石灰替换无水硫酸铜,也可以达到检验H2和CO目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1 mol X气体和0.5 mol Y气体混合于2 L密闭容器中,发生如下反应:3X(g)+Y(g)![]() nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
(1)前2 min内,用X表示的平均反应速率________;
(2)2 min末时Y的转化率________;
(3)化学方程式中Z的化学计量数n________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,反应:A(s)+2B(g)![]() C(g) +D(g)。下列不能表明反应
C(g) +D(g)。下列不能表明反应
达到平衡状态的是( )。
A.气体的压强不变B.气体平均相对分子质量不变
C.气体的密度不变D.B物质的量浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子均属于极性分子且中心原子均为sp3杂化的是()
A. NH3、H2O B. SO2、SCl2 C. PCl3、SO3 D. CH4、P4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积固定的密闭容器中,加入1 molCO2,2 molH2进行吸热反应![]() ,下列情况能说明反应一定达到平衡状态的是
,下列情况能说明反应一定达到平衡状态的是
A. 容器内混合物的相对分子质量不再随时间改变B. 生成1 mol H—H键的同时消耗1 mol CO2
C. 容器内的气体总压强不再随时间改变D. 容器内CO2与H2的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莱佐卡因(对氨基苯甲酸乙酯)是目前常用的止痛药物之一。实验室通过对氨基苯甲酸和乙醇发生酯化反应制备莱佐卡因的一种方法如下:
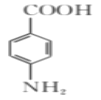 +CH3CH2OH
+CH3CH2OH![]()
 +H2O
+H2O
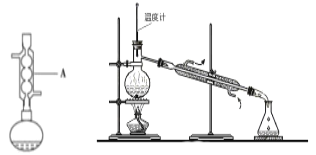
实验过程:在圆底烧瓶中加入0.400g(0.0029mol)对氨基苯甲酸和0.082mol乙醇,振荡溶解,将烧瓶置于冰水浴中并加入0.220mL浓硫酸;将烧瓶中的混合物用水浴加热回流1h,并不断振荡。分离提纯:冷却后,分批加入10%NaHCO3溶液直至无明显气泡产生,再加入少量NaHCO3溶液至PH≈9,将混合液转移至分液漏斗中,用乙醚(常温下难溶于水,沸点34.6℃,密度0.714g·cm-3)分两次萃取并分液,向分液后所得到的醚层中加入无水硫酸钠,蒸出乙醚,冷却结晶,最终得到产物0.2000g。回答下列问题:
(1)仪器A的名称为______________。
(2)“将烧瓶置于冰水浴”中的原因是______________。
(3)给烧瓶中的液体加热时,为防止液体暴沸,须向烧瓶中加入______________。
(4)分液漏斗在使用之前必须进行的操作是__________。萃取后静置,乙醚层位于______(填“上层”或“下层”)。分液后,向醚层中加入无水硫酸钠的作用是______________。
(5)本实验中,莱佐卡因的产率是________%(精确到0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com